Ipercolesterolemia: nuove tecnologie farmacologiche
L’ ipercolesterolemia è un Killer silenzioso che ogni giorno causa tantissimi decessi per malattie cardiache e vascolari.
Numerosi e autorevoli studi hanno dimostrato che esiste una correlazione tra ipercolesterolemia e malattie cardiache e vascolari.
In particolare mi riferisco al colesterolo cattivo meglio conosciuto come colesterolo LDL.
Più semplicemente tanto più è alto il colesterolo cattivo LDL, maggiore sarà il rischio di avere un evento cardiovascolare (Infarto o Ictus).
Nella figura 1, si vede chiaramente che la riduzione della colesterolemia LDL è sempre associata a una riduzione del rischio cardiovascolare, questo vuol dire che tanto più manteniamo bassi i valori del colesterolo LDL, maggiore saranno i benefici per il nostro cuore.
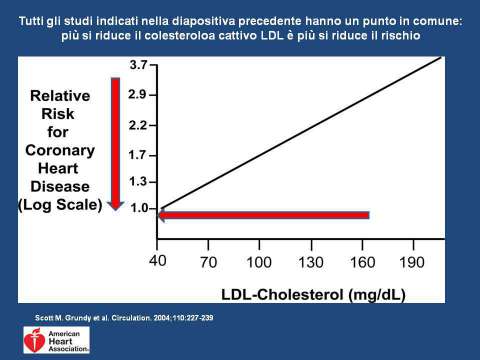
Quindi, quando facciamo le analisi del sangue, dobbiamo sempre considerare il Colesterolo LDL, insieme al Colesterolo Totale, ai Trigliceridi e colesterolo HDL (quello buono).
Nello studio dell’ ipercolesterolemia, non ha assolutamente senso richiedere solo uno di questi parametri, ma devono essere richiesti tutti e quattro contemporaneamente per avere un quadro completo del rischio cardiovascolare della persona in esame e iniziare una terapia idonea e personalizzata.
Premetto che esiste anche un altro tipo di colesterolo chiamato Lipoproteina (a) piccola che è una forma di colesterolo molto più aggressiva del colesterolo LDL, basti pensare che in persone che non hanno il colesterolo alto, ma hanno una Lipoproteina (a) piccola elevata rischiano di avere seri problemi cardiovascolari anche in età giovanile.
Consiglio sempre di dosare la Lipoproteina (a) piccola in tutti coloro hanno avuto storia di infarto anche in età giovanile (sotto ai 40 anni)
Attualmente non esistono farmaci per l’ ipercolesterolemia capaci di ridurre la Lipoproteina (a) piccola, i pazienti che presentano dei moderati valori, è possibile ridurre il rischio cardiovascolare riducendo il più possibile il colesterolo LDL, altrimenti in pazienti dove la Lipoproteina (a) piccola è molto elevata, l’unica opzione terapeutica possibile e il lavaggio del sangue. (plasmaferesi)
Ipercolesterolemia: terapie attuali
Pazienti che oltre al colesterolo cattivo LDL hanno anche altri fattori di rischio quali Fumo, Obesità, Ipertensione, Malattia Renale, Diabete, recente oppure storia di Infarto o altre malattie cardiache, familiarità per malattie cardiache, devono abbassare il loro colesterolo cattivo con un trattamento farmacologico.
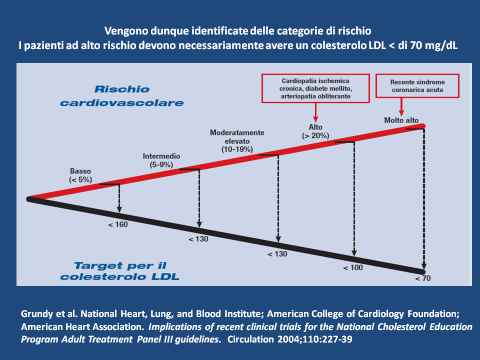
I principali farmaci attualmente in commercio più utilizzati nella terapia dell’ ipercolesterolemia , sono le statine che bloccano la sintesi del colesterolo LDL a livello epatico.
Esistono diverse statine che differiscono sia per struttura chimica, per dosaggio ed potenza.
Altro farmaco è l’ ezetimibe, ha un meccanismo d’azione differente da quello della statina, inibisce l’assorbimento del colesterolo a livello intestinale, può essere utilizzato nella terapia dell’ ipercolesterolemia , sia da solo che in combinazione con le statine.
La associazione statine con ezetimibe è utile quando:
- la sola statina non riesce a ridurre sufficientemente il colesterolo cattivo
- il paziente non tollera alti dosaggi di statina
- se si desidera evitare di somministrare alti dosaggi di statina in pazienti pediatrici oppure in pazienti con malattie renali o pazienti in trattamento con farmaci immunosoppressori o chemioterapici
statine” width=”480″ height=”360″ />
Se oltre al colesterolo i pazienti hanno anche elevati trigliceridi, i farmaci idonei sono i fibrati che possono essere utilizzati o da soli oppure in combinazione con statine ( con prudenza) oppure in associazione con omega 3.
Nella pratica clinica accade che alcuni pazienti presentano intolleranza ai farmaci appena descritti (dolore muscolare, aumento delle transaminasi ) e lo specialista è costretto a ridurre il dosaggio del farmaco con scarso controllo della colesterolemia LDL e in alcuni casi a sospenderlo, lasciando quindi il paziente esposto a rischio cardiovascolare.
Per fortuna sono disponibili nuovi farmaci (frutto di studi di Biologia Molecolare) utili per trattare l’ ipercolesterolemia con meccanismi d’azione completamente diversi ai farmaci sopra descritti.
Il primo farmaco che vi presento è un anticorpo monoclonale ( chiamato Evolocumab ) completamente umano che blocca la proteina PCSK9.
In breve si è visto che elevati livelli della proteina PCSK9 nel sangue impediscono lo smaltimento da parte del corpo del Colesterolo cattivo LDL, la somministrazione di un anticorpo monoclonale altamente specifico che si lega solamente alla proteina PCSK9 disattivandola, riduce significativamente i livelli del Colesterolo cattivo LDL.
Il farmaco non viene assunto per via orale ma sottocute, tramite una piccola iniezione sotto la pelle mediante un apposito iniettore, l’iniezione è indolore, e deve essere fatta una volta ogni 2 settimane o addirittura una volta al mese.
Cambia così il modo di assumere un farmaco per l’ ipercolesterolemia : non sarà più necessario assumerlo per via orale attraverso una compressa tutti i giorni, ma sottocute ogni 15 o 30 giorni riducendo i fastidi gastrointestinali e non solo.
Le indicazioni autorizzate sono:
- in pazienti adulti con diagnosi di ipercolesterolemia primaria (familiare eterozigote e non familiare) o dislipidemia mista
- in combinazione con statine o con altre terapie ipolipemizzanti in pazienti in trattamento che non riescono a raggiungere i target di C-LDL con statine al massimo dosaggio tollerato
- in monoterapia o in combinazione con altre terapie ipolipemizzanti in pazienti intolleranti alle statine o per i quali l’uso di statine è controindicato
- per il trattamento di adulti e adolescenti dai 12 anni in poi con ipercolesterolemia familiare omozigote in combinazione con altre terapie ipolipemizzanti.
Questo farmaco rappresenta un’opzione terapeutica di estremo valore per i pazienti ad alto rischio cardiovascolare e per garantire un rapido accesso al farmaco per i pazienti che possono beneficiarne verrà attivato subito l’iter di richiesta della rimborsabilità in Italia.
Per chi vuole approfondire può leggere il seguente articolo
(First-in-class treatment to lower cholesterol Repatha® to offer therapy for patients unable to control high cholesterol with currently available treatment )
Un’altra classe di farmaci frutto sempre di studi di biologia molecolare, sono rappresentati da oligonucleotidi antisenso (ASO) vengono chiamati così per la loro sequenza complementare all’RNA senso.
La somministrazione di questi farmaci antisenso a singolo filamento una volta iniettati al paziente per via sottocutanea (indolore) con frequenza settimanalmente tramite un apposito iniettore, hanno la capacità di spegnere selettivamente l’interruttore che invia il segnale al corpo di produrre colesterolo, di conseguenza si osserverà ad una riduzione significativa del Colesterolo cattivo LDL. (Figura 5)
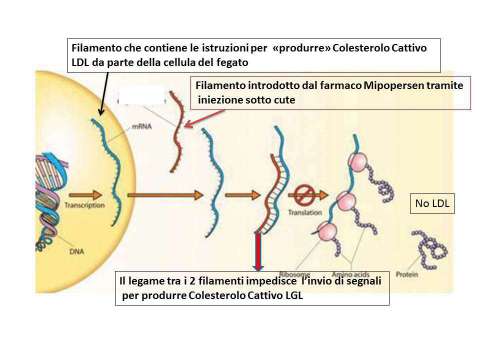
Per usare un linguaggio più tecnico: Il Mipomersen è il nome dell’ oligonucleotide antisenso di seconda generazione contro l’apolipoproteina B 100 (apoB100) umana.
L’apoB100 fornisce la struttura proteica per tutte le particelle lipidiche aterogene circolanti nel sangue.
L’uso di Kynamro (Mipomersen) riduce i livelli epatici di mRNA per l’apoB100 in maniera dose-dipendente, seguita da una riduzione dei livelli ematici di LDL-C, numero di particelle LDL, TG e lipoproteina (a) (Lp(a)).
Un altro nuovo farmaco ampiamente studiato è un inibitore chiamato Lomitapide (Lojuxta) selettivo della proteina microsomiale di trasporto dei trigliceridi (MTP), una proteina intracellulare di trasporto dei lipidi che si trova nel lume del reticolo endoplasmatico ed è responsabile del legame e del movimento di molecole singole di lipidi attraverso le membrane.
L’MTP svolge un ruolo nell’assemblaggio dell’apo B contenente lipoproteine nel fegato e nell’intestino. L’inibizione dell’MTP riduce la secrezione di lipoproteine e le concentrazioni circolanti di lipidi trasportati da lipoproteine, inclusi colesterolo e trigliceridi.( figura 6)
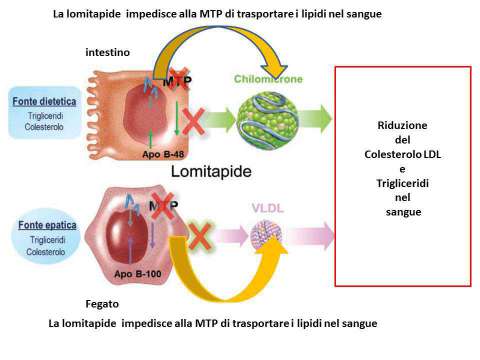
Per usare termini più semplici questo nuovo farmaco blocca quella proteina che trasporta i trigliceridi (che si accumulano sia nel fegato che nell’intestino) nel sangue. Immaginiamo di avere tanti camion, ma non c’è nessuno che può caricarli, di conseguenza il loro carico rimane vuoto.
Questo farmaco che vi ho appena illustrato, a differenza degli altri due sopracitati viene assunto come compressa per via orale.
Vorrei concludere questa breve rassegna, segnalandovi una nuova statina la Pitavastatina. Questa statina disponibile in Italia, ha la caratteristica di essere efficiente (nel ridurre il Colesterolo cattivo LDL) a dosaggi bassissimi 1 o al massimo 2 mg al giorno. Attualmente solamente la Rosuvastatina è disponibile a partire da 5 mg al giorno.
La possibilità di usare bassissimi dosaggi di statina apre finalmente un nuovo scenario terapeutico in pazienti “delicati” quali bambini, adulti che non tollerano alti dosaggi di statine, anziani, pazienti sottoposti a multiple terapie farmacologiche o coloro che assumono farmaci particolari come immunosoppressori, anticorpi monoclonali, farmaci biologici ect.
BIBLIOGRAFIA
- PCSK9 inhibitors – past, present and future. – Reiner Z. – Expert Opin Drug Metab Toxicol. 2015 Aug 3:1-5
- Are PCSK9 Inhibitors the Next Breakthrough in the Cardiovascular Field? – Giugliano RP, Sabatine MS. – J Am Coll Cardiol. 2015 Jun 23;65(24):2638-51. doi: 10.1016/j.jacc.2015.05.001. Review.
- Efficiency and safety of proprotein convertase subtilisin/kexin 9 monoclonal antibody on hypercholesterolemia: a meta-analysis of 20 randomized controlled trials. – Li C, Lin L, Zhang W, Zhou L, Wang H, Luo X, Luo H, Cai Y, Zeng C. – J Am Heart Assoc. 2015 Jun 15;4(6):e001937. doi: 10.1161/JAHA.115.001937
- Management of patients with familial hypercholesterolaemia. – Reiner Z. – Nat Rev Cardiol. 2015 Jun 16. doi: 10.1038/nrcardio.2015.92. [Epub ahead of print] Review
- Efficacy and safety of the proprotein convertase subtilisin/kexin type 9 inhibitor alirocumab among high cardiovascular risk patients on maximally tolerated statin therapy: The ODYSSEY COMBO I study. – Kereiakes DJ, Robinson JG, Cannon CP, Lorenzato C, Pordy R, Chaudhari U, Colhoun HM. – Am Heart J. 2015 Jun;169(6):906-915.e13. doi: 10.1016/j.ahj.2015.03.004. Epub 2015 Mar 13
- PCSK9 inhibitors on the way. – Patel KR. – Manag Care. 2014 Nov;23(11):43
- Homozygous autosomal dominant hypercholesterolemia: prevalence, diagnosis, and current and future treatment perspectives. – Sjouke B, Hovingh KG, Kastelein JJ, Stefanutti C. – Curr Opin Lipidol. 2015 Apr 16.
- Recent advances in the understanding and care of familial hypercholesterolaemia: significance of the biology and therapeutic regulation of proprotein convertase subtilisin/kexin type 9. – Page MM, Stefanutti C, Sniderman A, Watts GF. – Clin Sci (Lond). 2015 Jul;129(1):63-79. doi: 10.1042/CS20140755.Review.
- Familial Hypercholesterolemia: a Review of the Natural History, Diagnosis, and Management. – Najam O, Ray KK. – Cardiol Ther. 2015 Jun;4(1):25-38. doi: 10.1007/s40119-015-0037-z. Epub 2015 Mar 14
- Homozygous familial hypercholesterolemia] – KayikioÄŸlu M. – Turk Kardiyol Dern Ars. 2014 Oct;42 Suppl 2:47-55. Review. Turkish.
- The genetics of familial hypercholesterolemia and emerging therapies. – Vogt A. – Appl Clin Genet. 2015 Jan 28;8:27-36. doi: 10.2147/TACG.S44315. eCollection 2015.Review
- Mipomersen is a promising therapy in the management of hypercholesterolemia: a meta-analysis of randomized controlled trials. – Li N, Li Q, Tian XQ, Qian HY, Yang YJ. – Am J Cardiovasc Drugs. 2014 Oct;14(5):367-76. doi: 10.1007/s40256-014-0077-0.Review
- Safety and tolerability of injectable lipid-lowering drugs: a review of available clinical data. – Cicero AF, Tartagni E, Ertek S. – Expert Opin Drug Saf. 2014 Aug;13(8):1023-30. doi: 10.1517/14740338.2014.932348. Epub 2014 Jun 24.Review.
- Treating homozygous familial hypercholesterolemia in a real-world setting: Experiences with lomitapide. – Roeters van Lennep J, Averna M, Alonso R. – J Clin Lipidol. 2015 Jul-Aug;9(4):607-17. doi: 10.1016/j.jacl.2015.05.001. Epub 2015 May 14
- Evaluation of the effects of the weak CYP3A inhibitors atorvastatin and ethinyl estradiol/norgestimate on lomitapide pharmacokinetics in healthy subjects. – Patel G, King A, Dutta S, Korb S, Wade JR, Foulds P, Sumeray M. – J Clin Pharmacol. 2015 Jun 26.
- Treatment of primary hypertriglyceridemia states–General approach and the role of extracorporeal methods. – Stefanutti C, Julius U. – Atheroscler Suppl. 2015 May;18:85-94
- Mipomersen and lomitapide: Two new drugs for the treatment of homozygous familial hypercholesterolemia. – Gouni-Berthold I, Berthold HK. – Atheroscler Suppl. 2015 May;18:28-34. doi: 10.1016/j.atherosclerosissup.2015.02.005
- The lipid-lowering effects of lomitapide are unaffected by adjunctive apheresis in patients with homozygous familial hypercholesterolaemia – a post-hoc analysis of a Phase 3, single-arm, open-label trial. – Stefanutti C, Blom DJ, Averna MR, Meagher EA, Theron Hd, Marais AD, Hegele RA, Sirtori CR, Shah PK, Gaudet D, Vigna GB, Sachais BS, Di Giacomo S, du Plessis AM, Bloedon LT, Balser J, Rader DJ, Cuchel M; Phase 3 HoFH Lomitapide Study Investigators. – Atherosclerosis. 2015 Jun;240(2):408-14
- Statin intolerance: diagnosis and remedies. – Pirillo A, Catapano AL. – Curr Cardiol Rep. 2015 May;17(5):27.
- Lomitapide. – Goulooze SC, Cohen AF, Rissmann R. – Br J Clin Pharmacol. 2015 Aug;80(2):179-81
- Homozygous familial hypercholesterolemia. – KayikçioÄŸlu M. – Turk Kardiyol Dern Ars. 2014 Oct;42 Suppl 2:47-55
- Long-term clinical results of microsomal triglyceride transfer protein inhibitor use in a patient with homozygous familial hypercholesterolemia. – Raper A, Kolansky DM, Sachais BS, Meagher EA, Baer AL, Cuchel M. – J Clin Lipidol. 2015 Jan-Feb;9(1):107-12.
- Pitavastatin in children. – Daniels SR. – J Pediatr. 2015 Aug;167(2):219-21.
- Treatment options for dyslipidemia in chronic kidney disease and for protection from contrast-induced nephropathy. – Athyros VG, Tziomalos K, Karagiannis A. – Expert Rev Cardiovasc Ther. 2015 Jul 23:1-8
- Stabilization of atherosclerotic plaque by pitavastatin in Watanabe heritable hyperlipidemic rabbits: A serial tissue-characterizing intravascular ultrasound study. – Haruta H, Hiro T, Mitsumata M, Takayama T, Sudo M, Li Y, Takahashi R, Taniguchi Y, Shiomi M, Hirayama A. – J Cardiol. 2015 Jul 17.
- The effect of food on the pharmacokinetic properties and bioequivalence of two formulations of pitavastatin calcium in healthy Chinese male subjects. – Shang D, Deng S, Yao Z, Wang Z, Ni X, Zhang M, Hu J, Lu H, Zhu X, Huang W, Qiu C, Wen Y. – Xenobiotica. 2015 Jul 17:1-6.
- Pitavastatin: Other statin to be used and monitored. – Mora Cuadrado N. – Rev Esp Enferm Dig. 2015 Jul 14
- A New Therapeutic Modality for Acute Myocardial Infarction: Nanoparticle-Mediated Delivery of Pitavastatin Induces Cardioprotection from Ischemia-Reperfusion Injury via Activation of PI3K/Akt Pathway and Anti-Inflammation in a Rat Model. – Nagaoka K, Matoba T, Mao Y, Nakano Y, Ikeda G, Egusa S, Tokutome M, Nagahama R, Nakano K, Sunagawa K, Egashira K. – PLoS One. 2015 Jul 13;10(7):e0132451
- A Trial of Pitavastatin Versus Rosuvastatin for Dyslipidemia in Chronic Kidney Disease. – Abe M, Maruyama N, Maruyama T, Okada K, Soma M. – J Atheroscler Thromb. 2015 Jul 3
- Statin treatment alters serum n-3 to n-6 polyunsaturated fatty acids ratio in patients with dyslipidemia. – Nozue T, Michishita I. – Lipids Health Dis. 2015 Jul 7;14(1):67
- Differential Effects of Atorvastatin and Pitavastatin on Inflammation, Insulin Resistance, and the Carotid Intima-Media Thickness in Patients with Dyslipidemia. – Nakagomi A, Shibui T, Kohashi K, Kosugi M, Kusama Y, Atarashi H, Shimizu W. – J Atheroscler Thromb. 2015 Jun 17
- Pharmacokinetic Properties of Single- and Multiple-Dose Pitavastatin Calcium Tablets in Healthy Chinese Volunteers. – Luo Z, Zhang Y, Gu J, Feng P, Wang Y. – Curr Ther Res Clin Exp. 2015 Mar 3;77:52-7
- Efficacy and Safety of Pitavastatin in Children and Adolescents at High Future Cardiovascular Risk. – Braamskamp MJ, Stefanutti C, Langslet G, Drogari E, Wiegman A, Hounslow N, Kastelein JJ; PASCAL Study Group. – J Pediatr. 2015 Aug;167(2):338-343
- Inhibitory effect of statins on inflammation-related pathways in human abdominal aortic aneurysm tissue. – Yoshimura K, Nagasawa A, Kudo J, Onoda M, Morikage N, Furutani A, Aoki H, Hamano K. – Int J Mol Sci. 2015 May 18;16(5):11213-28


