Mandarino
Tratto da “Piante Medicinali – Chimica, Farmacologia e Terapa” di R. Benigni, C. Capra e P.F.Cattorini
[Citrus nobilis (Lour.) Andrews – Fam. Rutacee/Aurantioidee/Citrinee] (Sin. – Citrus nobile Risso – Citrus deliciosa Ten. – Citrus nobilis var. deliciosa (Swingle) Guillamin – Citrus madurensis Lour.)
Mandarino- Ultimo aggiornamento pagina: 27/02/2018
Indice dei contenuti
- Generalità
- Componenti principali
- Proprietà farmacologiche
- Estratti e preparati vari
- Preparazioni usuali e Formule
- Bibliografia
Generalità

Etimologia – Citrus, nome latino, dal greco kitron.
nobilis o nobile – nel senso di eccellente, per il gusto delicato.
deliciosa – per il sapore delicato.
madurensis – perchè alligna nell’isola di Madura (nord di Giava).
Mandarino – Il vocabolo, secondo alcuni Autori, deriva dal sànscrito mantrin = consigliere, dotto; secondo altri, dal portoghese mandarim = caporione, dal verbo mandar = comandare. Il vocabolo, come titolo degli alti funzionari del Celeste Impero, viene attribuito ai Portoghesi, alludendo al colore del frutto della tonalità di quello delle veste dei ministri cinesi.
All’isola Maurizio (Mascarene) corrisponde a màndara.
Nomi volgari – Tangerino (Mentone), mannarino, mannarinolo (nap.). Mandarinier (fr.), mandarin (spagn.), lim kinia, mandarina (Tripoli). tch’eng, soan tch'en, kin k’ieou, kon kio (cinese).
Habitat – Originaria dalla Cina e Cocincina ed ivi coltivata da tempi remoti, dove è detto Kan. Mou-nou. In Cina si trova nei territori di Fukien, Honan, Kiangsi, Chekiang, Kiangsu, Yunnan. Alligna nelle isole dell’Arcipelago della Sonda, dove lo vide coltivato il Rumphius (1750). Coltivato in India nel distretto di Khasia (Clarke) e in Birmania (Kurz). Ignota in Europa sino al principio del secolo XIX: introdotta nel 1828. Costa Azzurra (Nizza). Coltivata all’Isola Mauritius, in Sicilia, a Malta, nelle Azzorre, a Tripoli, in Brasile e in U.S.A. (California).
Arboscello (3 m.) molto ramificato.
Parte usata – La corteccia del frutto.
Componenti principali
Olio essenziale: a) (dai frutti interi) 0,75-0,85 % (Sicilia e Calabria), 0,2% (Brasile) (1); b) (dal pericarpo) 1,8-2,5%(Italia) (2).
La produzione dell’olio dei frutti del Citrus nobilis var. deliciosa Swingle («tangerine») della Florida è di circa 0,1% di olio dai frutti interi (1).
Durante la maturazione del frutto il contenuto di olio essenziale diminuisce (1) (3) [dallo 0,895% allo 0,338 % del frutto intero, secondo le analisi di Pico (4)] e pertanto la raccolta dei frutti per l’espressione della essenza è fatta prima della maturazione: in Italia dalla fine di ottobre alla fine di novembre. I frutti di piccole dimensioni danno maggiore rendimento di olio rispetto ai frutti più voluminosi (3) (4).
La composizione chimica dell’olio essenziale di Mandarino italiano, come è stato dimostrato dall’esito delle analisi di Nelson (5), differisce da quella del «tangerine» di Florida. La differenza principale consiste nella presenza dell’estere metilico dell'acido metilantranilico nell'olio italiano, presenza che conferisce a quest'ultimo la fluorescenza e l'odore caratteristici.
Nell'olio essenziale italiano sono stati identificati i seguenti costituenti:
— d-limonene (98%) (6), dl-limonene (dipentene) (7), a-pinene (26), b-pinene, g-pinene, terpinolene (26) (27).
— linalolo, terpineolo, nerolo, acetati di linalile e di terpinile (26), p-cimolo (26) (27).
— estere metilico dell'acido metilantranilico C9H11O2N, trovato da Walbaum (8). Nell'olio italiano si trova solo nelle proporzioni dell’1 %, ma è il componente odoroso più importante dell'essenza.
— aldeidi 0,62-0,79% (media 0,66%) espresse in aldeide decilica (analisi di 9 campioni di olio essenziale genuino di Sicilia e di Calabria) (9) (10). Sono state isolate le aldeidi ottilica (9), nonilica, decilica (9) (11), dodecilica, citrale e citronellale (9).
— residuo fisso 2,4-3,5%, secondo Gildemeister e Hoffmann (12), 1,9-4,2% (media 2,95 %), secondo Riganesis (9). Nel residuo fisso di olio italiano è stata riconosciuta la presenza della tangeretina (13) C20H20O7. Separata per la prima volta dal residuo dell’olio di Citrus nobilis var. deliciosa della Florida da Nelson (14), essa è stata in un primo tempo indicata da Goldsworthy e Robinson (15) quale 3,4’,5,6,7-pentametossiflavone e successivamente dagli stessi AA. (16) riconosciuta invece identica al 4’,5,6,7,8-pentametossiflavone (poncanetina).
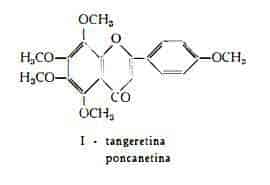
Nell’olio essenziale dei frutti di Florida (Dancy «tangerine») sono
stati trovati i seguenti componenti:
— d-limonene 95,75% dell’olio ed un altro idrocarburo identificabile probabilmente con il cadinene (5).
— aldeidi, 0,8-1,7% calcolate come aldeide decilica (1), che Nelson (5) ha identificate con le aldeidi ottilica, decilica e citrale (?).
— gli alcooli linalolo, citronellolo (?) ed altri non identificati, in parte liberi ed in parte presenti in forma di esteri (5),
— residuo fisso 2,3-4,7% (1), Nel residuo, formatosi nell’olio conservato a bassa temperatura, il flavonoide tangeretina (0,3-0,35% nell’olio totale) (14), già descritto sopra tra i componenti dell’olio di Mandarino italiano.
Altri componenti del pericarpo del Mandarino oltre all’olio essenziale:
— i pigmenti flavonoidi poncanetina, già nominata sopra, e nobiletina (3’,4’5,6,7,8-esametossiflavone), C21H22O8, (16 a) (16b), i carotinoidi criptoxantina, C40H56O, (17) (18), che costituisce la principale sostanza colorante del pericarpo del Mandarino (17), una sostanza ossicantaxantina-simile, licopene ed una frazione rubixantina-simile (18). Nel pericarpo fresco sono stati trovati mg 7,98-14,1% (in media mg 12,04%) di carotene (19).
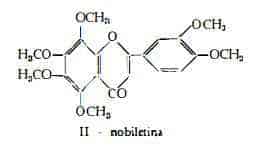
— vitamina A mg 20,05% nel pericarpo fresco (19).
— vitamina C, il cui contenuto è stato trovato in quantità variabile da 60 a 200 mg % nella buccia dei frutti raccolti in diverse zone dell’India dalla fine di novembre alla fine di gennaio (20). Durante il magazzinaggio il contenuto di vitamina C diminuisce nel frutto totale, ma risulta più stabile nel pericarpo (21).
— pectine 2,59% nei frutti di Spagna dopo espressione del succo (22).
— acido chinico (23).
— enzimi: perossidasi, ossidasi e catalasi (24).
Proprietà farmacologiche ed impiego terapeutico
Il Mandarino ha proprietà amaro-aromatiche, toniche ed eupeptiche. Impiegato nella tecnica galenica soprattutto come correttivo dell’odore e del sapore di preparati contenenti vitamine (K in particolare), sulfamidici, sostanze acide in generale, sostanze inodore e insipide e per l'aromatizzazione di molti preparati galenici (sciroppi, pozioni ecc.) (25).
La corteccia di Mandarino è largamente impiegata anche in liquoreria.
Estratti e preparati vari
a) Estratto fluido per tintura (g 1 = LVI gtt).
Dosi: g 2-10 pro die.
b) Estratto fluido per sciroppo (g 1 = XXXIII gtt).
Dosi: g 2-10 pro die.
Preparazioni usuali e formule galeniche
Tintura
Estratto fluido mandarino per tintura……………………………. g 20
Alcool di 70°……………………………………………………………….. g 80
(g 1-3 più volte pro die).
Sciroppo
Estratto fluido mandarino per sciroppo………………………… g 5
Sciroppo semplice F.U. ……………………………………………… g 95
(a cucchiai).
BIBLIOGRAFIA
(1) GUENTHER E., The Essential Oils, III ed., voi. III, pp, 336-345 – (2) DANESI e BOSCHI, Staz. Sper. Agr. Ita/., 28, 700, 1895: WEHMER C., Die Pftanzenstoffe, II, ed., p. 635 – (3) DI GIACOMO A., Riv. ital. ess. prof, 39, 39, 1957 – (4) PICO P. S., Idia, 123, 33, 1958; Chem. Abs., 53, 1642a, 1959 – (5) NELSON, Am. Perfumer, 29, 347, 1934 – (6) GILDEMEISTER e STEPHAN, Arch. Pharm., 235, 583, 1897; WEHMER C., Die Pftanzenstoffe, Il ed., p. 635 – (7) SCHIMMEL, Ber. Schimmel, ott. 35, 1901; ott. 39, 1911. (8) WALBAUM, J. prakt. Chem.. 62, 135, 1900 – (9) RIGANESIS M. D. e CALVARANO M., Ess.‘Deriv. Agrumari, 26, 167, 1956 – (10) RIGANESIS M. D., Riv. ita/. ess. prof., 38, 487, 1956 –
(II) SCHIMMEL, Semi-Annua/ Rep, II, 36, 1901 – (12) GILDEMEISTER E. e HOFFMANN F., Die Aetherische Oele, 3“ ed., vol. III, p. 111 – (13) RIGANESIS M. D., Ess.-Deriv. Agrumari, 26, 107, 1956 –
(14) NELSON E. K., J. Am. Chem. Soc., 56, 1392, 1934 – (15) GOLDSWORTHY L. J. e ROBINSON R., J. Chem. Soc., 46, 1937 – (16) GOLDSWORTHY L. J. e ROBINSON R., Chem. Jnd., 47, 1957 – (16a) TSENG K. F., J. Cht>m. Soc.. 1003, 1938: ROBINSON R. e TSENG K. F., J. Chem. Soc., 1004, 1938 – (16b) VENTURELLA P., BELLINO A. e CUSMANO S., Anii. Chimica, 51, 105, 1961 – (17) ZECH- MEISTER L e TUZSON P., Z. physio/. Chem., 240, 191, 1936; Ber., 69, 1878, 1936 – (l8) CURL H. L. e BAILEY G. F.. J. Agr. Food Chem., 5, 605, 1957; Chem. Abs., 51, 17010e, 1957 – (19) BORRELL S.. Ana/er Bromato/., 8, n. 2. 1956; Monit. farm. y terup., 62, 279, 1956 – (20) RIAZ-UR-RAHMAN e SADIQ ALI, Punfab Fruit J., 19, 30, 1955; Chem. Abs, 52, 14890d, 1958 – (21) METLITSKII L. V. e TSEKHOM- SKAYA V. M., Biokhim. P/odov i Ovoshchei. Akad. Nauk S.S.S.R.,lnst. Biokhim., Sbornik, 3, 163, 1955; Chem. Abs., 50, 2755b, 1956 – (22) FUERTES POLO C. e ROYO IRANZO J., lon, 14, 455 ,1954; Chem. Abs., 49, 6499h, 1955 – (23) TING S. V. e DESZYCK E. J., Nature, 183, 1404, 1959; Chem. Abs., 55. 839 f, 1961 – (24) AJON, Riv. ital. ess. prof., 8, 87, 1926 – (25) CAPRA C., Il Farmaco, 13, 500, 1958 – (26) CALVARANO M., Ess.-Deriv. Agrumari, 28, 107, 1958 – (27) LIBERTI A. e CARTONI G. P., Ricerca Sci., 28, 1192, 1958.

