Rabarbaro Rapontico
Tratto da “Piante Medicinali – Chimica, Farmacologia e Terapa” di R. Benigni, C. Capra e P.F.Cattorini
(Rheum Rhaponticum L. – Fam. Polygonacee)
Rabarbaro Rapontico- Ultimo aggiornamento pagina: 27/02/2018
Indice dei contenuti
- Generalità
- Componenti principali
- Proprietà farmacologiche
- Estratti e preparati vari
- Preparazioni usuali e Formule
- Bibliografia
Generalità

Etimologia – Rheum (ved. Rabarbaro cinese).
Rhaponticum – dal radicale Rha (radice) e l'aggettivo ponticum, da Pontus (il Ponto Eusino = mare ospitale, da euxeinos) (Pontus, da pontos = profondo e pontos = il Mar Nero e pontikos = del Mar Nero) , cioè della regione che è attorno al Mar Nero, compresa fra il Tanais (tanais), l'odierno Don, e il Rha (Volga).
Nomi volgari – Rapontico, reupontico, riobarbaro.
Pontischer Rhabarber (ted.), pontic rhubarb (ingl.), rhapontic (fr.).
Si distinguono due varietà: il Rhapontic exotique o d’Asie (il selvaggio) e rhubarbe de France, rhubarbe pontique indigène (il coltivato in Europa).
Habitat – Originario dall’Asia, Urali, Caucaso, monti subalpini della Siberia altaica, baicalica e trasbaicalica. Coltivato in Francia (Piccole Alpi della Provenza), in Inghilterra, in Svizzera (Davos), in Austria.
Pianta erbacea perenne.
Parti usate – Rizoma e radici.
Componenti principali
Composti antracenici in forma ridotta ed ossidata, liberi e combinati in forma glucosidica:
1) Crisofanolo (acido crisofanico) (ved. Rabarbaro cinese) nel Rheum Rhaponticum L. (1) (2) e nel Rheum undulatum L. (3).
2) Glucocrisarone, C21H20O10, è stato estratto dal Rh. Rhaponticum (4). Per idrolisi si scinde per dare la genina crisarone, C15H10O5, trovata anche in forma libera, ed una molecola di glucosio, la cui posizione nel glucoside non è stata determinata (4). La struttura I del crisarone è stata confermata per sintesi (5) (6):
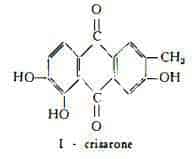
Il contenuto di derivati antracenici è risultato pari all’1,6 % nel Rabarbaro rapontico tedesco, secondo Tschirch (7), 1,89-2,49 % secondo Fairbairn e Lou (8), 2,12 % di cui circa 1 % di derivati antranolici, secondo Auterhoff (9).
Il confronto tra il titolo chimico e l’attività farmacologica dei rizomi di Rabarbaro cinese e di R. rapontico finlandese ha messo in evidenza che un R. cinese di 30-40 % più ricco di derivati antracenici, secondo l'esito dei saggi chimici, era per il 100 % più attivo biologicamente rispetto al R. rapontico (10).
Oltre a composti antracenici il Rabarbaro rapontico contiene un particolare glucoside, raponticina (rapontina, ponticina) (11), C21H24O9, che per idrolisi produce una molecola di glucosio e l'aglucone rapontigenina (pontigenina), C15H14O4 (12). La rapontigenina, trovata anche in forma libera nei rizomi del Rh. undulatum L. (3), è stata identificata con il 3,3',5'-triossi-4-metossistilbene (13) (14).
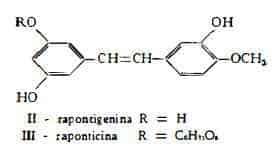
La raponticina è stata estratta dal Rh. Rhaponticum L. in quantità sino al 5,5 % (15). Tschirch e Cristofoletti (1) hanno segnalato un contenuto dell'1,42% e Neuholf e Auterhoff (16) del 7,5 % di raponticina.
Nei rizomi del Rh. Rhaponticum L. sono stati inoltre identificati glucogallina, acido gallico (4), tannino, olio etereo 0,041 % ( 2) e acido ossalico (17).
Proprietà farmacologiche ed impiego terapeutico
L'azione del Rabarbaro rapontico è qualitativamente la stessa di quella del Rabarbaro cinese. Quantitativamente il rapontico è invece meno attivo per il minor contenuto di composti antracenici, specialmente in forma ridotta. Strom e Kilstrom (10) infatti, trovarono una notevole differenza fra il risultato della titolazione chimica e quello ottenuto dalla titolazione biologica (ved. parte chimica), secondo la quale l'attività del Rabarbaro cinese si sarebbe dimostrata molto più elevata (100 %) di quanto avrebbe potuto apparire dalla differenza esistente fra il titolo chimico dei composti antracenici totali nelle due droghe (30-40 %). E' quindi logico presumere che la maggior attività del Rabarbaro cinese sia dovuta, più che alla differenza del contenuto dei composti antracenici totali, al diverso rapporto esistente fra i composti antracenici ridotti più attivi e composti antracenici ossidati meno attivi (ved. Rabarbaro cinese).
Siegfried (18), con lo scopo di sostituire con il rapontico il Rabarbaro cinese (Rheum palmatum), la cui reperibilità in commercio era resa particolarmente difficile dalle condizioni di mercato che si erano venute determinando durante l’ultimo conflitto mondiale, eseguirono ricerche comparative sull’attività lassativa di estratti secchi ottenuti da campioni di Rabarbaro cinese, di Rabarbaro rapontico di provenienza francese e di Rumex alpinus. Gli estratti furono preparati secondo la Ph. Helv. V e saggiati su topi bianchi. I risultati dimostrarono che l’estratto di Rabarbaro rapontico è meno attivo del Rabarbaro cinese di circa 3-4 volte e il Rumex alpinus di 4 volte.
Secondo l’A. l’attività lassativa del R. rapontico è dovuta all'acido crisofanico e alla eventuale presenza di resine, ma non alla raponticina la quale sperimentata sui topi bianchi, alla dose di 0,5 g/kg, si è dimostrata del tutto inattiva o quasi.
Fairbairn e Lou (8) inoltre, trovarono che un Rabarbaro rapontico inglese da essi esaminato, conteneva meno composti reinosimili attivi del Rabarbaro cinese e che campioni di Rabarbaro rapontico austriaco e francese, ne contenevano soltanto in tracce.
Lo stesso Siegfried (18) in considerazione del fatto che la raponticina appartiene chimicamente alle sostanze del gruppo degli ossistilbeni (ved. parte chimica), ha voluto indagare se anch’essa fosse dotata di un’azione follicolinosimile. Egli infatti potè dimostrare che la raponticina dimostra un’azione estrogena la cui intensità è però soltanto debolmente paragonabile a quella dell’estrone. L’A. ritiene che la possibilità di un impiego terapeutico della raponticina, tenuto conto dell’elevata attività degli stilbeni sintetici, potrebbe essere appena considerato.
Knorr e coll. (19) invece, in base ai risultati di loro ricerche chimiche e terapeutiche, hanno dimostrato che la raponticina ottenuta dai rizomi di Rabarbaro rapontico è dotata di una buona attività estrogena e che pertanto potrebbe essere prescritta in tutti i casi in cui è indicata una terapia follicolinica orale.
Per quanto riguarda la tossicità, Siegfried (18) trovò che essa è molto bassa. La dose letale nel topo è pari a 15-20 g/kg per una sola somministrazione o alla dose di 5 g/kg ripetuta in due giorni successivi. Fu osservata una reazione infiammatoria a carico degli elementi secernenti renali, ma nessuna alterazione a carico dell’intestino. La raponticina e, eventualmente, la rapontigenina, può essere riscontrata nelle urine dei topi, dei ratti, dei conigli e anche dell’uomo, dopo 1-2 ore dalla somministrazione.
Estratti e preparati vari
a) Estratto fluido per tintura (g 1 = XLVIII gtt).
Dosi: g 0,15-2,0 pro dose.
b) Estratto fluido per sciroppo (g 1 = XLI gtt).
Dosi: g 0,15-2,0 pro dose.
c) Estratto molle acquoso (1 p. = 3 p. circa di droga).
Dosi: g 0,05-0,5 pro dose.
d) Estratto secco acquoso (1 p. = 4 p. circa di droga).
Dosi: g 0,05-0,5 pro dose.
Preparazioni usuali e formule galeniche
Tintura
Estratto fluido rabarbaro rapontico per tintura………………. g 20
Alcool di 60°………………………………………………………. g 80
(da 3 a 30 g pro die).
Sciroppo
Estratto fluido rabarbaro rapontico per sciroppo…………… g 5
Sciroppo semplice F.U. g 95
(a cucchiai).
BIBLIOGRAFIA
(1) TSCHIRCH c CRISTOFOLETTI, Arch. Pharrn.. 243. 443, 1905; TSCHIRCH c EDNER, ibid.. 245. 141, 1907 – (2) HAENSEL. Apoth. Z.. 17, 498, 1902 – (3) GSTIRNER F. e HOLTZEM H„ Chem. Abs., 43. 9383, 1949 – (4) MESSE O., 3- prakt. Chtm., 77. 321, 1908; Chsm. ZbL. I, 1713, 1908 – (5) KEIMATSU S. e MIRANO J., Chem. Zbi. I. 2533, 1929 – (6) KEIMATSU S„ MIRANO J. e TANABE T., ibidem., II, 995, 1929 – a) TSCMIRCM A.. Mandbuch der Pharmakognosie, 1917, p. 1393 – (8) FAIRBAIRN J. W. e LOU T. C.. 3. Pharrn. Pharmacoi. 3. 93. 1951 – (9) AUTERMOFF M„ ArZneinL-Forsch.. 3. 23. 1953; Piamo Med., J, 106, 1953 – (10) STRÓM H. e KILSTRÒM T., Meddtìetser Norsk Farmacfutisk Sehkap, 10, 67, 1948 – (11) RUSZKOWSKI M., Chtm. ZbL L 1339, 1930 – (12) MOHIUDDIN M. G. e KAITI M. C. T., ibid., II, 1059, 1933 – (13) KAWAMURA S„ ibid., I, 130, 1939 – (14) TAKAOKA M., ibid., I, 2117, 1941 . (15) SIEGFRIED B„ Chem. Abs., 3S, 1843, 1944 – (16) NEUHOFF E. W. e AUTERHOFF H„ Disch. Ap. Zig., 94, 541, 1954 – (17) WEHMER C„ Die Pflanzcnsioffe, li ed., p. 273 – (18) SIEGFRIED B., Pharrn. Aera Helv.. 18, 531, 1943 – (19) KNORR K„ LEHR H. e PROBST W„ Die Medizin., l, 195, 1956.

