Quebraco (blanco)
Tratto da “Piante Medicinali – Chimica, Farmacologia e Terapa” di R. Benigni, C. Capra e P.F.Cattorini
(Aspidosperma Quebracho Schlecht. (A. Quebracho-blanco) Fam. Apocinacee/Plumieree/Alstoniee)
Quebraco (blanco)- Ultimo aggiornamento pagina: 27/02/2018
Indice dei contenuti
- Generalità
- Componenti principali
- Proprietà farmacologiche
- Estratti e preparati vari
- Preparazioni usuali e Formule
- Bibliografia
Generalità

Etimologia – Aspidosperma, dal greco aspis -idos = scudo e sperma = seme, perchè i semi hanno forma sub-orbicolare, contornati da un'ampia ala denticolata crespa.
Quebracho (pronuncia Quebratcho): il nome deriva da quiebrahatcha = quebrar = rompere e hacha = accetta e designa, nell’America del sud, e specialmente in Argentina, parecchi alberi di famiglie ben diverse, aventi in comune l’estrema durezza del legno e una grande ricchezza di tannino.
Nomi volgari – Quebracho blanco o branco. White Quebracho (ingl.).
Habitat – Argentina (distr. Catamarca, prov. Santiago de l'Estero, Sierra d’Ancasta, Corrientes, Missiones, Tucuman, S. Jouan, Salto). Chacos, S. Luis, nord della Patagonia, Cile, Brasile, Paraguay, Uruguay, Bolivia.
Albero sempre verde, di grandi dimensioni (15 m. x 1,26 m. diam.).
Parti usate – La corteccia del tronco e dei rami.
Componenti principali
I seguenti alcaloidi:
Aspidospermina, C22H30O2N2, è stata isolata da Fraude (1) (2) e poi da Hesse (3) dalla corteccia dell’Aspidosperma Quebracho-blanco. Lo studio della composizione chimica dell’aspidospermina, specialmente per opera delle più recenti ricerche di Conroy, Brook e Amiel (4), di Mills e Nyburg (5) e di Smith e Wrobel (6), ha condotto alla formulazione della struttura I:
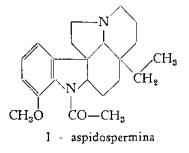
Yoimbina, C21H26O3N2, è stata estratta dalla corteccia dell'A. Quebracho-blanco da Hesse (3), che l’ha denominata quebrachina. L’identità della quebrachina e della yoimbina è stata a lungo discussa (7) (8) ed infine stabilita (9) (10) (ved. Yohimbe).
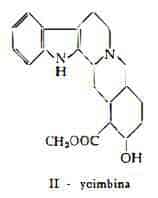
(—)-Quebracamina, C19H26N2, è stata ottenuta da Hesse (3) dall'A. Quebracho-blanco e più recentemente da Orazi, Corral, Holker e Djerassi (11) dalla corteccia dell'A. chakensis Speg. Per essa è stata proposta la formula di struttura III (6) (12) (12a), che è stata successivamente confermata (12b).
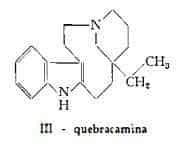
Quebracacidina, C26H28O11N2, è un glucoalcaloide, separato da Tunmann e Rachor (13) mediante cromatografia su carta, dalla corteccia dell'A. Quebracho-blanco. Mediante scissione idrolitica con acido esso produce glucosio e un aglucone contenente un carbossile, ma privo di ossidrili fenolici. La quebracacidina e l’aglucone da essa derivante presentano caratteristiche avvicinabili a quelle dell’indol-N-metilarmano e dell’alstonidina.
Altri alcaloidi sono stati segnalati e cioè: aspidospermatina, C22H28O2N2 (3), aspidospermicina, C17H21ON (14), una base con p.f. 176°-177° non denominata (10), aspidosamina e ipoquebrachina (3). E' stata avanzata l'ipotesi che l'aspidosamina e la ipoquebrachina siano miscele di prodotti di decomposizione, derivanti dall'idrolisi dell'aspidospermina (10).
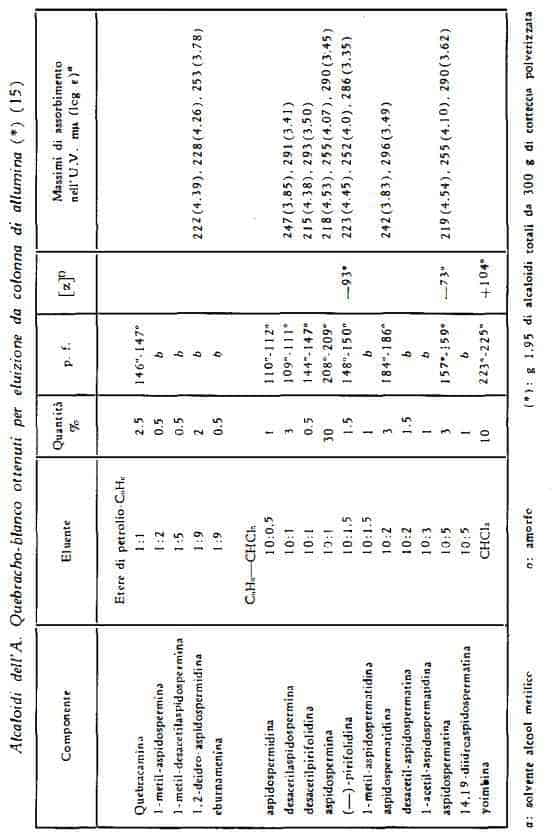
Recentemente, per mezzo di tecniche basate sulla cromatografia in fase gassosa e sulla spettrometria di massa, Biemann e coll. (14a) (15) hanno riconosciuto nella corteccia dell’Aspidosperma Quebracho-blanco la presenza di oltre venti alcaloidi, diciassette dei quali sono stati identificati. Tre sono stati riconosciuti identici agli alcaloidi già noti aspidospermina (I), yoimbina (II) e quebracamina (III), mentre degli altri alcuni sono risultati raggruppabili con l’aspidospermina, altri riunibili in un nuovo gruppo, di cui l’aspidospermatina (XV) è il più abbondante. Si tratta dei seguenti alcaloidi:
I) Gruppo dell'aspidospermina – aspidospermidina (IV), l-metilaspidospermidina (V), desacetilaspidospermina (VI), l-metildesacetil-aspidospermina (VII), desacetilpirifolidina (VIIl), (—)-pirifolidina (IX), 1,2-deidroaspidospermidina (X):
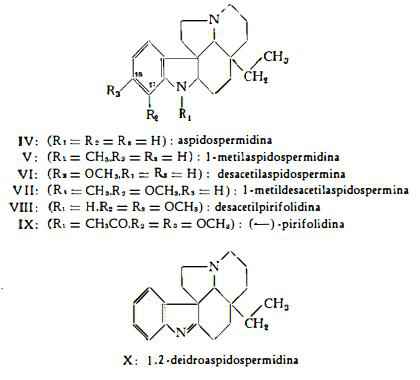
II) Gruppo dell’aspidospermatina – aspidospermatidina (XI), I-metilaspidospermatidina (Xll), desacetilaspidospermatina (XIII), I-acetilaspidospermatidina (XIV), aspidospermatina (XV), 14,19-diidroaspidospermatina (XVI):
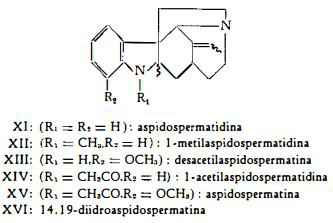
L’alcaloide con formula XV è stato identificato con l'aspidospermatina di Hesse (3) sopracitata ed è stato perciò designato con questo nome (15). Un altro degli alcaloidi isolati da Biemann e coll. (15), la (—)-pirifolidina (IX), era già stato estratto dall’Aspidosperma pyrifolium da Djerassi e coll. (16) nella forma destrogira.
Eburnamenina, C10H22N2, isolata precedentemente da Bartlett, Taylor e Raymond-Hamet (14b) dall’apocinacea Hunteria eburnea e trovata poi anche nell’Aspidosperma Quebracho-blanco da Biemann e coll. (14a), è rappresentata dalla formula XVII (14b) .
Il Quebraco blanco del Paraguay sembra essere il più ricco di alcaloidi (17). La base principale è la yombina, che è stata trovata nella corteccia in quantità pari a 0,3-1,4% (18). Biemann e coll. (15) hanno separato per cromatografia su colonna g 1,95 di alcaloidi da g 300 di corteccia, pari ad una resa di g 0,65%.
Oltre agli alcaloidi, nella corteccia del Quebraco sono stati identificati tannino 2-4% (18) e quebrachitolo (19),
Il quebrachitolo, C7H14O6, (etere metilico dell'inositolo) è stato isolato per la prima volta dalla corteccia dell’A. Quebracho-blanco da Tanret (19) ed è stato in seguito identificato in numerose altre droghe (19a). Posternak (19b) ne ha determinata la formula di configurazione XVIII.
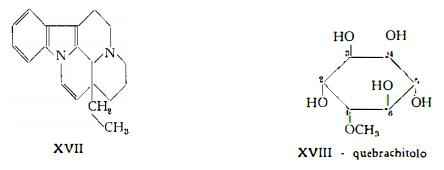
Proprietà farmacologiche ed impiego terapeutico
Diverse piante del genere Aspidosperma erano usate nella medicina tradizionale dei paesi di origine fin dall’epoca precolombiana.
Dopo la conquista spagnola queste droghe destarono l’interesse di alcuni dotti gesuiti i quali, avendo notato come esse venissero usate dagli indigeni per curare le febbri intermittenti, impiegarono una di esse e precisamente l’Aspidosperma Quebracho-blanco, per combattere le febbri periodiche endemiche nelle provincie andine dell’Argentina settentrionale.
Lo studio chimico di questa droga venne iniziato nel 1873 dall'argentino Peron il quale estrasse dalla corteccia un alcaloide cristallizzato che chiamò quebrachina, una sostanza colorante simile al rosso-china e un corpo dall’aspetto resinoso.
I risultati di queste ricerche furono pubblicati nel 1878 (20), anno in cui alcuni campioni di corteccia di Quebracho giunsero per la prima volta in Europa, per merito dello Schickentanz, residente tedesco in Argentina, il quale li inviò al Baeyer, con l’informazione che la droga era usata dagli indigeni come febbrifugo.
Sempre nello stesso anno e quasi contemporaneamente alla nota del Peron, comparve in Germania uno studio di Fraude di Monaco (1) (2) con il quale egli comunicava di aver isolato un altro alcaloide dalla corteccia di Quebracho, l’aspidospermina, esprimendo l’opinione che in questa droga dovevano essere contenute anche altre basi alcaloidee.
L’anno seguente (1879), l’argentino Burgos in una «Tesi inaugurale» rimasta inedita, trattò del Quebracho-blanco considerandolo come un vero succedaneo della China alla quale, secondo l’A., potrebbe essere sostituito in tutti i suoi preparati officinali e magistrali, avendo sulla corteccia peruviana il vantaggio di poterla ottenere più facilmente e a prezzi molto inferiori.
L’alcaloide contenuto nella corteccia di Quebracho-blanco è considerato dall’A. un antipiretico e un antimalarico dell'importanza della chinina, capace di produrre gli stessi effetti alla stessa dose e, come la chinina, dotato di proprietà antitermiche e antisettiche (21).
Lo studio clinico fu iniziato nel 1880 da Penzoldt di Erlangen (22) il quale proconizzò l'impiego di questa droga nella terapia dell’asma nervosa, della dispnea, dell'enfisema e anche come antimalarico, pur notando una notevole incostanza d’azione dovuta, verosimilmente, oltre alla variabilità del contenuto aicaloideo, anche alle frequenti sostituzioni di essa con altre meno attive o del tutto inattive.
Fin dall’anno prima infatti, la corteccia di Quebracho-blanco fu oggetto di una grande richiesta sui mercati europei e la sua scarsezza non mancò di incoraggiare le adulterazioni e la sostituzione della droga vera coi materiali più diversi, i quali peraltro, venivano venduti a prezzi assai elevati.
Si aggiunga poi che in Argentina il nome volgare di Quebracho veniva attribuito a vegetali appartenenti a famiglie diverse e dotati di differenti proprietà terapeutiche, cosicché era molto frequente il caso che corteccie di vegetali diversi, venissero vendute e usate come corteccie di Quebracho-blanco.
Tutto ciò fu causa di non poca confusione in campo medico e, inevitabilmente, condusse a risultati clinici contraddittori e ad opinioni molto discordi sul valore terapeutico della droga.
L’importazione in Europa del Quebracho-blanco in migliori condizioni ebbe inizio dopo il 1880 e in questo periodo ebbero inizio anche le ricerche chimiche da parte di Hesse (3) e quelle farmacologiche di molti autori fra i quali Gutmann (23), Harnach e Hoffman (24), Huchard (25), Eloy e Huchard (26), Canali (27), Bordeaux (28), Hale (29) ecc.
L’attività farmacologica del Quebracho è dovuta al suo contenuto alcaloideo (ved. parte chimica) e in particolare alla quebrachina e alla quebracamina.
Secondo il Coronedi (30) il Quebracho e la quebracamina esercitano inizialmente un’azione eccitante sul centro respiratorio che verrebbe invece paralizzato dalle dosi più elevate. La morte degli animali a sangue caldo avviene sempre per paralisi del centro respiratorio mentre negli animali a sangue freddo la morte è dovuta ad arresto cardiaco ed è per questo che, secondo Luzzatto (31), la quebrachina riesce più tossica nei primi che nei secondi.
Wood (32) dimostrò che tutti gli alcaloidi contenuti nel Quebracho-blanco possiedono proprietà farmacologiche simili e che la quebrachina è, fra essi, la più attiva.
Dosi moderate di questo alcaloide, in animali anestetizzati, determinano una leggera caduta della pressione, accompagnata da una marcata stimolazione dell’attività respiratoria.
Successivamente da Fourneau e da Page (9) la quebrachina venne identificata con la yoimbina ciò che però non venne ammesso da Filippi (33), il quale pur avendo trovato che la quebrachina determina sui vasi isolati, contrariamente a quanto aveva affermato il Cow (34), un effetto vasodilatatore simile a quello prodotto dalla yoimbina, ritenne che questa non poteva essere identificata con la quebrachina, distinguendosi essa per la sua più forte azione inibitrice dell’ipertensione adrenalinica, per l’azione paralizzante che essa possiede sul simpatico cervicale, azione di cui non sarebbe dotata invece la quebrachina, per la sua più debole tossicità cardiaca, per una soglia di eccitazione dei vasodilatatori periferici differente da quella della quebrachina, per l’aumento dell’energia muscolare che essa sola provoca, per la sua più forte azione anestetica locale e iperemizzante, per la più lunga durata del tetano che si manifesta nella rana nel corso dell’intossicazione yoimbinica e, infine, per la sua più elevata tossicità generale.
L’argomento dell’identità della quebrachina e della yoimbina venne ripreso alcuni anni più tardi da Raymond-Hamet (35) il quale stabilì che, per quanto riguarda la tossicità, essa è molto diversa da quella trovata da Filippi essendo quella relativa alla quebrachina assolutamente analoga a quella trovata dall’A. per la yoimbina.
Anche per ciò che concerne l’azione sul simpatico, Raymond-Hamet (36) trovò che essa è identica per i due alcaloidi. L'azione dell’adrenalina sulla pressione carotidea è completamente invertita sia dalla quebrachina che dalla yoimbina e la quebrachina inoltre, aumenta nettamente la frequenza degli atti respiratori. L’A. conclude quindi che i due alcaloidi, la cui identità chimica era già stata stabilita da Fourneau e Page e confermata da Spiegel (7-8), hanno anche la stessa azione farmacologica, ciò che confermerebbe ulteriormente l’assoluta identità delle due sostanze.
L’effetto della quebrachina sull’attività respiratoria negli animali normali e anestetizzati sarebbe secondo Weinberg (37), notevolmente diverso, ma la causa di ciò non è stata dall’A. ben chiarita.
Questo A. avrebbe trovato che dosi moderate di quebrachina deprimono l’attività respiratoria e innalzano la pressione sanguigna negli animali normali, mentre per ottenere gli stessi effetti negli animali anestetizzati occorrerebbero dosi molto più elevate.
Più recentemente Raymond-Hamet (38) notò l'azione anestetica locale della quebrachina, trovandola circa due volte più attiva di quella dovuta alla cocaina.
Per quanto riguarda l’azione degli altri alcaloidi contenuti nella corteccia di Quebcacho-blanco, Raymond-Hamet (39-40), trovò che la quebracamina possiede alcune delle proprietà farmacologiche della sparteina e, in particolare, quella di aumentare l'azione ipertensiva e vasocostrittrice renale di dosi medie di adrenalina e di invertire l'ipotensione prodotta da dosi minimali di adrenalina e dei suo omologhi superiori N-alchili (41-42).
Si potrebbe tuttavia pensare che l’azione della quebracamina differisca da quella della sparteina poiché, mentre questa è vasocostrittrice a concentrazioni deboli, è vasodilatatrice a concentrazioni più elevate (43), la quebracamina, secondo l’opinione di alcuni AA., fra i quali Toshiki Choda (44), determinerebbe soltanto un'azione vasocostrittrice. I risultati delle più recenti ricerche di Raymond-Hamet (45) avrebbero invece dimostrato che la quebracamina si comporterebbe, in questo caso, esattamente come la sparteina, agendo essa sui vasi con un’azione vasocostrittrice o vasodilatatrice, a seconda che la si faccia agire a deboli o a forti dosi.
L'aspidospermina è stata studiata da Benerjee e Lewis (46) secondo i quali essa sarebbe dotata di alcune delle proprietà comuni agli altri alcaloidi contenuti nella corteccia del Quebraco.
L’aspidospermina non antagonizza specificamente l’azione dell’acetilcolina, dell’istamina e del bario sull’ileo isolato di cavia e manifesta una azione tossica sul miocardio. Analogamente ad altri derivati indolici, l’aspidospermina influisce sulla risposta dei vasi sanguigni all’adrenalina, essa inverte l’azione vasocostrittrice di questa sui vasi perfusi dell'orecchio di coniglio e degli arti posteriori di ratto e ne antagonizza inoltre, l’azione spasmolitica sull’utero di coniglia.
Come la quebrachina, l’aspidospermina è dotata di un’azione stimolante dell’attività respiratoria.
Il Quebracho-blanco viene usato, isolatamente o in associazione con altre droghe ad azione simile, nella terapia dell’asma, dell'enfisema, in varie forme di dispnea e come analettico respiratorio.
Estratti e preparati vari
Estratto fluido (g 1 = XXXV gtt).
Dosi: g 1 pro dose due-tre volte pro die.
Preparazioni usuali e formule galeniche
Tintura
Estratto fluido quebraco……………………………………………….. g 20
Alcool di 30°…………………………………………………………………. g 80
(g 5 pro dose).
Sciroppo
Estratto fluido quebraco………………………………………………. g 5
Sciroppo semplice F.U…………………………………………………. g 95
(a cucchiai).
Elisir
Estratto fluido quebraco………………………………………………. g 6
Sciroppo china……………………………………………………………… g 30
Elisir Garus q. b. per…………………………………………………….. g 500
(a cucchiai).
Pozione
Estratto fluido quebraco g 2
Estratto fluido lobelia g 1
Estratto fluido menta alcool-idrosolubile ……………………….. g 3
Glicerina e alcool di 95° ….. ana g 5
Sciroppo semplice F.U………………………………………………. g. 40
Acqua q. b. a……………………………….. …………………………… g 100
(a cucchiaini).
BIBLIOGRAFIA
(1) FRAUDE G., Ber,, 11, 2189, 1878 – (2) FRAUDE G., Ibid , 12, 1560, 1879 • (3) MESSE O., Lieb Ann., 211, 249, 1882 – (4) CONROY H., BROOK P. R. e AMIEL Y„ Tetrahedron Letters, n. 11, 4, 1959 – (5) MILLS J. F. D. e NYBURG S, C., ibid„ n. 11. 1, 1959; J, Chem. Soc., 1458, 1960 – (6) SMITH G. F. e WROBEL J. T., J. Chem Soc., 1463, 1960 – (7) SPIEGEL L., Ber., 48, 2077, 1915 – (8) SPIEGEL L., ibid., 48, 2084, 1915 – (9) FOURNEAU E. e PAGE H. J., Bull. sci. pharm., 21, 7, 1914 – (10) EWINS A. J., J. Chem. Soc., 105, 2739, 1914 – (11) GRAZI O. O., CORRAL R. A., HOLKER J. S. E. e DJERASSI C., J. Ory. Chem., 21, 979, 1956; An, Soc. Quim. armeni., 44, 177, 1956; Chem Abs., 51, 13313, 1957- (Ila) DJERASSI C., BREWER H, W., BUDZIKIEWICZ H., GRAZI G. G. e CGRRAL R. A., J. Am. Chem. Soc., 84, 3480, 1962; Experientia, 18, 113, 1962 – (12) KNY H. e WITKGP B., J. Ory. Chem., 25, 635, 1960 – (12a) CGHEN L. A., DALY J. W., KNY H. e WITKGP B., J. Am. Chem Soc., 82. 2184, 1960 – (12 b) BIEMANN K. e SPITELLER G., ibid., 84, 4578, 1962 – (13) TUNMANN P. e RACHGR J., Naturwiss., 47. 471, 1960 – (14) DGMINGUEZ J. A., Rev. farm. (Buenos Aires). 73, 82, 1932; Chem. Abs., 26, 4102, 1932 – (14 a) SCHNGSS H, K., BURLINGAME A. L, e BIEMANN K., Tetrahedron Letters. 993, 1962; Chem. Abs., 58, 9155, 1963 • (14b) BARTLE7T, TAYLGR e RAYMGND- HAMET, C. R. Acad. Sci., 249. 1259, 1959; Chem. Abs., 54, 16473. 1960 – (15) BIEMANN K.. SPITEL- LER-FRIEDMANN M c SPITELLER G., J. Am. Chem Soc., 85, 631, 1963 – (16) DJERASSI C„ ARCHER A. A. P. G„ GEGRGE T., GILBERT B. e ANTGNACCIG L, D., Tetrahedron, 16. 212, 1960; DJERASSI C, GILBERT B., SHGGLERY J. N., JGHNSGN L. F. e BIEMANN K., Experientia, 17, 162, 1961 – (17) RGSSI G. A., Monit. jarm. )â– terap., 52. 157. 175. 1946; Chem. Abs., 40, 5530. 1946 – (18) WEHMER C., Die Pflanzenstoffe, II cd„ p. 982 – (19) TANRET C., Compì. rend„ 109, 908, 1889 – (19 a) KARRER W,, Konstilulion und Vorlcommen der organischen Pflanzensloffe, ed, 1958, p. 118-119 – (19 b) PGSTERNAK T„ Helv. Chim. Acta, 35, 50, 1952 – (20) PERGN T„ Soc. Scient. Argentina. 6, 234, 1878 • (21) BURGGS F„ cit. da RGTHLIN in Trabajos del Instituto de Botanica y Farmacologia, Facultad de Ciencias Médicas de Buenos Aires, n. 38: Contribucion al estudio de los Aspidosperma, J. Peuser Ed., Buenos Aires 1918, p. 22 – (22) PENZGLDT F., Berliner Klin. Woch., n. 10, 1880 e Die Wirkung der Quebracho droguen, Erlangen 1881 – (23) GUTMANN, Arch. exp. Path. u. PharmakoU, 17, 451, 1881 – (24) HARNACH e HGFFMAN, Zéitschr. KUn. Med., 8, 471, 1884 – (25) HUCHARD, Bull, et Mem. Soc, de Thér., 8, 135, 1886 – (26) ELGY e HUCHARD, Arch. Physioi Norm. Path,, 7. 236,
1886 – (27) CANALI, Gali, degli Osped., 7, 76. 83, 1886 – (28) BGRDEAUX, Arch. Méd. belges, 3. 213,
1887 – (29) MALE, Hahneman Month., 34, 81, 1889 – (30) CGRGNEDI G., Saggio di uno studio critico sperimentale intorno all’azione biologica del Quebracho bianco e dei suoi alcaloidi, Sassari 1899 * (31) LUZZATrG R., Lo Sperimentale, 57, 310, 1903 – (32) WGGD H. C. Jun., Vniv. Pensyl. Med. Bull., 23. 1, 1910 – (33) FILIPPI E., Arch. Hai, farmacol. sper . 23. 107, 1917 – (34) CGW D„ J. Pharmacoi exp. Ther., 5. 341, 1913-1914 – (35) RAYMGND-HAMET, Bull. Acad. Méd., 91. 145, 1924 – (36) RAYMGND-HAMET, Comp, rend. soc. bÌoÌ.. 96, 2, 1927 – (37) WEINBERG, J. Pharmacoi. exp. Ther., 47 , 79. 1933 – (38) RAYMGND-HAMET, Comunicar, alla Soc. de Biol., 19. XH, 1953, in Presse Méd., 62. 33, 1954 – (39) RAYMGND-HAMET, C.R. Acad. Sci., 187. 142, 1928 – (40) RAYMGND-HAMET, Comp, rend. soc. bici., 149, 940, 1955 – (41) MERCIER F., C. R. Acad. Sci., 185, 1162, 1927 – (42) RAYMGND-HAMET, ibid., 150, 967. 1956 – (43) MERCIER F. e RAYMGND-HAMET. Bull Acad. Méd., 107, 430, 1932 – (44) TGSHIKI CHGDA, Okayama Igakkal ZasslU, 50, 1062, 1938 – (45) RAYMGND- HAMET, Comp. rend soc. bioL, 151, 74. 1957 – (46) BENERJEE J. N. e LEWIS J. J.. /. Pharm. Phar- macol., 7, 46. 1955.

