Se hai un abbonamento attivo ACCEDI QUI
Salici
Tratto da “Piante Medicinali – Chimica, Farmacologia e Terapa” di R. Benigni, C. Capra e P.F.Cattorini
1) Salix alba L. – Fam. Salicacee
2)Salix nigra(Willd.) Marsch.[Sin. –Salix carolinianaMich. –Salix pentandraWalt. (non L.)]
Salici- Ultimo aggiornamento pagina: 27/02/2018
Indice dei contenuti
- Generalità
- Componenti principali
- Proprietà farmacologiche
- Estratti e preparati vari
- Preparazioni usuali e Formule
- Bibliografia
Generalità

Salix alba
Etimologia – Salix, nome usato da Virgilio (Egl. IlI, 82). Secondo M. Servio dal latino salio, salire = saltare, balzare, perchè il salice cresce tanto in fretta che sembra salti fuori dal terreno. Secondo Theis, dal celtico sul = vicino e lis = acqua, cioè presso all'acqua, allusione al suo frequente habitat.
alba, per le foglie bianco/setose sulle due pagine, specialmente sull'inferiore. Anche per la corteccia biancastra dei rami ed i germogli biancastri.
Nomi volgari – Salcio, salicene, salicastro, ecc. (tosc.), saxu giancu, sarxu domestegu (lig.), sales de pertich, sales bropé, gura (piem.), sàres bianch. gaba (lomb.), salgher da latole, venco (ven.), sales da broch, sales da cavagnen (emil.), salici jancu, gurra (sic.), salixi biancu (sard.).
Osier blanc, saule blanc (fr.), Weide o Weisse (ted.), white willow (ingl.), sauce (spagn.), salqueiro bianco (port.), fuzfa (ungh.), Wierzba (pol.).
Habitat – Diffusa in tutto l'emisfero boreale, lungo le strade, presso gli abitati (borghi e villaggi), nei boschi. In Italia comune lungo i corsi di acqua (fossi, torrenti, fiumi), nei terreni acquitrinosi, sabbiosi, pingui e freschi dal piano ai monti. Qua e là anche nei boschi umidi. Estesamente coltivato (assieme alla varietà vitellina Lightfoot) nelle bassure umide, lungo i fontanili, al limite delle marcite.
Albero, generalmente tenuto a capitozza, può arrivare a 10 m.
Parti usate – La corteccia dei rami di 2-3 anni.
Salix nigra
Etimologia – Salix – c. s.
caroliniana – della Carolina (U.S.A.).
pentandra – i fiori hanno 5 stami.
Nota – Non va confusa con Salix nigricans Sm. (Alpi, Appennini) nè col Salix pentandra L., il nostrale Salcio odoroso (Alpi, Appennini).
Nome volgare – Black Willow.
Habitat – America del nord.
Albero.
Parti usate – La corteccia dei rami.
Componenti principali
Nella corteccia del Salix purpurea L.: i glucosidi salicina 3,83 % (1) anche 7,4 % (2), populina (3), salipurposide 1,4 % nella corteccia fresca (4), isosalipurposide sino al 3 % nella corteccia dei tronchi vecchi (5), salireposide nella corteccia del S. purpurea L. var. angustifolia Koidz. (6). Inoltre tannino 1,7% (3), anche 8 % (7).
Nella corteccia del Salix alba: salicina 0,3 tannino 3-4% (3) anche 9,4% (7).
Nella corteccia del Salix nigra Marsh. è stata trovata salicina (8), secondo altri AA., non vi è salicina, ma salinigrina (9). Nella corteccia del Salice nero americano sono stati trovati zuccheri riduttori, quali prodotti di idrolisi dell'estratto della corteccia, di cui glucosio 69 %, xilosio 18%, arabinosio 6 %, galattosio 3 %, mannosio 1 % (10). Inoltre ceneri 6 % e acqua 6,7 % (10).
Salicina (salicoside), C13H18O7, è stata isolata per la prima volta dalla corteccia del Salix helix L. da Leroux (11) e poi dalla corteccia di numerose specie di Populus, oltre che da altre specie di Salici, S. alba L., S. nigra Marsh, S. purpurea L., S. fragilis L., S. vitellina L., S. pentandra L., S. Humboldtiana Willd., S. lucida Mhlb., S. fissa Ehrh., S. retusa L., S. mollissima Ehrh., S. reticulata L., S. conifera Muhlb., S. rubra Huds., S. polyandra Gl., S. hastata L. (12-15).
Dalla scissione idrolitica della salicina (II) si formano glucosio (1 mol.) e la genina saligenina (saligenolo, alcool-salicilico) (Il), C7H8O2 (16)(17).
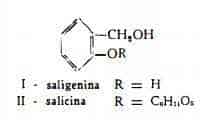
Populina (populoside), C20H22O8, identificata nella corteccia, nelIe foglie e nei germogli di numerose specie di Populus (14), è stata segnalata anche come componente del Salix purpurea L. (3), ciò che non è stato però confermato da studi più recenti.
E' la monobenzoilsalicina (lII) che per idrolisi produce glucosio (1 mol.), acido benzoico e saligenina (18-20).
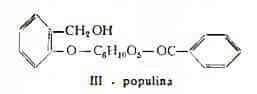
Salireposide, C20H22O9, è stato trovato nella corteccia di diverse specie di Salici, Salix repens (21), S. repens var. dunensis (22), S. purpurea L. var. angustifolia Koidz. (6), S. koriyanagi (23). Sottoposto a scissione idrolitica, produce glucosio (1 mol.), acido benzoico ed alcool gentisico (salirepolo), C7H8O3 (22) (24).
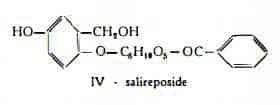
Salinigrina (piceina, piceoside, salicinereina, ameliaroside) è il nome dato da Jowett (9) al glucoside estratto dallo stesso A. da una droga, indicata quale corteccia di Salice nero e derivante verisimilmente dal Salix discolor Muhlb. e dal S. nigra Marsh. La presenza della salinigrina nel S. nigra non è stata successivamente confermata da altri AA.
La salinigrina è stata identificata da Bridel e Rabaté (25) al piceoside, C14H18O7, che è stato estratto dalle foglie del Pinus picea da Tanret (26) e che per scissione idrolitica dà glucosio e p-ossiacetofenone (piceolo, ameliarolo), C8H8O2 (V).
Rabaté (22) ha isolato il piceoside da nove specie di Salice, Salix nigricans, S. cinerea, S. serpyllifolia, S. grandifolia, S. reticulata, S. glauca, S. retusa, S. phylicifolia e S. discolor.
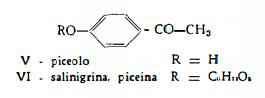
Salipurposide (fioribundoside), C21H22O10, è stato estratto da Charaux e Rabaté (4) dalla corteccia del Salix purpurea L. ed è stato identificato con il glucoside flavanonico (VIII), che per idrolisi produce glucosio (1 mol.) e naringenina (4',5,7-triossi-flavanone), C15H12O5 (4) (5). Questa composizione è stata più tardi confermata attraverso sintesi, da Zemplén, Bagnar e Székely (27). Più recentemente Hansel, Heise e Pinkewitz (28) hanno constatato che il salipurposide del S. purpurea è una miscela di due stereoisomeri del 5-b-D-glucoside della naringenina e che il glucoside avente aglucone levogiro, (—)-naringenina, costituisce la maggior parte (ca. 80%) della frazione glucosidica totale. Il salipurposide è stato pure riconosciuto quale componente dell'Acacia floribunda e denominato perciò anche floribundoside (29).
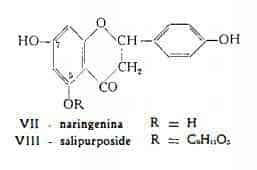
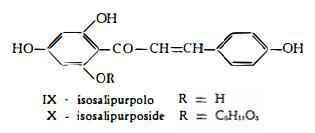
Isosalipurposide, C21H22O10, trovato da Charaux e Rabaté (5) nella corteccia degli alberi vecchi del Salix purpurea L. è la forma calconica del salipurposide. E' costituito da isosalipurpolo (calcone della naringenina), C15H12O5, legato ad una molecola di glucosio.
Proprietà farmacologiche ed impiego terapeutico
Il Salice bianco possiede l'azione antipiretica ed antireumatica caratteristica dell'acido salicilico e dei suoi derivati, azione dovuta alla presenza della salicina, glucoside dalla cui scissione si formano glucosio e saligenolo (ved. parte chimica).
Secondo Leclerc però, l'azione più importante del Salice bianco sarebbe quella che svolge sull’eccitabilità nervosa, come deprimente e come anafrodisiaco.
Queste azioni che furono note a Dioscoride, sono state confermate, se non dai risultati di indagini farmacologiche, che non ci risulta siano state eseguite, dalla sperimentazione clinica eseguita da alcuni autori francesi durante i primi due decenni dello scorso secolo.
Leclerc (30) riferì sui buoni risultati da lui ottenuti impiegando preparati di corteccia e specialmente di amenti di Salice bianco, nell'insonnia nervosa, nell’eretismo sessuale come anafrodisiaco, come sedativo e analgesico nei disturbi da dismenorrea, casi nei quali ottenne l'attenuazione dei sintomi dolorosi e la scomparsa delle turbe nervose che ne conseguono.
Renon (31) riferì di aver ottenuto buoni risultati impiegando questa droga come sedativo, in numerosi casi di ipereccitabilità nervosa dovuta alla cosiddetta «angoscia di guerra» e il Liegeois (32) riferì sulla sua favorevole influenza nelle dispepsie cloridriche e lienteriche.
Leclerc consiglia l'estratto fluido alla dose di 5-10 g come tonico e come antitermico; come antispasmodico e come sedativo, l'A. consiglia l’estratto fluido di infiorescenze, alla dose di 1-2 cucchiai prima di coricarsi e un terzo dopo mezz’ora, se necessario, per combattere i dolori pelvici, l’eretismo genitale, l'insonnia, l’angoscia.
Il Salice nero ha le stesse azioni e le stesse indicazioni del Salice bianco.
Estratti e preparati vari
a) Estratto fluido salice bianco (g 1 = XXXIII gtt).
Dosi: g 5-20 pro die.
b) Estratto molle acquoso salice bianco (1 p. = 10 p. circa di droga).
Dosi: g 0,5-2.
c) Estratto fluido salice nero (g 1 = XLVII gtt).
Dosi: g 2-5 pro die.
d) Estratto secco idroalcoolico salice nero (1 p. = 5 p. circa di droga).
Dosi: g 0,40-1 pro die.
Preparazioni usuali e formule galeniche
Tintura salice bianco
Estratto fluido salice bianco…………………………………………. g 20
Alcool di 20°………………………………………………………………. g 80
(a cucchiai).
Tintura salice nero
Estratto fluido salice nero ………………. g 20
Alcool di 60° g 80
(a cucchiaini).
Sciroppo
Estratto fluido salice bianco…………………………………………. g 10
Sciroppo semplice F.U. g 90
(1-2 cucchiai pro dose più volte pro die).
Pozione sedativa
Estratto fluido salice nero……………………………………….. g 30
Estratto fluido valeriana……………………………………………. g 5
Sciroppo semplice F. U. ……………………………………………. g 100
(1 cucchiaino 3-4 volte pro die).
BIBLIOGRAFIA
(1) CLARK e GILLIE, Amer. J. Pharm., 93, 618, 1921 – (2) BROWN, Pharm. J., Jb, 558, 1903 – (3) WEHMER C., Die Pflanzenstoffe, Il ed., p. 201 – (4) CHARAUX C. e RABATÉ 1., Compt. rend., 192, 1478, 1931 – (5) CHARAUX C. e RABATE J., ibidem, 196, 816, 1933 – (6) SAKAI S., TSURUMI M., ENO y, e INUKAI F., Chem. Abs., 43, 7924, 1949 – (7) DEKKE, Gerbstoffe, 1913, p. 124 –
(8) WEHMER C., Die Pflanzenstoffe, Il ed., p. 202 – (9) JOWETI, Proc. Chem. Soc., 16, 89, 1900; J. Chem. Soc., 78, 707, 1900 – (10) CHANG Y. e MITCHELL R. L., Tappi, 38, 315, 1955; Chem. Abs., 50, 2971 b, 1956 – (11) LEROUX, Ann. ch/m. et phys., 43, 440, 1830 – (12) WEHMER C., Die Pflanzenstoffe, II ed., pp. 200-204 – (13) VAN RIJN J. J. L., Die Glykoside, Berlin, 1931, pp, 66-67 – (14) RABATÉ J.. Bufl. soc. chim. biol., 17, 439, 1935; Chem. Zb/., lI, 3929, 1935 • (15) CANTORINI P. E., Fitoterapia, 19, n. 2, 5, 1948 – (16) PIRIA R., Lieb. Ann., 56, 35, 1845 – (17) REINECKE A. e BEILSTEIN F., ibidem, 128, 179, 1863 – (18) PIRIA R., ibidem, 81, 245, 1852; 96, 315, 1855 – (19) SCHIFF H., ibidem, 154, 1, 1870 – (20) RICHTMYER N. K. e YEAKEL E. H., 1. Am. Chem. Soc., 56, 2495, 1934 – (21) WATTIEZ M., fluii. Soc. chim. bioi., 13, 658, 1931 • (22) RABATÉ J., ibidem, 328, 439, 1935 – (23) FUJIKAWA F. e TOKUOKA A., Chem. Abs., 45, 9506, 1951 – (24) ZEMPLÉN G., BOGNAR R. e MORVAY S., Ber., 76, 1165, 1943 – (25) BRIDEL M. e RABATÉ J., Compt. rend., 189, 1304, 1929; Chem. Zbi., I, 2568, 1930 – (26) TANRET C., Compt. rend., 119, 80, 1894 – (27) ZEMPLÉN G., BOGNAR R. e SZÉKELY J., Ber., 76, 386, 1943 – (28) HANSEL R., HEISE D. e PINKEWITZ G., Pharm. Acta He/v., 35, 27, 1960 – (29) PARIS R. A., Compì. rend., 238, 2112, 1954 – (30) LECLERC H., J. des Praticiens 1913; Précis de Phytothérapie, Masson, Paris 1935, p. 80 – (31) RENON L., J. des Praticiens 1916, cit. da LECLERC I.e. – (32) LIEGEOIS M., Rev. Général de Clin. et de Thér., 1903, cit. da LECLERC ibid.

