Se hai un abbonamento attivo ACCEDI QUI
Saponaria (rossa)
Tratto da “Piante Medicinali – Chimica, Farmacologia e Terapa” di R. Benigni, C. Capra e P.F.Cattorini
(Saponaria officinalis L. – Fam. Cariophyllacee/Dianthee)
(Sin. – Saponaria vulgaris Park. – Lychnis officinalis Scop. Lychnis saponaria Ray.)
Saponaria (rossa)- Ultimo aggiornamento pagina: 27/02/2018
Indice dei contenuti
- Generalità
- Componenti principali
- Proprietà farmacologiche
- Estratti e preparati vari
- Preparazioni usuali e Formule
- Bibliografia
Generalità

Etimologia – Saponaria, dal greco sapon = sapone e dal latino sapo id., allusione alla radice che fa spumeggiare l'acqua come il sapone ed ha proprietà detersive. officinalis, delle officine farmaceutiche.
vulgaris – comune.
Lychnis, dal greco lucnon o lucnos = lume, lucerna, perchè le foglie di una specie di questo genere (Lychnis coronaria (L.) Desr.) erano utilizzate come lucignoli.
Nomi volgari – Centauria maggiore (antiq.), saponai, savonella, garofalo a mazzetti (tosc.), savonèa, sannaria, erva savonina (lig.), erba savana, savonin (piem.), savonaria, gelsomin selvadegh, giasmin matt (lomb.), reciarolina (ven.), mazzet de S. Juseff (emil.), saponara (nap.), sapuneddu, lignu sapuneci (sic.), sabonaria (sard.).
Seifenkraut, waschkraut (ted.), soapwort, sheep wood, fuller’s herb (ingl.), saponaire, herbe à foulon, savonnière (fr.), jabonera (spagn.), saboeira (port.), szappanfu (ungh.) .
Habitat – Diffusa in tutta Europa e in Asia. In Italia frequente nei luoghi freschi, lungo i corsi d'acqua, nel greto dei fiumi, nelle siepi, nei prati e boschi umidi, lungo le strade ferrate, sui muriccioli, dal mare alla zona subalpina. In tutta la penisola, Ischia, grandi isole.
Pianta erbacea perenne.
Parti usate – Rizomi e radici.
Componenti principali
Saponine, cui sono stati assegnati vari nomi, saporubina, saponaria-sapotossina, acido saporubico, lattossina (1). Nel 1940 Kon e Soper (2) hanno separato dalle radici della Saponaria officinalis L. circa 15 % di saponina grezza, dalla quale mediante idrolisi acida hanno ottenuto l’aglucone gipsogenina (gipsofilasapogenina, albasapogenina), sapogenina, C30H46O4, nota come componente di saponine di alcune specie di Gypsophila e di altre Cariofillacee.
In seguito alle ricerche di Karrer e coll. (3) e di Ruzicka e coll. (4-6) alla gipsogenina è stata assegnata la struttura I di derivato triterpenico del gruppo della b-amirina.
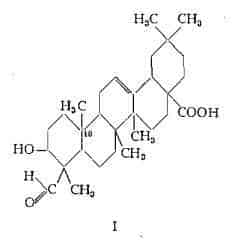
Il contenuto di saponine nelle radici è massimo durante aprile e maggio poco prima della fioritura ed è minimo durante la fioritura in luglio e agosto (7) (8). Nel periodo di aprile-maggio nelle radici è stato trovato un contenuto di saponine pari a 7,74-8,18% ed in agosto pari al 2,3 % (7). La diminuzione del titolo in agosto è probabilmente dovuta ai processi biologici cui partecipano le saponine negli organi vegetativi, durante lo sviluppo dei fiori e delle foglie (8).
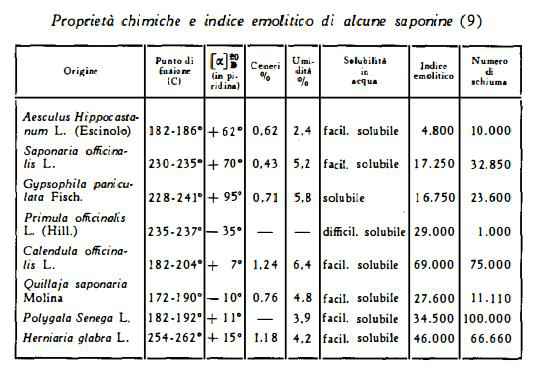
Altri componenti delle radici: gli acidi glicolico e glicerico (11), zuccheri riduttori 2,8%, galattano 10,7%, gomma 2,6%, grasso 0,125%, olio etereo 0,185%; ceneri 1,9% (1), acqua 67% (10).
Dalle foglie della Saponaria officinalis L., Barger (12) ha estratto un glucoside flavonoide, saponarina, da cui per idrolisi ha ottenuto glucosio (1 mol,), saponaretina e vitexina. Quest'ultima era già stata estratta da Perkin (13) dalla Vitex littoralis. Più recentemente Cambie (14) ha identificato la saponaretina alla isovitexina (omovitexina), C21H20O10, isomero destrogiro della vitexina, alla quale ultima Evans e coll. (15) hanno assegnato la struttura II, sostituendola alle formule precedentemente proposte da Barger (12) e da Nakaoki (16). La formula di Evans e coll. (15) è stata in seguito confermata da Briggs e Cambie (17).
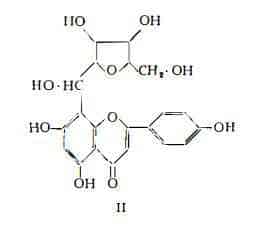
Seikel e Geissman (18) hanno dimostrato che esiste un equilibrio tra vitexina e saponaretina in soluzione con acido cloridrico diluito a caldo ed hanno proposto per la saponaretina la formula III a catena aperta, riferendo l’equilibrio alla formazione dell'anello per processo di deidratazione e, viceversa, all’apertura dell’anello per idratazione in presenza di acido.
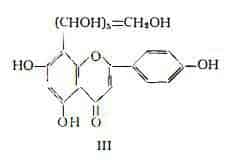
Proprietà farmacologiche ed impiego terapeutico
La Saponaria era nota a Ippocrate come droga ad azione emmenagoga ma una più vasta diffusione del suo impiego terapeutico si deve ai medici arabi i quali la usavano nella terapia della lebbra, di alcune dermatosi e delle ulcere maligne.
Ci sembra interessante notare che un'azione antileprosa venne da tempo notata e recentemente confermata in molte piante del genere Smilax (ved. Salsapariglia) a contenuto saponinico. Sembrerebbe quindi che l'attività antileprosa sia una proprietà comune a molte piante che contengono saponine, lo studio delle quali, sotto questo aspetto, meriterebbe di essere maggiormente approfondito.
L'azione terapeutica della Saponaria è dovuta alla presenza nella sua composizione di saponine, sostanze molto diffuse in natura, le cui principali caratteristiche farmacologiche sono quelle di diminuire la tensione superficiale, di aumentare la permeabilità cellulare, di produrre emolisi, di irritare i tessuti con cui vengono poste a contatto, e di essere dotate di proprietà schiumogene ed emulsionanti per le quali la Saponaria venne impiegata in tutti i tempi, anche come detergente.
Le saponine sono poco assorbite dalle mucose gastro-intestinali ma possono facilitare l'assorbimento di altre sostanze [Kofler e Fischer (19)]. La tossicità di alcune di esse è notevolmente elevata (sapotossine).
Iniettate direttamente in circolo esse provocano i fenomeni tossici a loro caratteristici: convulsioni seguite da indebolimento o paralisi della attività motoria, depressione cardiocircolatoria e respiratoria, infiammazione degli organi emuntori, emolisi, ematuria, gastroenterite e diarrea ematica. Le dosi elevate possono riuscire rapidamente mortali.
Iniettate per via sottocutanea esse determinano la stessa sintomatologia ma più attenuata. Applicate localmente le saponine determinano irritazione, aboliscono la contrattilità muscolare e la conducibilità nervosa [Yagi (20), Kobert (21)].
I pesci sono molto sensibili all'azione delle saponine le quali possono esercitare le loro proprietà ittiotossiche anche a forti diluizioni.
Somministrate per bocca esse vengono poco assorbite dalle mucose del tratto gastro-intestinale sulle quali determinano per ciò, soltanto effetti locali con sintomi di vomito, gastroenterite più o meno grave, diarrea persistente. Soltanto dopo che l'integrità della mucosa intestinale è stata alterata dalla loro azione locale, esse possono essere assorbite ed esplicare anche un'azione generale.
La tossicità delle diverse saponine è proporzionale al loro potere emolitico e può variare da 10 a 100 volte, a seconda che siano introdotte nell'organismo per via endovenosa o per via enterale.
Somministrata a piccole dosi la Saponaria, sotto forma dei suoi preparati galenici, agisce come espettorante, diuretico e diaforetico. A dosi elevate provoca gli stessi fenomeni tossici già descritti per le saponine.
Recentemente Vacek e Kozlik (22) hanno studiato l’azione delle saponine ottenute dalla Saponaria e da diverse altre droghe, sulla corticale surrenalica di ratti ipofisectomizzati. Essi hanno constatato che la concentrazione di vitamina C nel tessuto corticosurrenalico subiva una riduzione significativa dopo l’iniezione sottocutanea di dosi superiori a 1 mg/kg,
Impiegata a piccole dosi, la Saponaria agisce come espettorante, diuretico e diaforetico.
Estratti e preparati vari
a) Estratto fluido (g 1 = LV gtt).
Dosi: g 1-2 pro die.
b) Estratto molle acquoso (1 p. = 4 p. circa di droga).
Dosi: g 0,25-0,5 pro die.
Preparazioni usuali e formule galeniche
Tintura
Estratto fluido saponaria……………………………………………… g 20
Alcool di 20° …………………………………………………………. g 80
(g 5-10 pro die).
Sciroppo
Estratto fluido saponaria …………………………………………….. g 5
Sciroppo semplice F. U. …………………………………………….. g 95
(a cucchiai).
BIBLIOGRAFIA
(1) WEHMER C., Die Pflanzenstoffe, II ed., p. 303 – (2) KON G. A. R. e SOPER H. R., I. Chem. Soc.. 617, 1940 – (3) KARRER P., FIORONI W., WIDMER R. e LIER H., Helv. Chim. Acta, 7, 781, 1924 • (4) RUZICKA L. e VAN EEN A. G., Ree. Trav. Chim., 48, 1018, 1929 – (5) RUZICKA L. e GIACO- MELLO G., Helv. Chim. Acta, J9, 1136, 1936; 20, 299, 1937 • (6) RUZICKA L., JEGER O. e VOGEL A., ibidem, 34, 2321, 1951 • (7) PAWELCZYCK E. e DROZDZ B., Farm. Polska, 9, 38, 1953; Chem. Abs., 48, 5301 f, 1954 – (8) DROZDZ B., Diss. Pharm., 13, 171, 1961 – (9) BOZENA PASICH, ibidem, 13, 1, 1961 – (10) HEEGER E. F. e BRUCKNER K., Pharmazie, 7, 177, 1952 • (11) BALANSARD, Prod. Pharm., 7, 457, 1952 – (12) BARGER G., I. Chem. Soc., 89, 1210, 1906 • (13) PERKIN A. G., ibidem, 73, 1019, 1898 – (14) CAMBIE R. C., Chem. Ind., 87, 1959 – (15) EVANS W. H., MCGOOKIN A., JURD L., ROBERTSON A. e WILLIAMSON W. R. N., J. Chem. Soc., 3510, 1957 – (16) NAKAOKI T., J. Pharm. Soc. Japan, 64, 57, 1944 • (17) BRIGGS L. H. e CAMBIE R. C., Tetrahedron, 3, 269, 1958 – (18) SEIKEL M. K. e GEISSMAN T. A.^ Arch. Biochem. Biophys., 71, 17, 1957 – (19) KOFLER e FISCHER, Arch. exp. Path. u. Pharmakol., 130, 319, 1928 • (20) YAGI, ibid., 54, 141, 1911 – (21) KOBERT, Biochem. Handtex, 7, 1914 – (22) VACEK L. e KOZLIK V,, Arznetm.-Forsch., 11, 325, 1961.

