Salsapariglia
Tratto da “Piante Medicinali – Chimica, Farmacologia e Terapa” di R. Benigni, C. Capra e P.F.Cattorini
(da due parole indiane sarsa o zarça = rovo e parilla = piccola vite, cioè pianta che ha della vite e del rovo) (Lemery).
Con questo nome si indicano gli elementi radicali (rizomi e radici) di varie specie di Smilax americane (e asiatiche), che giungono in commercio in diverse varietà. Non sempre è agevole riferire le varietà commerciali ad una data specie.
Fam. – Liliacee/Smilacee.
Salsapariglia- Ultimo aggiornamento pagina: 27/02/2018
Indice dei contenuti
- Generalità
- Componenti principali
- Proprietà farmacologiche
- Estratti e preparati vari
- Preparazioni usuali e Formule
- Bibliografia
Generalità

Nomi volgari – Sarsaparille (ted.), the medicinal smilax Salsaparilla (ingl.), sarzaparilla (spagn.), salsaparilha (port.) , salsapareille (fr.).
Le qualità commerciali della Salsapariglia si possono suddividere in quattro gruppi.
1° – Salsapariglia di Vera Cruz e di Tampico, detta del Messico o spagnola, ricavata dalla Smilax medica Schiecht, detta mecapatli.
2° – Salsapariglia della Giamaica, detta Salsapariglia rossa o barbuta, ricavata dalla Smilax ornata Lem. (sin. – Smilax macrophylla var. maculata Vers.).
3° – Salsapariglia dell'Honduras, detta, pur essa, Salsapariglia spagnola, ricavata dalla Smilax officinalis Humb. (sin. – Smilax saluberrima Gilg. – Smilax utilis Hemsley).
4° – Salsapariglia del Brasile, detta del Parà, del Portogallo o di Lisbona, che si ricava da varie specie: Smilax pseudosyphylitica Kunt., Smilax papiracea Poiret ed altre.
La Salsapariglia di Vera Cruz e di Tampico è la più ricercata ed è abbastanza rara. Proviene dal Messico (Vera Cruz, versante orientale delle Ande, Orizaba, da Manzanilla — costa orientale del Messico — da Tuzpani, Hidalgo, S. Luis Potosi, Tamaulipa). E' di color grigio/giallastro o grigiastro (Tampico), grigio/bruno (Manzanilla) ed anche grigio/rossastro.
La Salsapariglia della Giamaica proviene dal Guatemala — via Giamaica — è di color bruniccio o bruno/rosso, con molte radichette avventizie (da ciò, barbuta).
La Salsapariglia dell'Honduras proviene dall'Honduras e, in parte, dal Nicaragua, è di color grigio/giallastro o bruno/gialliccio o grigio/brunastro. L'interno è farinoso, di color bianco/roseo. E' stimata.
La Salsapariglia del Brasile proviene dal Parà e dall'Amazonia. E’ di colore grigiastro o nero/rossastro (perchè sottoposta a fumigazione). Specie secondarie sono le Salsapariglie dette di Caraques (o di Caracas) provenienti dalla Nuova Granata, dal Venezuela e Costarica. Sono di color bruno/pallido, tendenti qua e là al rossiccio, con solchi larghi.
In commercio queste varie specie sono distinte con nomi desunti dalla grossezza delle radici. E’ detta fiorettino (o fine) la più sottile e legnosa; fioretto o fioretta, quella di grossezza mediocre; fiorettone la più grossa e finalmente grossa o stragrossa, quella che ha un diametro di un cm.
Il diametro varia da 3 a 5 sino a 8-10 mm circa (in media, quello d'una penna d'oca). Giungono in commercio raccolte nei c.d. «sigari» formati dalle radici (lunghe da 1 m. a 1,50 m.) ripiegate più volte su se stesse, in modo da formare un fascio lungo circa 30-40 cm e grosso 5-7 cm strettamente avvolto, per tutta la lunghezza, con altre radici ed anche con liane.
Si trovano in commercio anche sciolte, spesso ancora unite a pezzi di rizoma.
Sono anche suddivise in due gruppi: Salsapariglie dell'America centrale (del Messico, Vera Cruz, Tuzpan, Manzanilla, Giamaica, Honduras, Guatemala); Salsapariglie dell’America del Sud (Brasile, Parà, di Guayaquil, di Lima e di Caraques).
Le specie asiatiche sono:
— Smilax China L. (Cina, Giappone, Indie or.) (Nepal, Khasia, Sikkim) Assam. E’ la c.d. «squine» (sin. – Smilax ferox Wall. – S. japonica A. Gray – Coprosmanthus japonicus Nunth.) in cinese T’ou fou ling; Cay-khuc-khac (Cocincina).
— Smilax lancaefolia Roxb. e la S. glabra Roxb. (Cina, Giappone, Corea, India, Assam, Persia, Mar Caspio).
Sono grossi pezzi arrotondati o allungati, brunastri esternamente e rosei nell'interno, duri, inodori, di sapore acre.
Etimologia – Smilax (o zmilax) dal greco smilax = smilace o edera spinosa. Il nome si ricollega al mito di Smilax, la fanciulla che, morta d'amore per il giovane Crocus, fu mutata nella pianta (Ov. Met. 4283). Secondo altri, da smilh = stilo, coltello, per gli aculei.
Falsificazioni – Le radici di Salsapariglia possono essere falsificate con quelle della Aralia nudicaulis L. (fam. Araliacee) (U.S.A.) (Virginia), della Herreria stellata H. Br. (fam. Liliacee) (Brasile), del Philodendron acerum Schott. (fam. Aracee), della Passiflora incarnata L. (fam. Passifloracee) (U.S.A. – Brasile), della Carex arenaria L. (fam. Ciperacee), la c.d. Salsapariglia di Germania, della Smilax aspera L., la c. d. Salsapariglia nostrale, d'Italia o di Spagna.
Sostituzioni grossolane sono le radici di Asparagus, di Solanum Dulcamara L., radici di Smilax officinali esaurite (bollite).
Le specie officinali non vanno confuse con la Salsapariglia indiana data dalle radici dell’Hemidesmus indicus R. Br. (fam. Asclepiadacee) il «nunnari», nè con la Salsapariglia del Texas – Menispermum canadense L. (fam. Menispermacee) (U.S.A. – Canada, Québec, Manitoba) (Yellow Parilla, Canada Moonseed).
Parti usate – Le radici (Sarsaparillae radix F.U.).
Componenti principali
Saponine, che sono state designate con diversi nomi, pariglina, parillina, salseparina, smilacina, acido parillinico (1). Probabilmente le diverse specie di Smilax contengono saponine differenti. Le sostanze saponiniche attualmente riconosciute quali componenti delle radici di Salsapariglia sono le seguenti:
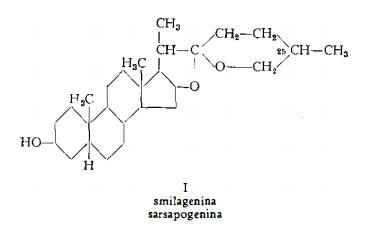
1) Sarsaponina è stata cosi denominata da Schulz (2) che l’ha estratta dalla Smilax medica Cham. e Schl. Con lo stesso nome Power e Salway (3) hanno denominato una saponina estratta dalla Smilax ornata Hook Fil., probabilmente identica alla sarsaponina della S. medica. In seguito alle ricerche, eseguite sui prodotti di idrolisi (3-5) e sulla composizione chimica della genina (6) (7), si è dedotto che la scissione idrolitica della sarsaponina produce 2 molecole di glucosio, una molecola di ramnosio e l’aglucone sarsapogenina, con la composizione centesimale C27H44O3 (6) e con la formula di struttura steroidica I (7).
2) Smilagenina, C27H44O3, è stata isolata per la prima volta nella quantità dello 0,02% da Askew, Farmer e Kon (8) dalle radici della Smilax ornata Hook, dopo idrolisi operata su un estratto. E’ stata identificata alla isosarsapogenina (9), derivante dalla sarsapogenina per trattamento con acido cloridrico (7). La smilagenina ha formula strutturale riferibile a quella della sarsapogenina, dalla quale differisce per la presenza di un C asimmetrico in posizione 25 (10).
3) Dalle radici della Smilax ornata Lem. Paris, Vaillant e Bénard (11) hanno separato un saponoside, producente per idrolisi glucosio, galattosio e sarsapogenina e quindi diverso dalla sarsaponina della Smilax medica. Gli stessi AA. (11) dalla Smilax Japicanga Griseb hanno estratto un’altra saponina, da cui, per idrolisi acida, sono stati ricavati glucosio, galattosio, ramnosio ed una genina, che sembra isomera della sarsapogenina.
Il titolo di saponosidi grezzi delle radici della Smilax ornata, della S. medica e della S. Japicanga, secondo le analisi di Paris e coll. (11), è risultato essere di 5,1%, 6,6% e 4,1% rispettivamente.
Nel genere Smilax, Altman (12) ha trovato 0,47% e 0,50% di sapogenine.
Nella Smilax aristolochiaefolia e precisamente in due campioni di radici con umidità 9,6% e 7,8% rispettivamente. Girai e Aguilar (13) hanno dosato un contenuto di vitamina C pari a mg 20,4% e 14,8% nella droga fresca ed a mg 22,6% e 16,1% nella droga secca rispettivamente.
Nella Smilax aspera: olio essenziale contenente metilvanillina e piperonale (14).
Lo studio anatomico delle specie Smilax auriculata Walt., S. hispida Muhl., S. glauca Walt., S. bona-nox L. e S. herbacea L., ha messo in evidenza che nei rizomi sono contenuti mucillaggine, rafidi di ossalato di calcio ed amido (15).
Nelle radici della Smilax ornata Lem., della S. medica Schlecht et Cham., e della S. Japicanga Griseb., Paris e coll. (11) hanno trovato un titolo di acqua pari a 7,59%, 11 % e 8,6% e di ceneri pari a 12%, 11,5% e 5,4% rispettivamente.
Altri componenti delle radici di Salsapariglia: olio essenziale e olio grasso, resina 2,5%, amido ca. 50%, zuccheri (16), tannino (17) (18), alcool cetilico (4), sitosterolina, C35H60O6 (3), stigmasterina (3), b-sitosterina ed e-sitosterina (19).
Proprietà farmacologiche ed impiego terapeutico
La Salsapariglia venne introdotta in Europa attraverso la Spagna nel 1536, ma essa era largamente usata nella medicina dei paesi di origine già da molto tempo prima che vi giungessero gli spagnoli.
Essa deve alla sua fama di potente antiluetico, fama accreditata dai più noti medici dell’epoca, quali il Lusitanico, il Falloppio, il Cardano, il Ximenes, il Guidi, il Cesalpino, la sua rapida diffusione in tutti i paesi d’Europa e il suo incontrastato impiego, per circa due secoli, come sovrano rimedio antiluetico.
Verso il principio del 1700 essa venne tuttavia dimenticata per un certo periodo, sino cioè al 1757 allorché venne ancora rivalorizzata da Fordice (20), il quale ne preconizzò l’uso oltre che come antiluetico, nel trattamento del reumatismo cronico, di varie malattie cutanee e della scrofolosi.
Con tali indicazioni la Salsapariglia venne ancora impiegata sino al principio del 1800, epoca in cui il suo uso venne quasi completamente abbandonato dai medici i quali continuarono a prescriverla, a volte, soltanto come depurativo, per le sue proprietà diuretiche e diaforetiche.
In realtà occorre riconoscere che le sue proprietà antiluetiche non vennero mai seriamente confermate anche se in epoca alla nostra relativamente più vicina, Perutz (21), in base ai risultati desunti da un’estesa rassegna critica dei dati più recenti, giunse alla conclusione che l’uso della Salsapariglia può essere di considerevole utilità nel trattamento della lue e che questa sua azione è dovuta alla stimolazione dei poteri di difesa dell'organismo.
Philippsohn (22) riferì di aver ottenuto buoni risultati nel trattamento della psoriasi e l'attività della droga in questi casi, venne in seguito confermata da Grutz e Berger (23), da Ritter (24), da Thurmon (25) e Deneke (26) spiegò quest'azione da lui stesso constatata, attribuendo alla Salsapariglia un'azione favorente l'eliminazione della colesterina. Tale azione venne però successivamente negata da Lasch e Perutz (27) i quali, in base ai risultati di esperienze eseguite sugli animali e sull’uomo, negarono che la droga possa comunque influenzare la colesterinemia, a meno che essa non venga somministrata a dosi tali da determinare un effetto irritante sulle mucose del tubo digerente.
Rittmann e Schneider (28) dimostrarono che la Salsapariglia è dotata di una notevole azione diuretica, azoturica e ipoazotemica, ciò che venne più tardi confermato da Falzoi e Bertazzoni (29).
Questi AA. studiarono l’azione della Salsapariglia sulla diuresi, sulla azotemia, sull’uricemia e sull'eliminazione urinaria dell'acido urico, su 15 pazienti iperazotemici e su 5 normali. Essi poterono così stabilire che la diuresi non è sensibilmente influenzata, per quanto sia possibile notare una tendenza, sia pur di modica entità, ad una maggior eliminazione giornaliera di urine.
L’azotemia sarebbe invece nettamente influenzata nei soggetti iperazotemici, nei quali essa subisce una costante diminuzione; negli individui normali tale azione non sarebbe invece dimostrabile.
L’eliminazione ureica percentuale e globale, è costantemente aumentata sia nei normoazotemici che negli iperazotemici, mentre l'uremia è sensibilmente influenzata nel senso di una netta diminuzione, solo nei casi di iperuricemia.
Il tasso percentuale globale dell'acido urico urinario viene costantemente aumentato tanto nei soggetti patologici quanto in quelli normali.
Il comportamento dei corpi aromatici nel sangue, segue invece le variazioni azotemiche, riportandosi alla normalità con la normalizzazione e la diminuzione dei valori rappresentativi dell'azoto non proteico. Gli AA. concludono che, in via di ipotesi logica, si può ammettere per la Salsapariglia un duplice punto di attacco; il primo indirettamente sul metabolismo ureico e nucleinico, tramite un'azione a livello del fegato; il secondo sul meccanismo di escrezione renale, tramite un aumento funzionale dei poteri di concentrazione di quest'organo.
Dal punto di vista terapeutico gli AA. concludono che l'azione della Salsapariglia sull'azoto non proteico, si rivela con una diminuzione di molti dei disturbi soggettivi lamentati dai pazienti (riduzione della cefalea, attenuazione del vomito, miglioramento della fenomenologia parestesica e irritativa ecc.). Tale azione mancherebbe però nei casi gravissimi con lesioni anatomo-funzionali irreversibili, come per es. nel coma uremico con forte tossicosi aromatica.
Pur tuttavia, se non uniformemente e nella totalità dei pazienti, la Salsapariglia, associata o meno ad altre pratiche terapeutiche, sarebbe in grado secondo gli AA., di dare risultati favorevoli in molte delle forme morbose che decorrono con un aumento nel sangue e nei tessuti dei cataboliti del ricambio azotato.
Chessa (30) aveva invece precedentemente negato che la droga fosse capace di influenzare l'azotemia e la funzionalità renale ma, commentano Falzoi e Bertazzoni. Chessa stesso ammette di aver sperimentato su casi normali o quasi e di aver impiegato la droga a dosi minime; dai protocolli riportati, se pur non è percepibile un effetto costante, è pur vero che nella maggior parte dei casi, sono state osservate diminuzioni, sia pur modiche, dell'azotemia. D’altro lato, affermano i suddetti AA., i risultati da essi ottenuti su individui normali, collimano perfettamente con quelli ottenuti dal Chessa ed essi stessi confermarono l'azione incostante del farmaco, dovuta in parte a caratteristiche reattive individuali e in gran parte all'impossibilità di ottenere una risposta positiva all’azione del farmaco, da parte di elementi parenchimali irreversibilmente alterati anatomicamente e funzionalmente.
Un’altra attività riscontrata nella Salsapariglia e degna di attenzione, è quella antileprosa, attività sulla quale è stato attirato anche recentemente l'interesse di alcuni ricercatori.
Paris, Vaillant e Bénard (11) fanno notare a questo proposito, il fatto interessante che in paesi anche molto lontani fra loro, figurino nella terapia antileprosa alcuni vegetali appartenenti al genere Smilax (31-32) e Rollier (33-35) recentemente, ha sperimentato una varietà di Salsapariglia, la Salsapariglia rossa (Smilax ornata Lem.) del Marocco, nella terapia di varie forme di lebbra, con risultati sorprendenti.
La composizione di questa droga venne recentemente studiata da Paris e coll. (11), i quali riuscirono ad isolare da essa, un saponoside che si distingue dalla sarsaponina contenuta nella Smilax medica, per la composizione della catena zuccherina, ma avente in comune l’aglicone sarsapogenina (ved. parte chimica).
Per quanto riguarda le indicazioni terapeutiche che possono essere attribuite alla Salsapariglia, esse derivano soprattutto dalle sue proprietà diuretiche e detossicanti generali che si manifestano con un aumento della eliminazione dei cataboliti con relativo aumento dei valori dell'acido urico urinario. Dai risultati ottenuti da Falzoi e Bertazzoni, risulta «Che la Salsapariglia influenza direttamente o indirettamente il tenore dell'acido urico nel sangue, soltanto quando esso raggiunge limiti superiori alla norma, vale a dire quando esso assuma il reale significato di scoria azotata tossica per l'organismo». Essa sarà pertanto indicata, sola od associata ad altri farmaci, nella terapia delle malattie del ricambio (diatesi artritica, uricemia, gotta, alcune malattie della pelle su base dismetabolica). Falzoi e Bertazzoni ottennero buoni risultati nei diversi gruppi di pazienti da essi studiati, nei quali erano compresi nefropatici, cardiopatici, epato-colecistopazienti e soggetti colpiti da malattie febbrili generiche.
In base alle considerazioni del Perutz, la Salsapariglia potrebbe trovare utile indicazione come coadiuvante nella terapia antiluetica e, secondo le più recenti acquisizioni sull'attività di questa droga, essa può essere annoverata fra i più interessanti farmaci ad azione antileprosa.
Estratti e preparati vari
a) Estratto fluido F.U. (g 1 = XLVI gtt).
Dosi: g 1-10 pro die.
b) Estratto secco idroalcoolico (1 p. = 10 p. circa di droga).
Dosi: g 0,1-1 pro die.
Preparazioni usuali e formule galeniche
Tintura
Estratto fluido salsapariglia F.U………………………………….. g 20
Alcool di 50°……………………………………………………………….. g 80
(a cucchiaini).
Sciroppo
Estratto fluido salsapariglia F.U. ………………………………… g 5
Sciroppo semplice F.U. ……………………………………………… g 95
(a cucchiai).
BIBLIOGRAFIA
(1) WEHMER C., Die Pflanzenstoffe, li ed., p. 161 – (2) SCHULZ W. V., Inaug. Dissert. Dorpat 1892; Arbeit. Pharm. Inst. Dorpat., 14, 30, 1896 – (3) POWER F. B. e SALWAY A. H., J. Chem. Soc., 105, 201, 1914 – (4) KAUFMANN H. P. e FUCHS C., Ber., 56, 2527, 1923 – (5) VAN DER HAAR A. W., Ree. Trav. Chim, 48, 726, 1929; Chem. Zbl., I, 687, 1930 – (6) SIMPSON J. C. E. e JACOBS W. A., J. Biol. Chem., 109, 573, 1935 – (7) MARKER R. E. e ROHRMANN E., J. Am. Chem. Soc., 61, 846, 1939 – (8) ASKEW F. A., FARMER S. N. e KON G. A. R., J. Chem. Soc., 1399, 1936 – (9) KON G. A. R., SOPER H. R. WOOLMAN A. M., ibid., 1201, 1939 – (10) SCHEER J., KOSTIC R. B. e MOSETTIG E., J. Am. Chem. Soc., 77, 641, 1955 – (11) PARIS R., VAILLANT M. e BÉNARD M., Ann. pharm. franf., 10, 328, 1952 – (12) ALTMAN R. F. A., Bol. téc. inst. agron. notte., 31, 67, 1956; Chem. Abs., 52, 506, 1958 – (13) GIRAL F. e AGUILAR M. D., Ciencia, Mex., 12, 283, 1953; Chem. Abs., 48, 4177b, 1954 – (14) SALGUES R., Compt. rend., 241, 987, 1955; Chem. Abs., 50, 897li, 1956 – (15) CAPONEm J. D. e QUIMBY M. W., J.A.Ph.A., ed. sci., 45, 691, 1956 – (16) KOMMENTAR ZUR PHARMACOPOEA HELVETICA V, 1947, p. 699 – (17) WALL M. E., FENSKE C. S.. KENNEY H. E., WILLAMAN J. J., CORRELL D. S., SCHUBERT B. G. e GENTRY H. S., J.A.Ph.A., ed. sci., 46, 653, 1957 – (18) WALL M. E., KRIDER M. M., KREWSON C. F., ROLAND EDDY C., WILLAMAN J. J., CORRELL D. S. e GENTRY H. S., ibidem, 43, I, 1954 – (19) SIMPSON J. C. E. e WILLIAMS N. E., J. Chem. Soc., 733, 1937 • (20) FORDlCE, cit. da OSOL A. e FARRAR
G. in The Dispensatory of the U.S.A., 25“ ed., 1960, p. 1215 – (21) PERUTZ, Handbuch der Haut- und
Geschlechteskrank., 1928 – (22) PHILIPPSOHN, Derm. Woch., 93, 1220, 1931 – (23) GRUETZ e BURGER, Klin. Woch., 12, 373, 1933 – (24) RlTTER, Dstch. med. Woch., 62, 1629, 1936 – (25) THURMON, New. Eng. J. Med., 227, 128, 1942 – (26) DENEKE, Dtsch. med. Woch., n. 9, 1936 -(27) LASCH e PERUTZ, Wien. Klin. Woch, 1925 – (28) RITIMANN e SCHNEIDER, Klin. Woch., n. 9, 401, 1930 – (29) FALZOJ
M. e BERTAZZONI G., Giorn. di Clin. Med., 21, n. 5, 1940 – (30) CHESSA, Accad. Med., n. 5, 479, 1939 – (31) NOTHNAGEL H. e ROSSBACH M. J., Nouveaux éléments de Matière Medicale et de Thérapeutique Baillière, Paris, 1880, p. 449 – (32) WILDEMAN E., Mém. Inst., Royal Colonial Beige, 13, 62, 1948 •
(33) ROLLIER R., Maroc Médical, 29, 238, 1950 – (34) ROLLIER R., NOURY, WEISGERER e MAURY, ibid, n. 316, 776, 1951 – (35) ROLLIER R., Inst. Leprosy, 27, 328, 1959.

