Piretro c.d. romano
Tratto da “Piante Medicinali – Chimica, Farmacologia e Terapa” di R. Benigni, C. Capra e P.F.Cattorini
(Anacyclus Pyrethrum DC. – Fam. Composite) (Sin. – Anthemis Pyrethrum L.)
Piretro c.d. romano- Ultimo aggiornamento pagina: 27/02/2018
Indice dei contenuti
- Generalità
- Componenti principali
- Proprietà farmacologiche
- Estratti e preparati vari
- Preparazioni usuali e Formule
- Bibliografia
Generalità

Etimologia – Anacyclus, dal greco anakuklwsis = circonvoluzione, allusione all’ala che contorna certi acheni, da anakuklhsis = giro (anakuklew = rigiro).
aneu = senza e kuklos = anello, cerchio, cioè senza cerchio di ligule nei capolini.
Anthemis, dal greco anqemis = piccolo fiore, antico nome della Camomilla da anqemos = fiore.
Pyrethrum, dal greco pureqron, da puressw = ho la febbre, cioè pianta febbrifuga. Secondo altri da pur = fuoco e aiqw = brucio, per il sapore bruciante.
Nomi volgari – Salivaria (port.), parietaire d’Espagne, oeil de bouc, racine pour les dents, racine salivare (fr.), Bertram, pyretrum romanum (ted.), pellitory of Spain (ingl.), zebne ziele (pol.), piretro d'Africa, piretro salivario, agher ghereha (arabo, nome di origine iraniana), a’aqirqarh’à e a’qerqer, marocch.), igent’es e tigent'est (berbero, regione di Azrou). In Tripolitania: Ud el hamm, ud ghindisc, saleh Lendar, sono probabilmente radici della pianta (si dicono di provenienza marocchina).
Habitat – Asia, Asia Minore, Turchia, Siria, Africa settentrionale (Tunisia, Algeria), Marocco (nella regione di Fès, il bacino de la Moluouya, il medio, il grande e l’anti-Atlante).
Parti usate – La radice.
Componenti principali
Pellitorina è la sostanza dotata di proprietà insetticide, isolata da Parisel (1) nel 1834 dalle radici dell’Anacyclus Pyrethrum DC. Il nome di «piretrina», dato da Parisel, fu mutato in pellitorina da Dunstan e Garnett (2). Fu estratta dalle radici del Piretro in quantità pari allo 0,43 % da Ott e Behr (3), allo 0,038 % da Gulland e Hopton (4) ed allo 0,14 % da Jacobson (5). La composizione chimica della pellitorina è stata studiata da Ott e Behr (3), da Gulland e Hopton (4), da Jacobson (5) e da Crombie (6) (7). Quest’ultimo, in base all’esame dei prodotti di sintesi, ha considerato inesatta la formula di struttura proposta da Jacobson (5). Secondo Crombie (6) la pellitorina, esaminata dai precedenti AA., non era una sostanza unica, ma una miscela di almeno tre isobutilamidi di formula generale (I):
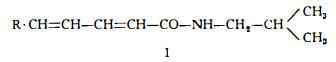
Alla principale di queste isobutilamidi Crombie (7) ha assegnato la seguente formula, equivalente a quella dell’N-isobutildeca-trans-2:trans-4-dienamide (II):
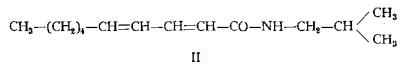
— Anaciclina, C18H25ON, Questa sostanza, con proprietà scialagoghe e debolmente insetticide, è stata estratta da Crombie (8) dalle radici dell’Anacyclus Pyrethrum DC. nella quantità dello 0,03-0,07%. E’ la N-isobutiltetradeca-trans-2:trans-4-diene-8:10-diinamide (III), composizione determinata da Crombie (8) e confermata per sintesi dallo stesso Crombie e Manzoor-I-Khuda (9) e da Bohlmann e Inhoffen (10).
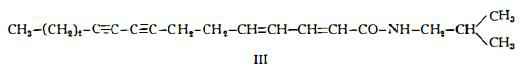
— Deidroanaciclina, C18H23ON, è stata isolata dall’Anacyclus Pyrethrum DC. da Crombie e Manzoor-I-Khuda (9). E’ stata trovata nelle forme di N-isobutiltetradeca-trans-2:trans-4:cis-12- e di N-isobutil-tetradeca-trans-2:trans-4:trans-12-triene-8:10-diinamide (IV) (9).
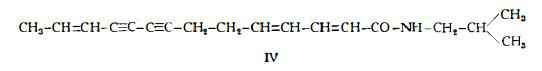
Nelle radici del Piretro sono stati inoltre trovati inulina 33 %, sino a 57 %, tracce di olio etereo e grasso con acido stearico (11).
Proprietà farmacologiche ed impiego terapeutico
Scialagogo, antalgico, antiparassitario. Usato specialmente come antiodontalgico, per la preparazione di colluttori e gargarismi e, esternamente, come antiparassitario.
Estratti e preparati vari
Estratto fluido (g 1 = XLVIII gtt).
Dosi: I-II gtt pro dose diluite in acqua come colluttorio.
Preparazioni usuali e formule galeniche
Tintura
Estratto fluido piretro g 10
Alcool di 60° g 90
(V-X gtt diluite in acqua come colluttorio).
Colluttorio
Tintura di piretro……………………………….. g 5
Acqua distillata…………………………………. g 300
BIBLIOGRAFIA
(1) PARISEL L. V„ Lieb. Ann., 9, 327, 1834 – (2) DUNSTAN W. R. e GARNETT H., J. Chtm. Soc., 67, 100, 1895 – (3) OTT E. c BEHR A., Ber., 60, 2284, 1927 – (4) CULLANO I. M. e HOPTON G. U., J. Chem. Soc., 6, 1930 – (5) JACOBSON M„ J. Am. Chem. Soc., 71, 366, 1949 – (6) CROMBIE L„ J. Cììem. Soc., 4338, 1952 – (7) CROMBIE L„ J. Chem. Soc., 999, 1955 – (8) CROMBIE L„ Nature, 174, 832, 1954 –
(9) CROMBIE L. e MANZOOR-I-KHUDA M„ Chem. Jnd., 409, 1956; J. Chem. Soc., 2767, 1957 –
(10) BOHLMANN F. e INHOFFEN E., Ber., «9. 1276, 1956 – (11) WEHMER c„ Die'PflinàeiKtolIe II ed, p, 1231.


