Cascara Sagrada
Tratto da “Piante Medicinali – Chimica, Farmacologia e Terapa” di R. Benigni, C. Capra e P.F.Cattorini
(Rhamnus purshiana DC. – Fam. Rhamnacee/Rhamnee))
Cascara Sagrada- Ultimo aggiornamento pagina: 27/02/2018
Indice dei contenuti
- Generalità
- Componenti principali
- Proprietà farmacologiche
- Estratti e preparati vari
- Preparazioni usuali e Formule
- Bibliografia
Generalità

Etimologia – Cascara sagrada – Corteza sagrada, Corteccia sacra. Nome dato dagli Spagnoli, nell'erronea opinione o nell'intento di far credere che il legno si identificasse con quello di Shittim, usato per costruire l'Arca dell'Alleanza.
Rhamnus, dal nome greco della pianta ramnos forse derivato da ramfos = rostro adunco, per le spine ricurve di talune specie (per es. R. infectoria L., R. cathartica L. o Spino cervino).
Purshiana – dedicato da De CandoIle ( 1825) al naturalista americano Federico Traugott Pursh che, sotto il nome di Rhamnus alnifolia, lo segnalò per primo nel 1805.
Nome volgare – Cascara Sagrada.
Habitat – Territori dell'America del Nord del versante del Pacifico, Stati di Washington, Oregon, California, Idaho, rive del fiume Kookoosky. Nevada, Arizona, Colorado, Columbia Britannica. Coltivato nel Kenia (corteccie sottili)
Albero.
Parti usate – La corteccia dei rami e del tronco (Rhamni purshianae cortex F.U.).
Componenti principali
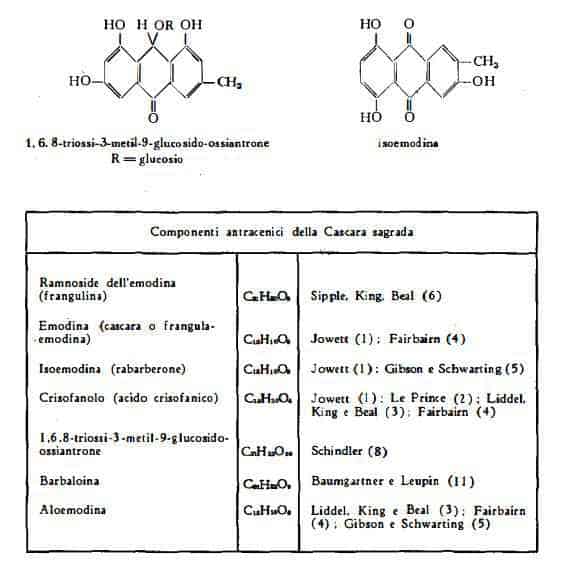
Composti antronici, antranolici (instabili) ed antrachinonici (stabili), liberi e combinati in forma glicosidica: a) emodina (1) (4) (= cascara- o frangula-emodina, 1,6,8-triossi-3- metilantrachinone); b) acido crisofanico o crisofanolo (1,8-diossi-3-metilantrachinone), la cui presenza è stata affermata da Le Prince (2), da Liddel e coll. (3) e da Fairbairn e coll. (4) e negata da Jowett (I) e da
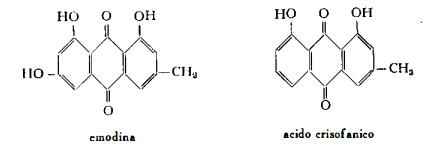
Gibson e Schwarting (5) : c} aloemodina (3) (4) (5) (1,8-diossi-3-ossimetilantrachinone – ved. Aloe): d) isoemodina (1) (5) (3,5,8-triossi-2-metilantrachinone): e) ramnoside dell'emodina (6) [= frangulina (7) ];
f) 1,6,8-triossi-3-metil-9-glucosido-ossiantrone (8): g) “casantranolo” di Lee e Berger (9), complesso glicosidico da cui sono stati ottenuti aloemodinantranolo e glucosio; h) glicoside aloinosimile di Fairbairn e Mital (10); i) barbaloina (11) (ved. Aloe).
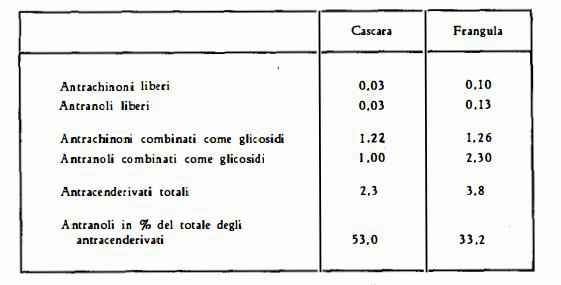
II contenuto di derivati antrachinonici della droga secca è risultato pari all’1,4-2 % di cui circa il 25 % combinati (1 2) (13). Auterhoff (14) ha trovato nella corteccia di cascara 0,03 % di antrachinoni liberi. 0,03 % di antranoli liberi, 1 % di antrachinonglicosidi e 1,22 % di antranolgli-cosidi, 2,3 % di antracenderivati totali, di cui il 53 % è costituito da composti antranolici. I valori che Auterhoff ( 14) ha trovato per analisi di corteccia di cascara e di frangula sono i seguenti (espressi in g % ):
Altri componenti: grasso circa 2 %, acido siringico, acidi linolico e miristico ( l), metilidrocotoina (= 2,4,6-trimetossi-benzofenone) ( 15), tannino 2,4 % secondo Jowett (1), assente invece secondo Peacock ( 16) ; inoltre un enzima presente nella droga fresca, secondo Meier e coll. ( 17), ma anche nella droga secca e vecchia, secondo Bauer e coll. ( 18). Jowett (1) ha identificato questo enzima con l'emulsina; Bauer e coll. (18) hanno segnalato che si tratta di un fermento arnilolitico, che non è distrutto dal riscaldamento a calor umido a 100° e che è parzialmente inattivato dal calore secco a 100° dopo sette giorni di riscaldamento, ma è riattivato per ebollizione con acqua.
Proprietà farmacologiche ed impiego terapeutico
Abbiamo svolto a proposito dell'Aloe la parte riguardante l'azione farmacologica generale dei composti antracenici, costituenti comuni delle droghe antraceniche e quindi anche della Cascara sagrada.
Per quanto riguarda questa droga in particolare, aggiungeremo che non essendo stata ancora completamente chiarita la sua costituzione chimica, anche le ricerche farmacologiche eseguite su di essa e su alcuni suoi principi attivi sono piuttosto scarse.
Lee e Berger ( 19) hanno isolato un complesso glicosidico dell'aloe-emodin-antranolo (casantranolo) e lo hanno descritto come responsabile delle proprietà purgative della droga stessa, mentre il glicoside dell'emodina di Sipple, King e Beai (20) sarebbe biologicamente inattivo.
Fairbairn e Mahran (21) esaminarono diversi campioni di corteccia e di estratto secco di Cascara e, titolandoli comparativamente col metodo chimico e col metodo biologico, ottennero risultati che potevano essere considerati soddisfacenti, ma i risultati di successive ricerche dimostrarono che in particolari condizioni di ossidazione si possono ottenere analiticamente risultati superiori. Secondo altri AA. inoltre, non esisterebbe un sufficiente parallelismo fra il titolo biologico e l’attività clinica [Mitchel e Fairbairn (22), Duncan (23)], ciò che potrebbe essere in relazione col fatto che i diversi animali reagiscono in maniera diversa all'azione della Cascara e dei composti antracenici in generale. Il topo è molto più resistente dell'uomo all'azione dell'aloina e, secondo Auterhoff (24) e Hazleton e Talbert (25), sarebbe meno sensibile alla Cascara che alla Frangola. Nei ratti invece l'azione della Cascara sarebbe positiva ma lenta (26). Impiegando la cavia, secondo Green, King e Beai (27), si otterrebbero risultati migliori. Secondo Paris e Moyse (28), soltanto il saggio sulla Daphnia magna, proposto da Viehower (29), data la scarsa e variabile sensibilità dei comuni animali da esperimento, sarebbe utilizzabile per la titolazione delle droghe antraceniche e dei loro preparati.
Metodi biologici per la titolazione delle droghe antraceniche sono stati descritti, fra gli altri da Loewe (30), da Hubacher e coll. (31), da Fairbairn (32), da Lou (33), da Lou e Fairbairn (34),
Come fu già detto a proposito dell'Aloe, la Raggi (35) avrebbe dimostrato che la Cascara sagrada (come anche altri Rhamnus) deve la sua attività, non soltanto ai composti antracenici noti, ma anche ad altri principi che non danno nessuna delle reazioni caratteristiche degli antrachinoni e che tuttavia manifestano la loro attività sia in vitro che in vivo (vedi Aloe).
Per quanto riguarda l’azione isolata ed associata dei diversi composti antracenici contenuti nella Cascara, Liddel, King e Beai (36), hanno dimostrato che l'associazione dei suddetti composti è biologicamente più attiva di quella dovuta ad ognuno di essi.
I suddetti AA. hanno isolato dalla corteccia di Cascara, l'Aloe-emodina (I) l'emodina (Il) e l'acido crisofanico (III) e trovarono che 25 mg di ogni sostanza somministrata isolatamente alla cavia, manifestava un'azione catartica lieve o trascurabile. L'azione di associazioni varie di due sostanze somministrate a dosi complessivamente uguali a quelle delle sostanze somministrate isolatamente, hanno manifestato un'azione leggera o moderata, mentre l’associazione delle tre sostanze (mg 10 della I. mg 10 della II e mg 5 della III) , dimostrò un'azione notevolmente più elevata di quella indotta da mg 25 di ciascuna di esse somministrate isolatamente.
Sull'attività purgativa dei principi attivi della Cascara, allorchè vengano somministrati parenteralmente, non esiste un completo accordo.
Alcuni studi in questo senso vennero eseguiti con una sostanza ottenuta dallo Tschirsch (37) cui fu dato il nome di «Peristaltina», nella cui composizione, secondo Tschirsch e Monikowski (38) entrerebbero alcuni glicosidi antracenici ma non sarebbero presenti antrachinoni liberi.
II Pietsch (39) che studiò sperimentalmente questa sostanza su conigli, cani e cavalli, concluse che essa, somministrata oralmente agisce come tutti gli altri purganti antracenici. Somministrata per via sottocutanea, agirebbe aumentando la peristalsi intestinale con conseguente effetto purgativo.
I riultati delle ricerche cliniche eseguite da diversi AA. (Walther (40), Bechamp (41), Linel (42), Massalongo e Piazza (43), Koch (44)], confermarono quelli sperimentali ottenuti dal Tschirsch, dimostrando che la Peristaltina iniettata alla dose di g 0,50 indurrebbe già un effetto purgativo senza dar luogo a spiacevoli fenomeni secondari.
Il Chistoni ( 45) al contrario, sperimentando su cavie, conigli e cani, giunse a risultati del tutto opposti e affermò che i glicosidi della Cascara sagrada (Peristaltina) non possono considerarsi come sostanze atte a produrre un effetto purgativo quando vengano somministrate per via sottocutanea.
Preparati di Cascara somministrati al cane per via endovenosa, determinano effetti tossici che si manifestano con caduta della frequenza delle contrazioni ventricolari e auricolari e con la morte dell'animale ( 46).
L'estratto privato della sostanza amara sarebbe, secondo Astruc e Giroux (46), meno tossico ma secondo Nelson (47), sarebbe anche meno attivo.
La Cascara sagrada è dotata di azione stomachica, lassativa o purgativa, secondo la dose impiegata e la sensibilità individuale verso questo tipo di droghe purgative.
L'azione non è, di solito, seguita da dolori o da altri disturbi secondari.
Come avviene per tutte le altre droghe della serie antracenica, la sua azione si svolge sull'intestino crasso (vedi Aloe) e, secondo alcuni, può manifestare anche una certa attività colagoga.
La droga fresca può dar luogo ad emesi ed a coliche, fenomeni questi attribuiti ad un albuminoide tossico, la ramnustossina e ad un enzima; tale azione scompare col tempo o col riscaldamento prolungato della corteccia a 100°.
L'Aitchison ( 48) ha descritto un caso di ipopotassiemia manifestantesi con alterazioni dell'attività cardiaca dimostrate elettrocardiograficamente e con una forte debolezza muscolare degli arti inferiori. L'A. riuscì a stabilire che tale stato di ipopotassiemia era dovuto indirettamente all'uso continuo di preparati di Cascara, cui seguì un'enterite diarroica cronica. In queste condizioni, l'aumentata eliminazione intestinale del potassio, non era compensata da un sufficiente apporto di questo elemento con la dieta.
I preparati di Cascara sono largamente impiegati, soli od associati con quelli di altre droghe ad azione simile, come lassativo nella terapia della stitichezza cronica. Non è consigliabile di usarli a dosi più elevate per ottenere un completo effetto purgativo perchè potrebbero dar luogo a fatti infiammatori intestinali [McGuigan (49)].
Bockus, Willard e Bank (50) hanno descritto casi di Melanosis coli, manifestantesi con una pigmentazione della mucosa del colon, dovuta ad uso prolungato di Cascara e Tyson (51) riferì di aver constatato un effetto lassativo del latte di nutrici cui erano stati somministrati preparati di Cascara.
I preparati di Cascara vengono per lo più somministrati la sera prima di coricarsi in un'unica dose: si è potuto constatare però che risultati migliori si ottengono somministrandoli a piccole dosi dopo i pasti.
L'associazione di preparati di Belladonna può essere utile nei casi di stitichezza spastica, che sono poi i più frequenti. L'utilità di questa associazione sarebbe invece dubbia allorchè viene prescritta allo scopo di evitare l'eventuale comparsa di dolori colici e ciò soprattutto perchè l'azione della Belladonna si esaurisce prima che l'effetto della Cascara (o delle altre droghe di questo gruppo) abbia cominciato a manifestarsi.
Estratti e preparati vari
a) Estratto fluido iperattivo (concentrato ed attivato) (g 1 = XXIX gtt).
Dosi: da X gtt a 1/2 cucchiaino pro dose.
b) Estratto fluido per tintura (g 1= XLIII gtt).
Dosi: 1/2-1 cucchiaino pro dose,
c) Estratto fluido F. U. (g 1 = XXXV gtt).
Dosi: come sopra.
d) Estratto fluido per sciroppo (g 1 = XXXV gtt),
Dosi: come sopra.
e) Estratto fluido decannizzato per sciroppo (g 1 = XXXII gtt).
Dosi: come sopra.
f) Estratto fluido deamarizzato e aromatizzato F. U. (g 1 = XXXII gtt).
Dosi: come sopra.
g) Estratto fluido deamarizzato e non aromatizzato (g 1 = XXVIII gtt).
Dosi: come sopra.
h) Estratto molle acquoso ( 1 parte = 4 p. circa di droga) .
Dosi: g 0,5-1 pro dose.
i) Estratto molle idroalcoolico F. U. (1 parte = 4 p. circa di droga).
Dosi: come sopra.
l) Estratto secco acquoso (1 parte = 5 p. circa di droga).
Dosi: g 0.4-0,8 pro dose.
m) Estratto secco idroalcoolico (1 parte = 5 p. circa di droga).
Dosi: come sopra.
n) Tintura al 20 % di droga.
Dosi: a cucchiai.
o) Compresse confettate (estratto secco di cascara cg 15 per una compressa).
Dosi: 1-3 compresse la sera.
Preparazioni usuali e formule galeniche
Tintura
Estratto fluido cascara p. tintura g 20
Alcool di 70°…………………………………….. g 80
(1-2 cucchiai pro dose)
Sciroppo di cascara
Estratto fluido cascara deamarizz. g 20
Sciroppo semplice F. U…………………… g 80
(1-2 cucchiai pro dose)
Sciroppo di cascara composto
Estratto fluido cascara deamarizz…………………………….. g 6
Tinture di noce vomica e genziana ana g 2
Sciroppo di arando amaro ………………………………………. g 60
(a cucchiaini prima dei pasti)
Elisir
Estratto fluido cascara…………………………………………… g 50
Estratto fluido arancio dolce alcool-idrosolubile…….. g 30
Sciroppo semplice F.U……………………………………………. g 600
Alcool di 95° … ………………………………….. g 220
Acqua q. b. a. . '…………………………………………………….. g 1000
(a cucchiaini)
Estratto composto lassativo
Estratto fluido cascara………………………………………………. g 24
Estratto fluido liquirizia………………………… g 35
Tintura di belladonna………………………………………………… g 5
( 1 cucchiaino pro dose)
Pillole lassative
Estratto molle idroalcoolico cascara . . g 0,2
Estratto molle idroalcoolico noce vomica g 0,002
Estratto secco idroalcoolico belladonna g 0,005
per 1 pillola.
(1-3 pillole pro dose)
Pillole lassative F. U. (Pilulae podophyllini et Rhamni purshianae)
Estratto molle idroalcoolico cascara………………….. g 0,20
Estratto molle idroalcoolico belladonna……………………… g 0.01
Podofillina……………………………………………….. g 0.01
(1-3 pillole pro dose)
Elisir cascara sagrada (B.P., B.N.F.)
Estratto fluido di cascara con aggiunta del 30 % v/v di glicerina e di aromatizzanti. (mezzo-un cucchiaino pro dose)
Pozione di cascara (B.N.F.)
Estratto fluido cascara………………………………………………… g 1,3
Ammonio carbonato…………………………………………………. g 0,12
Estratto fluido liquirizia……………………………………………….. g 1.3
Acqua cloroformica (0,25 % di cloroformio) q. b. a……. g 15
(un cucchiaio pro dose)
Pozione di cascara e di belladonna per bambini
Elisir cascara sagrada (ved. sopra)………………………….. g 0,3
Tintura belladonna g 0,15
Sciroppo zenzero . …………………………. g 0,6
Sciroppo semplice F.U. g 0,6
Acqua q. b. a ……………………………………………………………… g 4
(1-2 cucchiaini pro dose)
BIBLIOGRAFIA
(I) JOWEIT H. A. D., J.A.Ph.A., 52. 288, 1904 – (2) LE PRINCE M., Compt. rend., 129, 60, 11W9 – (3) LIDDEL R. W., KING C. G. e BEAL G. D., J.A.Ph.A., 31, 161, 1942 – (4) FAIRBAIRN J. W., e coll., J. Pharm. Pharmacol., 10, suppl., 217T, 1958 – (5) GIBSON M. R. e SCHWARTING A. E., J.A.Ph.A., 37, 206, 1948 – (6) SIPPLE H, L., KING C. G. e BEAL G. D., J.A.Ph.A., 23, 205, 1934 – (7) KUBLY M., Pharm. Zeitschr. j. Russland., 5, 160, 1866; KRASSOWSKI N., J. russ. phys.-chem, Ges., 40, 1510, 1908 – (8) SCHINDLER 0., Pharm. Acta Helv., 21, 136-196, 1946 – (9) LEE J. e BERGER L., U. S. Patent, 2, 552-896, 1951; ' Chem. Abs., 4$, 9083 g, 1951 – (IO) FAIRBAIRN J, W. e MITAL V. K., i. Pharm. Pharmacol., 9, 432, 1957; 10, 217T, 1958 – (11) BAUMGARTNER R. e LEUPIN K., Pharm. Acta Helv., 34, 296, 1959 – (12) TSCHIRCH e CRISTOFOLETTI, Schwelz. Woch. Pharm., 42, 456, 1904 – (13) PANCHAUD, Schwelz. Woch. Pharm., 43, 518, 1905 – (14) AUTERHOFF H., Arznelm-Forsch., 3, 137, 1953 – (15) GREEN M. W., KING C. G. e BEAL G. D., J.A.Ph.A., 27, 95, 1938 – (16) PEACOCK J., Amer, J. Pharm., 98, 395, 1926 – (17) MEIER H. F. e LEROY W. Y., Amer. I. Pharm., 60, 87, 1888 – (18) GOSSELIN M. C. e BAUER C. W., J.A.Ph.A., Sci. td., 43, 569, 1954 – (19) LEE I. e BERGER L., U S. Patent, 2. 552, 896, 1951 – (20) SIPPLE H., KING C. G. e BEAL G. D., J.A.Ph.A., 23, 205-208, 1934 – (21) FAIRBAIRN J. W. e MAHRAN G. L. H., /. Pharm. a. Pharmacol., J, 827, 1953 – (22) MITCHEL W. e FAIRBAIRN J, W., lbld., $, 78!1, 1953 – (23) DUNCAN A. S, – Brlt. Med. J., 439, 1957 – (24) AUTERHOFF H., Arznelm.-Forsch., 3, 137-139, 1953 – (25) HAZLETON L. W. e TALBERT K. D., J.A.Ph.A., 33, 171>-173, 1944 e 34, 260-264, 1945 – (26) LATVEN A. R., SLOAN A. B. MUNCH I., lbld:, 41, 548, 552, 1952 – (27) GREEN M W., KING C. G. e BEAL G. D., lbld., 25, 107-110. 1936 e 27, 95-100, 1938 – (28) PARIS R. e MOYSE H., Prod. Pharm., 14, 9, 462-473, 1959 – (29) VIEH^ WER A., Am. J. Pharm., 107, 47-72, 1935; J.A.Ph.A., 27, 668-671, 1938 – (30) LOEWE S., J.A.Ph.A.., 28, 427-432, 1939 – (31) HUBACHER M. e DOERNBERG S., ibld., 37, 265, 1948 e HUBACHER M., DOERN- BERG S. e HORNER A., ibld., 42, 23-30, 1953 – (32) FAIRBAIRN J. W., J. Pharm. a. Pharmacol., J, 10, 683, 1949 – (33) LOU T. C., ibld., 1, IO, 673, 1949 – (34) LOU T. C. e FAIRBAIRN J. W., lbld., 3, 5, 295, 1951 – (35) RAGGI, Atti Soc. Med. Chlr. Padova, 23, .1945 – (36) LIDDEL, KING e BEAL, I.A.Ph.A., 11, 161, 1942 – (37) TSCHIRSCH, Ber. d. Deut. Pharm. Gesell., p. 174, 1898 – (38) TSCHIRSCH e MONI- KOWSKI, Arch. d. Pharm., SO, 92, 1912 – (39) PIETSCH, Terapeutitsche Monat., 24, 35, 1910 – (40) WAI., THER, Milnch. Med. Woch., p. 1812, 1910 – (41) BECHAMP G., Progr. Med., n. 46, 1912 – (42) LINEL L., Etudc dc la Péristaltin^ Maloln Edit. Paris 1912 – (43) MASSALONGO R. ' e PIAZZA C., cFracastoro'l Gazz. Med. Veronese, 8, 1912 – (4t) KOCH C., Zentralbl, /, Gyniikologle n. 40, 1912 – (45) CHISTONI A., Arch. di Farmacol. Sper. e Sclen. Aff., 13, 17, 1914 – (46) ASTRUC A. e GIROUX J., Bull.â– Soc. Pharm. Montpellier, 1, 12-15, 1942 – (47) NELSON R. E., Proc. Amer. Pharm. Ass., SI, 313-322, ' 1904 – (48) AITCHISON J. D., Lancet, n. 7037, 75, 1958/U vol. – (49) McGUIGAN, J.A.M.A., 76, 513, 1921 • (50) BOCKUS, WILLARD e BANK, lbld., 101, 1, 1933 – (51) TYSON^J. Pedlatr., 743, 1937.

