Noce Comune
Tratto da “Piante Medicinali – Chimica, Farmacologia e Terapa” di R. Benigni, C. Capra e P.F.Cattorini
(Juglans regia L. – Fam. Juglandacee)
(Sin. – Nux Juglans Duham.). Esistono parecchie varietà (J. r. serotina Desf.) e secondo i frutti (fructu angulato, coniforme, maximo, tenero)
Non va confusa con la Juglans nigra L. (U.S.A.) e con la Juglans cinerea L. (sin. J. cathartica Michx.) (Canada, U.S.A.).
Noce Comune- Ultimo aggiornamento pagina: 27/02/2018
Indice dei contenuti
- Generalità
- Componenti principali
- Proprietà farmacologiche
- Estratti e preparati vari
- Preparazioni usuali e Formule
- Bibliografia
Generalità

Etimologia – Juglans da Jovis glans = ghianda di Giove ( Dios balanos ) (in antico, col nome Juglans si indicava il Castagno).
regia – regale.
Nomi volgari – Noxe, nuse (lig.), nosèra (piem.), nus (lomb.), nucia (abr.), nuci (sic.) ecc.
Wallnuss (ted.), the common Walnuttree (ingl.), noyer (fr.), greziaek orechi (russo), angus (armen.), karuon (grec.), souak (arab.), diófa (ungh.), hou t'ao, kiang t'ao (cinese).
Habitat – Spontanea in Armenia, nella regione a mezzodì del Caucaso e del
M. Caspio, in Persia or., nelle montagne del nord e del n/est dell'India, Birmania, Cina settentrionale e occidentale (coltivato), Thibet, Turkestan, Montagne delle Grecia (Tessaglia) e del Banato (Rumenia, Transalvania, Jugoslavia). L’habitat si estende quindi dall’Europa temperata al Giappone. Coltivato in tutta l’Europa centrale e meridionale (regione mediterranea) e nelle regioni temperate in tutto il mondo. Africa del Nord (Marocco) (Midelt) Rif, Medio – Grande e Antiatlante), Cirenaica (Derna).
In Italia ovunque nella penisola e isole, massime nei monti sino a 100 m sm.
Grande albero (12/25 m).
Parti usate – Foglie e mallo (involucro carnoso del frutto).
Componenti principali
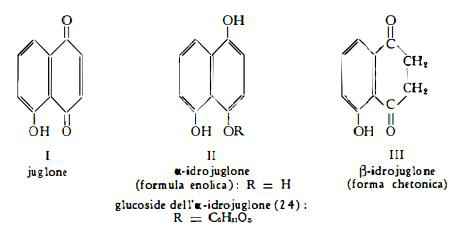
Juglone (1) (2), a- e b-idrojuglone (3), glucoside dell'a-idrojuglone (4) (5), vitamina C (6-9), tannino (10-12); nelle foglie mesoinosite (13) ed i flavonoidi 3-arabinosido-quercetina, iperina (14) e 3-arabinosido-canferolo (15).
Lo juglone, C10H6O3, estratto sin dal 1856 da Vogel e Reischauer (1) dal mallo del frutto immaturo della Juglans regia L., fu denominato nucina in un primo tempo e poi juglone dagli stessi AA., in considerazione del carattere chinonico della sostanza. E’ stato in seguito identificato da Reischauer (16) con la regianina, isolata dal mallo verde da Phipson (17). La composizione chimica dello juglone è stata stabilita in seguito agli studi, sia di Bernthsen (18), che ne ha fissato la formula grezza, C10H6O3, sia dello stesso A. che con Semper (19) ne ha definita la formula di struttura I, equivalente a quella del 5-ossi-1,4-naftochinone.
L’a- ed il b-idrojuglone, C10H8O3, furono isolati dal mallo immaturo della Juglans regia da Mylius (3), che ne ha determinato la formula centesimale, C10H8O3. Le ricerche di Bernthsen e Semper (20) (21) e di Mylius (3) sull'a-idrojuglone e di Mylius (3), di Willstatter e Wheeler (22) e di Meyer e Sander (23) sul b-idrojuglone hanno condotto alla proposta delle formule II e III rispettivamente.
Il glucoside dell’a-idrojuglone, C16H18O8, separato in forma amorfa da Daglish (4) da diverse parti della Juglans regia L., è stato poi estratto in forma pura dal mallo immaturo da Ruelius e Gauhe (5). Mentre precedentemente Daglish (4) aveva definito il glucoside come 5-b-D-glucosido-a-idrojuglone, Hayes e Thomson (24) hanno riferito che in esso il glucosio si trova in posizione 4.
La juglone è stato trovato nel mallo, nelle foglie, nei rami e nelle radici della Juglans regia L. (2). Nelle foglie fresche sarebbe presente soltanto juglone e non a-idrojuglone (25). Da 100 kg di mallo maturo essiccato sono stati estratti g 150 di juglone (19). Il glucoside dell’a-idrojuglone è stato determinato nel mallo immaturo nella quantità dello 0,13 % (5).
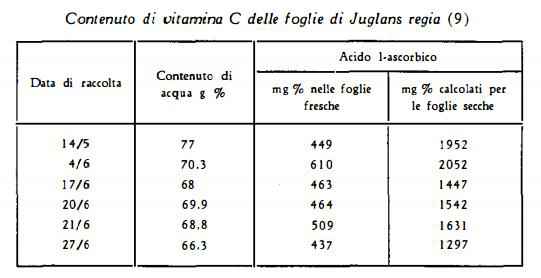
Vitamina C è risultata presente in quantità elevate sino all’1 % (6) nel mallo del frutto immaturo, mentre in minori proporzioni è stata trovata nel mallo del frutto maturo e nelle foglie (7). Durante il periodo di crescita nel mallo si è notato un contenuto di vitamina C pari a mg 800-900% (26).
Nelle foglie si è rilevata la presenza di una forte quantità percentuale di vitamina C all’inizio dell'estate; nel mesofillo ne sono stati trovati 750-850 mg %, nelle nervature mediane e nel picciolo quantità minori (8).
Nei frutti e nelle foglie il titolo di vitamina C aumenta sino alla prima metà di luglio, poi diminuisce. All'inizio del periodo vegetativo il contenuto percentuale aumenta gradualmente dalle parti più basse sino alla parte superiore della pianta; successivamente questa proporzione si inverte (27).
E’ da notarsi che con i metodi di titolazione, che si basano sul potere riducente della vitamina C, si dosano anche altre sostanze riducenti, quali
gli idrojugloni. Il contenuto di questa «pseudovitamina C», espresso in acido ascorbico, raggiungerebbe spesso anche il 30 % del titolo totale di acido ascorbico (28).
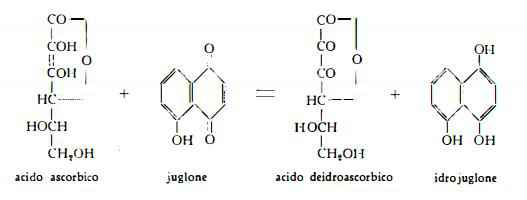
Sono state studiate le variazioni del contenuto di acido ascorbico e di juglone in varie parti del frutto e nelle parti verdi della pianta durante il ciclo vegetativo (29). Nel pericarpo l’acido ascorbico e lo juglone formano un sistema di ossido-riduzione secondo il seguente schema (6) (30):
Tannino catechico 1,5 % nel mallo fresco raccolto in settembre (10), anche 9-11 % nel pericarpo secco e nelle foglie (11), 5,9 % nelle foglie (12); nelle foglie fresche 2,64 % in giugno, 3,67 % in settembre (10).
Meso-inositolo nelle foglie della Juglans regia (13) (31) in quantità sino allo 0,3 % (32).
Nelle foglie sono stati inoltre trovati i flavonoidi 3-arabinosido-quer-cetina, iperina (14) e 3-arabinosido-canferolo (juglamina) (15) (33), carotene 0,118 % nelle foglie secche (34), nicotina (34a), 2-esen-1-ale (35), tirosinasi (36), olio etereo (con paraffina p.f. 61-62°) 0,0087% e 0,014% rispettivamente, per due campioni di differente provenienza (37); olio grasso (34); bario 0,0752% determinato come solfato (38).
Nel mallo sono stati trovati anche pentosano 5,9 % costituito principalmente da xilano (34), emulsina, perossidasi (36), zuccheri, fosfato ed ossalato di calcio, gli acidi citrico e malico (34); ceneri con 68,8 % Fe2O3 e 7,8% MnO2 (39).
Proprietà farmacologiche ed impiego terapeutico
Le foglie di Noce ebbero fama in passato, di buon rimedio nella terapia della scrofolosi, degli eczemi cronici, dell’artrite urica, delle gastroenteriti catarrali, come depurativo e in numerose altre affezioni.
Sino al secolo scorso vennero attribuite a questa droga notevoli proprietà antitubercolari ed essa era impiegata, non solo nelle linfoadeniti specifiche e nelle comuni forme di tubercolosi polmonari, ma anche nelle forme postprimarie generalizzate, quali la miliare.
Luton (40) afferma d’aver guarito tre casi di miliare col semplice estratto di foglie di Noce, affermazione che dette origine a una vivace polemica fra l’Autore e il Meslier (41) il quale si permise di insinuare che il Luton, molto probabilmente, aveva scambiato una adenopatia toracica o addominale, con una granulie.
Brissemont (42) trovò che lo juglone somministrato alla dose di g 0,10-0,30, determina un’azione purgativa intensa, accompagnata da coliche addominali e da vomito.
Reynaud (43) eseguì estese ricerche sperimentali e cliniche sull’azione ipoglicemizzante dei preparati galenici di foglie di Noci, senza peraltro raggiungere la dimostrazione definitiva dell’attività antidiabetica della droga. Egli constatò che un estratto di foglie di Noce, somministrato endovena nel coniglio, determina generalmente un effetto iperglicemico, mentre l’azione di un infuso concentrato, nelle stesse condizioni, si manifesterebbe di solito, con un effetto ipoglicemizzante. Non si può escludere che anche nelle foglie di Noce, analogamente a quanto è stato osservato sperimentando con altre droghe, possa essere contenuto, accanto ad un principio ipoglicemizzante, anche un principio iperglicemizzante, e ciò spiegherebbe come il prevalere dell'uno o dell altro nei diversi preparati, possa dar luogo ad effetti nulli o anche opposti.
Leclerc (44) avendo sperimentato con successo un infuso concentrato di foglie di Noce in un diabetico, attribuisce l’azione di questo preparato alla presenza del tannino il quale, secondo l’A., limiterebbe la saccarificazione degli amidi nell’intestino e la trasformazione del glicogeno nei tessuti.
Si dovrebbe dunque ammettere, secondo questa teoria, che tutte le droghe tanniche e il tannino stesso, siano dotate di un’azione ipoglicemizzante pressocchè analoga, ciò che però non risulta essere stato dimostrato.
D’altro lato Sendrail e coll. (45) avendo studiato l'azione dei principi vegetali che esercitano una leggera azione ipoglicemizzante e sulla formula cellulare delle isole del Langerhans, comparativamente con l’N-1-sulfanil-N-2-n-butilcarbamide, trovarono che le foglie di Noce, determinano segni di discreta ipergenesi delle cellule, correlate con la depressione glicemica, sebbene in misura inferiore a quelli prodotti dal Mirtillo (Vaccinium mirtillus) e dalla Galega.
I preparati di foglie di Noce sono impiegati come amaro-tonici e astringenti nel trattamento delle dispepsie e nelle infiammazioni catarrali del tubo gastroenterico. Nel trattamento della tubercolosi polmonare Leclerc (46) consiglia di associare alla terapia antibiotica specifica i preparati di foglie di Noce, con lo scopo soprattutto, di favorire i processi di riparazione dei tessuti lesi. Lo stesso A. ricorda che la decozione concentrata di foglie di Noce, per irrigazioni vaginali, è considerata dai ginecologi un rimedio classico nelle affezioni infiammatorie delle vie genitali (45).
I preparati di mallo sono usati in cosmetologia ed entrano nella formulazione di alcune tinture per capelli.
Estratti e preparati vari
a) Estratto fluido foglie (g 1 = XL gtt).
Dosi: g 5-10 pro die,
b) Estratto molle acquoso foglie (1 p. = 7 p. circa di droga).
Dosi: g 1-2 pro die.
c) Estratto fluido mallo (g 1 = XXXVI gtt).
Dosi: g 5-10 pro die.
d) Estratto fluido etereo mallo.
(uso esterno).
Preparazioni usuali e formule galeniche
Tintura
Estratto fluido noce foglie……………………………………………… g 20
Alcool di 20° g 80
(g 20-40 pro die).
Tintura
Estratto fluido noce mallo……………………………………………… g 20
Alcool di 20°…………………………………………………………………. g 80
(come sopra).
Sciroppo
Estratto fluido noce foglie……………………………………………… g. 5
Sciroppo semplice F.U…………………………………………………. g 95
(a cucchiai).
Sciroppo
Estratto fluido noce mallo……………………………………………… g. 5
Sciroppo semplice F.U…………………………………………………. g 95
(a cucchiai).
Olio di mallo noci (uso esterno).
Estratto fluido etereo mallo noci……………………………………. g 10
Olio vegetale………………………………………………………………… g 90
BIBLIOGRAFIA
(1) VOGEL e REISCHAUER, Buchn. Neues Magaz.. 5, 106, 1856; 7, 1, 1858 – (2) BRISSEMORET A. e COMBES R., Compì, rend.. Idi, 838, 1905 – (3) MYLIUS F., Ber., 18, 2567, 1885 – (4) DAGLISH C„ Biochem. J„ 47. 452, 458, 462, 1950; J. Pharm. PharmacoL, 4, 539, 1952 – (5) RUELIUS H. W. e GAUHE A., Lieb. Ann., 571, 69, 1951 – (6) BREINLICH J., Sudd. Apolli. Zig., 82, 195, 1942 – (7) MIRIMANOFF A. e MORI M., Schieeiz. Ap. Zig., 78, 685, 704, 1940 – (8) DAGLISH C„ Biochem. J„ 49, 639, 1951 – (9) GUENTHER E., HEEGER E. F. e ROSENTHAL C., Pharmazie, 7, 24, 1952 – (10) BOUCHERLE A.. Ann. pharm. frane., 7, 667, 1949 – (11) OLSZEWSKI Z., Acta Polon. Pharm., Il, 77, 1954 – (12) HERR- MANN K. e ENGE W., Pianta Med., 6, 98, 1958 – (13) TANRET e VILLIERS, Ber., 10, 496, 1877 – (14) HERRMANN K, Arch. Pharm., 288. 362, 1955; Chem. Abs, SI, 1392 I. 1955 – (15) TASHICHIRO NAKAOKI e NAOKATA MORITA, Yakagaku Zasshi, 78, 521, 1958; Chem. Abs., 52. 131901, 1958 – (16) REISCHAUER C„ Ber., 10, 1542, 1877 – (17) PHIPSON T. L„ Compì, rend., 69, 1372, 1869 – (18) BERNTHSEN A., Ber., 17, 1945, 1884 . (19) BERNTHSEN A. e SEMPER A., Ber., 18, 203, 1885; 19, 164, 1886; 20, 934, 1887 – (20) BERNTHSEN A. e SEMPER A., ibid., 18, 203, 1885 – (21) BERNTHSEN A. e SEMPER A., ibid., 18, 212„1885 – (22) WILLSTAETTER R. e WHEELER A. S„ Ber.. 47. 2796, 1914- (23) MEYER K. H. e SANDER A., Lieb. Ann., 420, 113, 1919 – (24) HAYES N. F. e THOMSON R. H„ J. Chem. Soc., 904, 1955 – (25) FISCHER R. e STAUDER F„ Chem. Zbl., I, 3379, 1931 – (26) DAGLISH C„ Biochem. J., 49. 639, 1951 – (27) MOLOTKOVS’KII G. K„ LOPUSHANSKII P. I. e SOLDATOVA M. A., Ukrain. Bolan. Zhur., 13, 56, 1956; Chem. Abs., 52, 17419 I. 1958 – (28) MIRIMANOFF A. e STADELMANN R„ Schneiz. Ap. Ztg., 88, 270, 1950 – (29) ZUMAN P., Chem. Lisly, 48, 524, 1954; Chem. Abs., 48, 8675e, 1954 – (30) MIRIMANOFF A. e STADELMANN R., Phyion, 2, 1, 1950 – (31) TANRET e VILLIERS, Ber., 12, 287, 1879 – (32) MAQUENNE, Compì, rend., 104, 225, 1719, 1887 – (33) GEHRMANN H. J„ ENDRES L„ COBET R. e FIEDLER U., Naturmss., 42, 181, 1955 – (34) WEHMER C., Die PSanzenstoflc, Il ed„ p. 208 – (34a) BLAIM K., Flora, 152, 171, 1962; Chem. Abs., 57, 15510, 1962 – (35) CURTIUS T. e FRANZEN K, Chem. Zbl., L 1142, 1911; Lieb. Ann., 390, 89, 1912 – (36) CHODAT e EVARD, Compì, rend. Soc. Phys. Misi. Nat. Genève, 45, 52, 1928; Boi. Zbl., 13, 147, 1928 – (37) Ber. Schtmmel. apr. 1912, 127 – (38) ARTIS e MAXWELL, Chem. News, 114, 62. 1916 –
(39) LINSTOW V., Natiirliche Aoreichenuig von Metallsalzen, Reperì. Spec. Nov. Beihefte, 31, 65, 1924 –
(40) LUTON A., Ball. Gén. de Thir., 140, 1876; cit. da LECLERC [vedere (46)1 – (41) MESLIER, cit. da LECLERC (46) – (42) BRISSEMONT A., Thèse de Méd. de Paris, 1903; cit. da LECLERC (46) – (43) REYNAUD G., Thèse de Lyon 1932; cit. da LECLERC (46) – (44) LECLERC H., Progris Méd., n. 50, 1935 – (45) SENDRAIL M-, VINCENT D-, SENDRAIL-PESQUÉ M. e MAHOUX M., IV Rèunion des Endocrinologistes de langue fran;aise, Paris 27-28 giugno 1957 (Presse Méd., 65, 1508, 1957); Semaine des H6p., p, 389, 1961 – (46) LECLERC H„ Rév. de Phytolhér., 19. 49, 1955.

