Marrubio
Tratto da “Piante Medicinali – Chimica, Farmacologia e Terapa” di R. Benigni, C. Capra e P.F.Cattorini
(Marrubium vulgare L. – Fam. Labiate/Stachioidee/Marrubiee)
(Sin. – Marrubium germanicum Schrank. – Marrubium album Black Marrubium candidum Dod.)
Marrubio- Ultimo aggiornamento pagina: 27/02/2018
Indice dei contenuti
- Generalità
- Componenti principali
- Proprietà farmacologiche
- Estratti e preparati vari
- Preparazioni usuali e Formule
- Bibliografia
Generalità

Etimologia – Marrubium, secondo Linneo, da Marruvium o Marrubium l’antica capitale dei Marsi, sulla riva orientale del Lago Fucino, oggi S. Benedetto dei Marsi (com. di Pescina), dove la pianta era abbondante nel terreno paludoso. Secondo altri Autori dall’ebraico mar = amaro e rob = succo, succo amaro. Altri dal latino marcidum = vizzo, appassito, per le foglie raggrinzite, bianchicce e come vizze (Lemery).
vulgare – volgare.
album e candidum – per le corolle bianche (bianco sporco).
Nome volgare – Marrobio, mal robbio, robbi, mentastrico, erba siderita, erba apiola (tosc.), marubiu (lig.), marubj, roumé (piem.), trifolon (lomb.), jerva riccia, marrujjo (abr.), marrubiu vranco, marruggeddu (sic.), marrubiu bianco (sard.) ecc.
Gemeiner Andorn (ted.), white horehound (ingl.), marrube blanc (fr.), marrubio bianco (spagn.), marroyo branco (port.), szanta biala (pol.), orvosi pemetefu (ungh.).
Habitat – Europa, Asia occidentale, Africa settentrionale (Tripolitania), (volg. rubia, sul litorale), Algeria, Marocco (merriyùtz, mrriouta-el-Gelb = pianta del fegato, arabo) (non el Kelb = del cane).
In Italia, comune negli incolti, nei campi arenosi, nei terreni sabbiosi e sassosi, lungo le strade, i muri, i fossi, dal mare alla zona montana: penisola ed isole.
Pianta erbacea perenne.
Parti usate – L’erba fiorita (da maggio all’autunno).
Componenti principali
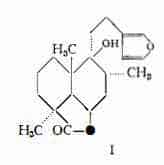
Marrubina (o marrubiina), sostanza amara che fu estratta dal Marrubium vulgare L. da Harms e Mein (1) sin dal 1855 e fu isolata in forma cristallina, poco più tardi, nel 1861 da Ludwig e Kromayer (2). La formula grezza C21H28O4, assegnatale nelle prime ricerche condotte da Gordin (3), fu poi modificata in C20H28O4 da Lawson ed Eustice (4) e da Robertson, Hollins e Richards (5). Allo studio della formula di struttura dalla marrubina si dedicarono molti AA. e particolarmente, oltre ai già citati Gordin (3), Lawson ed Eustice (4) e Robertson e coll. (5), anche Viguera Lobo (6), Ghigi e coll. (7-12a), Cocker e coll. (13) (14), Rigby e coll. (15-18), Moody (19) e Castine, Wheeler e Wheeler (19a). L’esito di questi studi ha permesso di riferire la composizione della marrubina a quella di un lattone diterpenico, che per riscaldamento con KOH alcoolica dà il sale potassico di un acido monobasico, denominato acido marrubico, facilmente trasformabile nella marrubina per disidratazione. Alla marrubina è stata attribuita da Cocker e coll. (13) (14) la formula di struttura I.
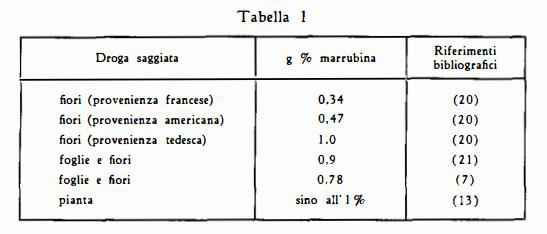
Per il contenuto di marrubina nel Marrubium vulgare dalla letteratura (7) (13) (20) (21) si sono dedotti i valori raccolti nella tabella I.
Altri componenti:
— tannino 2,6-2,9 % (22).
— materie mucillagginose e pectiche 2,7-3 % (22).
— sostanze resinose e cerose: 1) dalla frazione resinosa saponificabile è stata separata una sostanza C13H20O3 e dalla frazione insaponificabile una sterina di composizione non definita (23); 2) da una frazione cerosa sono state isolate una sostanza n-C31H64, b-sitosterolo e due composti di probabili formule C15H10O4 (O CH3)2 e C17H30O3 rispettivamente (18).
— acido ursolico nelle quantità dello 0,12% (18a).
— olio etereo 0,056 % (24).
— un glucoside non identificato 0,12%, una saponina (25) 0,18%, secondo Balansard (26), 0,80% secondo Rizzo (22).
— colina (27) 0,2% (25).
— vitamina C 33 mg % nelle foglie fresche (= mg 93% calcolati nelle foglie secche) in piante alte 40 cm., verso la fine della fioritura (28).
— alcaloidi non identificati (29).
— nitrato di potassio 2,8-3% (22).
Proprietà farmacologiche ed impiego terapeutico
Il Marrubio era noto ai sacerdoti egiziani e figurava fra le droghe usate nei sacrifici offerti ad alcune divinità. Dalla liturgia egiziana passò poi alla medicina greco-romana e, più tardi, a quella araba, come apprezzato rimedio balsamico, bechico ed espettorante, ritenuto utile in numerose affezioni dell’apparato respiratorio. Come tale venne conservato nella medicina medioevale e dell’Età moderna, epoca in cui vennero riconosciute a questa droga altre attività quali quelle antitermica modificatrice delle funzioni digestive e della funzionalità epatica [Leclerc (30)].
Le proprietà balsamiche, bechiche ed espettoranti vennero in seguito confermate clinicamente da Leclerc (31) e farmacologicamente, più tardi, da Adami (32).
Per le sue proprietà antitermiche, il Marrubio venne considerato da Wauters (33) come un buon succedaneo della chinina ed altri AA. [Thorel e Hanoune (34), Garnier e Vannier (35)] segnalarono la sua utilità nelle piressie di origine intestinale e in sostituzione della chinina nei casi di chininoresistenza e di intolleranza verso questo alcaloide.
L’attività colagoga del Marrubio venne controllata da Chabrol (36) il quale però non potè dimostrare alcun aumento della secrezione biliare. Contemporaneamente Mercier e Rizzo (37), sperimentando con i sali sodico e potassico dell’acido marrubico, trovarono che questi sali, somministrati sottocute ed endovena nei cani, determinano un aumento della secrezione biliare, ciò che fu più recentemente confermato da Krejci e Zadina (38) dai quali l’acido marrubico venne sperimentato sui ratti. Da questi AA. fu sperimentata anche la marrubina la quale però non dimostrò di essere dotata di tale azione.
La DL50 per l’acido marrubico nel ratto, è stata trovata dagli AA. pari a 115 mg/kg (valore medio), per via intraperitoneale e pari a 370 mg/kg (valore medio) per via orale. La marrubina è risultata priva di tossicità.
Pagés e Comte (39) hanno constatato che il Marrubio è dotato di una azione modificatrice del ritmo cardiaco che si manifesta in maniera più o meno rapida e completa nei casi in cui esistano alterazioni del ritmo dovute a varie cause. Tale effetto viene posto dagli AA. in relazione con una attività antitossica che il Marrubio manifesterebbe migliorando la digestione e la funzionalità epatica.
Granel (40) ritiene invece che la suddetta azione si eserciti sulla fibra cardiaca, tramite il sistema nervoso vegetativo e la Rizzo (41), che pure ha constatato un effetto favorevole del Marrubio nelle aritmie cardiache (in particolare nelle extrasistolie e nella fibrillazione), ritiene che esso non sia dovuto alla marrubina, ma alla presenza nella droga di elevate quantità di nitrato di potassio e di colina. Alla presenza di queste sostanze Mercier e Vignoli (42) hanno attribuito l’azione che il Marrubio esplica sugli apparati cardiovascolare, respiratorio e sulla motilità dell’intestino, attività simile a quella dovuta agli estratti di Hamamelis (ved. Hamamelis) nei quali la colina è contenuta in quantità comparabile a quella contenuta negli estratti di Marrubio.
Le ricerche su questa particolare attività del Marrubio vennero riprese più recentemente da Cavanna e Pirona (43) i quali sperimentarono, sulla rana, la tintura, l’estratto fluido di Marrubio e la marrubina da loro stessi isolata. Essi hanno osservato che l’estratto fluido alla dose di 6 millesimi di cc/g, determina sul cuore di rana in situ, rallentamento del ritmo e aumento della forza di contrazione.
Una dose superiore di 5 volte (3/100 di cc/g), arresta dopo 2 h il cuore in diastole. Queste azioni vengono inibite dalla somministrazione preventiva di atropina e potenziate dalla prostigmina.
L’ECG avrebbe posto in evidenza una notevole inibizione nella formazione degli stimoli (che viene intensificata dalla somministrazione preventiva di g 0,00005/g di prostigmina) e un evidente rallentamento della diffusione e della durata dell’eccitazione intraventricolare, mentre la fase di refrattarietà viene prolungata.
La tintura alcoolica agisce in maniera simile ma a dosi molto superiori; la marrubina invece, si è dimostrata inattiva.
Gli AA. concludono che l’estratto fluido e la tintura di Marrubio esplicano una vera e propria azione cardioregolatrice di tipo vagale, azione che, in accordo con le conclusioni cui giunse precedentemente la Rizzo, non sarebbe dovuta alla marrubina.
Anche più recentemente Aliev e Aliev (29), hanno studiato l’azione di estratti acquosi e alcoolici di Marrubio volgare proveniente dall’Arzebaidzhan. Essi hanno trovato che questi estratti, che si sono manifestati tossici sui topi alla dose di 2 cc di una soluzione al 10%, agiscono sul cuore isolato di rana diminuendo il numero delle pulsazioni e l’ampiezza delle contrazioni e che, inoltre, sono dotati di un’azione ipotensiva. Gli stessi risultati sono stati ottenuti dagli AA, impiegando, invece degli estratti, gli alcaloidi in essi contenuti, ai quali pertanto gli AA. attribuiscono la suddetta azione.
Concludendo quindi si può dire che i risultati delle prove cliniche e di quelle farmacologiche eseguite sul Marrubio e sui suoi derivati, hanno dimostrato che a questa droga possono essere attribuite attività amarotoniche, eupeptiche e colagoghe, balsamiche, bechiche ed espettoranti, antitermiche e modificatrici del ritmo cardiaco.
Estratti e preparati vari
Estratto fluido (g 1 = XXXVII gtt).
Dosi: g 1 pro dose 3-4 volte pro die.
Preparazioni usuali e formule galeniche
Tintura
Estratto fluido marrubio…………………………………………………….. g 20
Alcool di 25°……………………………………………………………………… g 80
(g 5 pro dose).
Sciroppo
Estratto fluido marrubio…………………………………………………….. g 5
Sciroppo semplice F.U……………………………………………………… g 95
(a cucchiai).
Pozione espettorante
Estratto fluido marrubio…………………………………………………….. g 7
Estratto fluido ipecacuana………………………………………………… g 0,3
Estratto fluido liquirizia……………………………………………………… g 8
Sciroppo balsamo tolù……………………………………………………… g 30
Acqua distillata…………………………………………………………………. g 80
(a cucchiai).
BIBLIOGRAFIA
(1) HARMS E. e MEIN, Arch. Pharm., 133, 144. 1855 – (2) LUDWIG e KROMAYER, Arch. Pharm.. 158, 257, 1861 – (3) GORDIN H. M„ J. Am. Chtm. Soc„ 30. 265, 1908 – (4) LAWSON A. e EUSTICE E.. J. Chem. Soc., 587, 1939 – (5) HOLLINS F., RICHARDS J. H. e ROBERTSON A„ Nature. 143, 609, 1939 – (6) VIGUERA LOBO, Medicamento, Ed. Farm., 3, 3, 1951 – (7) GHIGI E., Gaza. Chim. ha!., 78, 856, 1948 – (8) GHIGI E„ Gaza. Chim. Ita!., SI, 336, 1951- (9) GHIGI E.. Gaza. Chim. Ila!.. 83, 252, 1953 – (10) GHIGI E., POZZO BALBI T„ Gaza. Chim. Ita!., 84, 428, 1954 – (11) GHIGI E. e DRUSIANI A., Gaza. Chim, Ita!., 85, 187, 1372, 1955 – (11 a) GHIGI E. e POZZO BALBI T„ Atti Accad. Sci. Ist. Bologna, Sez. 11. 2, 1955 – (12) GHIGI E e DRUSIANI A.. Gaza Chim. hai.. 86. 682, 1956 – (12a) GHIGI E„ Atti Accad. Sci. Ist. Bologna, Sez. 11, 7, 1960 – (13) COCKER W„ EDWARD J. T. e HOLLEY T. F,, J. Chem. Soc., 2540, 1953; Chem. Ind.. 772, 1955; Chem. Abs.. 49. 13202d, 1955 – (14) COCKER W.. EDWARD J. T., HOLLEY T. F. e WHEELER D. M. S„ Chem, Ind., 386. 1955; Oiem. Abs., 50. 10049a, 1956 – (15) BURN D. e RIGBY W„ Chem. Ind., 386, 1955; Chem. Abs.. 50, 10049a, 1956 – (16) BURN D„ MOODY D. P. e RIGBY W., Chem. Ind., 928, 1956; Chem. Abs., 51. 4315a, 1957 – (17) HARDY D. G., RIGBY W. e MOODY D. P., J. Chem. Soc., 2955, 1957; Oiem. Abs., 52. 19591, 1958 – (18) BURN D. e RIGBY W., J. Chem. Soc., 2964, 1957; Chem. Abs., 52, 1960Ì, 1958 – (18a) BRIESKORN C. e coll., Arch. Pharm., 285, 290, 1961 – (19) MOODY D. P„ Chem. Ind., 75, 1960; Chem. Abs., 54, 9876c, 1960 – (19a) CASTINE W. H„ WHEELER D. M. S. e WHEELER M., Oiem. Ind., 1832, 1961 – (20) MAC CREA J., J.A.Ph.A., 19. 231,1930 – (21) BERNARDI A. C BRACCI A., Arch. il. sci. farm., 10, 251, 1941; Boll. chim. farm., 82, 14, 1943 – (22) RIZZO C., Thése de Pharmacie d’Aix, Marseille, 1943 – (23) BERNARDI A„ Boll, chim. farm., 90, 269 e 349, 1951 – (24) HAENSEL, Pharm. Ztg., 47, 74, 1902 – (25) MERCIER J. C MEROER F., Compì, rend., 195, 1102, 1932; Chem. Abs., 989, 1933 – (26) BALANSARD, Bull. sci. pharm., 43, 148, 1936 – (27) PARIS R. C MOYSE-MIGNON H., Ann. pharm. fran(., 14, 467, 1956 – (28) GUENTHER E„ HEEGER E. F. e ROSENTHAL C., Pharmazie, 7, 37, 1952 – (29) ALIEV R. K. e ALIEV A. M., Uchenye Zapiski Azerbaidzhan, 0.9, 69-75, 1956! Chem. abs., 52, 14761,1958- (30) LECLERC H„ Rey. de Phytothér,, 17, 134, 115, 1953 e Précis de Phytothérapie, Masson, Parigi 1935, p. 132 – (31) LECLERC H., Paris Médical, giugno 1917; Bull. sci. pharm, sett.-ott, 1918; J. des Pratìciens 1919 – (32) ADAMI E., Arch. it. sci. farm., 12, 1943 – (33) WAUTERS, cit. da LECLERC (30) – (34) THOREL c HANOUNE, cit. da LECLERC ibid. – (35) GARNIER c VANNIER, Bufi. Méd. de l’Algerie 1914, cit. da LECLERC ibid. – (36) CHABROL E., C. R. Soc. BioL, 109, 275, 1932 – (37) MERCIER F. e RIZZO C-, ibid. 114, 263, 1933 – (38) KREJCI I. e ZADINA R., Pianta Med., 7, 1, 1959 – (39) PAGÉS e COMTE, Bull. Soc. Se. Méd. Biol. de Montpellier et de Languedoc, luglio 1927, cic> da LECLERC (30) • (40) GRANEL R., Contrìbution a Tétude de marrube blanc. Son emploi dans le traitement de rarytmie extrasystolique; Tbése de Montpellier 1931 –
(41) RIZZO C., Etude Chimique-Pharmacologique sour le Marrubium vulgare; Thése de Marseille 1933 –
(42) MERCIER F. e VIGNOLI L., C. R. Soc. Biol.. 121, 668, 1936 – (43) CAVANNA D. e PIRONA M., Boll. chim. farm., 89, 267, 1950.


