Frassino
Tratto da “Piante Medicinali – Chimica, Farmacologia e Terapa” di R. Benigni, C. Capra e P.F.Cattorini
(Fraxinus excelsior L. – Fam. Oleacee/Frassinee)
Frassino- Ultimo aggiornamento pagina: 27/02/2018
Indice dei contenuti
- Generalità
- Componenti principali
- Proprietà farmacologiche
- Estratti e preparati vari
- Preparazioni usuali e Formule
- Bibliografia
Generalità

Etimologia – Fraxinus (Virgilio Egl. VII, 651) (dubbia), da frango-flecto = piegare (nel senso che i rami si piegano e si rompono facilmente) oppure «vel a fragolis locis» perchè l’albero vegeta nei luoghi selvaggi. Oppure dal greco jraxis = separazione, sepimento, da jrassw = chiudo, perchè si usava piantarlo come segnale di confine di proprietà o di campi.
excelsior, che diventa molto alto.
Nome volgare – Frassine, Noce selvatica (da non confondere con la Juglans) (Tosc.). Muddèu (Sic.). Oliastro de trumini (Sard).
Habitat – Europa, Asia occidentale. Africa mediterranea. In Italia nei boschi (continentale e insulare) dal mare alla zona montana.
Coltivato a filari nei campi e come pianta ornamentale.
Albero.
Parti usate – Foglie.
Componenti principali
Nelle foglie: mannite (= fraxinite) (1) (2), inositolo, quercitrina, destrosio, acido malico, gomma, tannino, olio etereo contenente terpeni (1), acido a-amminoadipico (3), acido ursolico (4) ed un chinone vitamina K2-simile con catena laterale isoprenoide (0,12% nelle foglie secche) (5).
La struttura chimica (1) di questo chinone, trovato nelle foglie di Frassino e di numerose altre piante, è stata stabilita e confermata da Kofler e coll. (5) per sintesi parziale a partire dal solanesolo. Per il solanesolo gli AA. hanno determinato la formula grezza C45H74O e per il chinone hanno proposto la seguente formula di struttura, equivalente a quella di un dimetil-banzochinone con una catena laterale di 9 gruppi isoprenici.
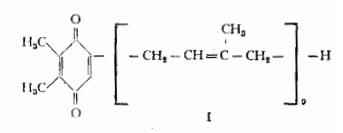
Interessante il confronto con la formula della vitamina K2 (II) che è stata rappresentata con un nucleo 2-metil-1,4-naftochinonico portatore di una catena laterale, formata da due radicali farnesilici oppure da sei gruppi isoprenici (9).
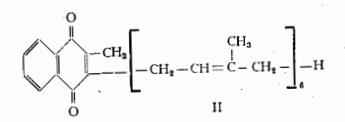
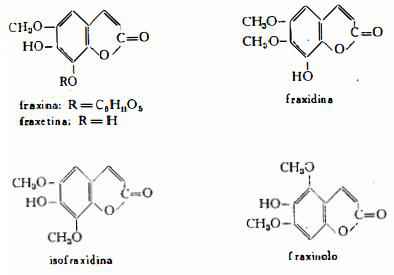
Nella corteccia del fusto sono stati trovati fraxina C16H18O10, che per idrolisi produce glucosio e fraxetina C10H8O5 (6-metossi-7,8-diossicumarina) (6) (7), fraxinolo C11H10O5 (5,7-dimetossi-6-ossicumarina), fraxidina C11H10O5 (6,7-dimetossi-8-ossicumarina), isofraxidina o calicantogenolo C11H10O5 (6,8-dimetossi-7-ossicumarina) (8).
Proprietà farmacologiche ed impiego terapeutico
Il Frassino è dotato di azione diuretica, diaforetica e lassativa ed è usato specialmente come rimedio popolare nella terapia del reumatismo e della gotta. Secondo Marbotin (10) tale impiego sarebbe giustificato dalla sua notevole attività diuretica e diaforetica.
Peyraud e Delarue (11) riferiscono di aver usato con buoni risultati, le foglie di Frassino sotto forma di the, come rimedio antireumatico e antigottoso.
Il Puget (12) trovò utile il Frassino nella terapia del reumatismo articolare acuto, caso nel quale si otterrebbe un potenziamento dell’azione di altri farmaci ad azione antireumatica.
Il Tschirch (13) riferisce che le foglie di Frassino vengono comunemente impiegate nella Svizzera francese per la loro azione diuretica, antireumatica e blandamente purgativa.
Estratti e preparati vari
Estratto fluido (g 1 = XLIIl gtt).
Dosi; g 0,3-1 pro dose due-tre volte pro die.
Preparazioni usuali e formule galeniche
Tintura
Estratto fluido frassino …. g 20
Alcool di 20°……………………. g 80
(XXX-L gtt più volte pro die)
Sciroppo
Estratto fluido frassino …. g 5
Sciroppo semplice F.U…. g 95
(a cucchiaini più volte pro die)
Pozione diuretica (uricemia, gotta, artritismo, ecc.)
Estratto fluido frassino g 30
Estratto fluido orthosiphon g 20
Estratto fluido gramigna g 20
Estratto fluido carciofo g 20
Alcool di 20° e sciroppo g 30
(mezzo cucchiaino pro dose)
BIBLIOGRAFIA
(1) GINTL e REINITZER, Monaish. Chem., 3. 74S, 1882; WEHMER C., Die PBanzenstoffe, 1931, p. 949 –
(2) PLACCOMIO E„ RIv. II. Ess. Prof., 35, 239, 1953 – (3) BERG A. M., KARI S„ ALFTHAN M. e VIRTANEN A. I., Aula Chtm. Scaiid., S, 358, 1954; Chem. Ahi.. 48, 10842 e, 1954 – (4) POURRAT H., LE MEN J. e BOUSTANY N., Aim. Pharm. Primi., 12, 59, 1954 . (5) KOFLER M„ LANGEMANN A„ RÙEG R., CHOPARD DIT.JEAN L. H„ RAYROUD A. e JSLER O., Heh. Chini. Aita, 42. 1283, 2252, 1959 – (6) SALM-HORSTMAR, Pogg. Ann. Phys. u. Chem., 97, 637, 1856; 100. 607, 1857; i07, 327, 1859 – (7) WESSELY F. e DEMMER E., Ber., 61. 1279, 1928; 62, 120, 1929 – (8) SPATH E. e JERZMANOWSKA Z., Ber., 70, 698, 1019, 1672, 1937 . (9) BINTLEY S,, MCKEE R„.THAYER S. ; DOISY E., J. Blol. Chem., 133, 721, 1940 – (10) MARBOTIN, cit. da LECLERC H. in Pr6cis de Phytothérapie, p. 49, Masson, Paris 1935 – (11) PEYRAUD e DELARUE, dt, da LECLERC H. Ibidem – (12) PUGET, cit. da LECLERC H. ibidem. – (i3) TSCHiRCH, Handb. d. Pharmakognosle,.Lipsia 1936.


