Vitamina K (Fillochinone): funzioni, carenza, fonti
La Vitamina K (Fillochinone) ha un ruolo fondamentale nell’emostasi e nella coagulazione del sangue: la sua carenza porta ad emorragie cutanee, nasali, urinarie o digestive. I più noti farmaci utilizzati nella anticoagulante-orale/”>Terapia Anticoagulante Orale (TAO), come il warfarin (Coumadin) o l’acenocumarolo (Sintrom) sono, appunto, degli inibitori della Vitamina K.
Indice dei contenuti
- Cenni storici
- Struttura chimica
- Proprietà fisico-chimiche
- Metabolismo
- Fisiologia
- Fonti, Unità, Apporti
- Carenza
- Diagnosi di carenza
- Farmacologia
- Indicazioni e Controindicazioni
- Ricerche attuali
- Conclusioni
Storia della Vitamina K
Per la prima volta nel 1929 si sospetta la presenza di un fattore antiemorragico alimentare.
H. Dam, effettuando degli studi sul colesterolo in polli alimentati con una dieta priva di lipidi, constata la presenza di versamenti emorragici in diversi organi. Considerando che l’assenza di un fattore alimentare è responsabile dei disturbi della coagulazione osservati, H. Dam lo chiama nel 1935 Koagulation vitamin o, più semplicemente, vitamina K.
Lo stesso anno, H.J. Almquist ed E.L.R. Stocks-Tad riescono a curare questi disturbi della coagulazione con estratti di erba medica.
Nel 1936, H. Dam isola una vitamina K oleosa dall’erba medica il cui nucleo attivo è un chinone.
Nel 1939, E.A. Doisy realizza la sintesi di questa vitamina detta vitamina K. Quindi ottiene, partendo da pesce avariato, un’altra sostanza con attività antiemorragica che chiama vitamina K2.
Nel 1943, H. Dam ed E.A. Doisy ricevono il Premio Nobel per la Medicina per aver scoperto rispettivamente la vitamina K, fattore di coagulazione, e la sua struttura chimica.
Benché H. Dam abbia dimostrato sin dal 1936 che l’attività della protrombina diminuisce in assenza di vitamina K, il ruolo esatto della vitamina K sarà riconosciuto solo a metà degli anni ’50 quando si scopre che la sintesi di alcuni dei fattori che permettono la trasformazione della protrombina in trombina dipende dalla vitamina K.
11 meccanismo d’azione della vitamina K sui fattori della coagulazione sarà dimostrato in seguito in diverse tappe.
In particolare nel 1974, J. Stenflo scopre uno specifico aminoacido, l’acido ?-car-bossiglutammico, responsabile della fissazione del calcio da parte della protrombina ed indispensabile all’azione della protrombina.
Nel 1975, C.T. Esmon e collaboratori mettono in evidenza che il fegato è la sede di una carbossiiazione vitamina K-dipendente.
A partire dal 1983, altre proteine carbossilate in presenza di vitamina K vengono isolate in diversi tessuti sani e patologici.
Struttura Chimica
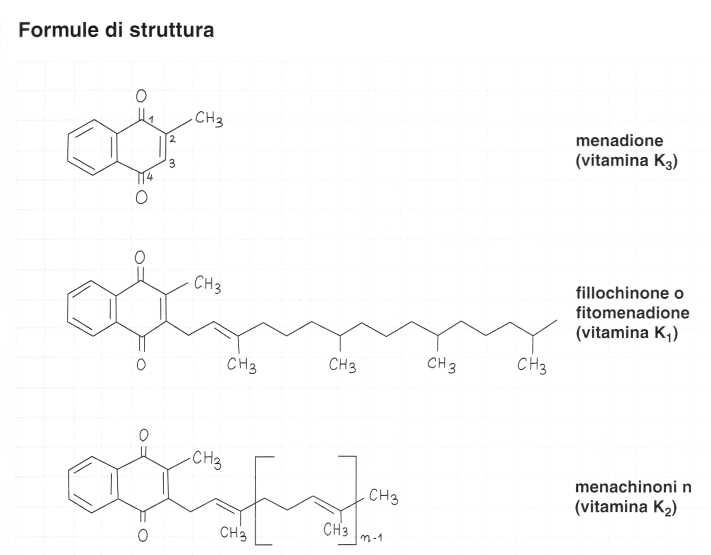
Il termine vitamina K raggruppa diverse sostanze che derivano dal nucleo 2-metil-l,4-naftochinone o menadione (vitamina K3) e che partecipano all’attivazione di certi fattori della coagulazione.
Esistono due forme naturali che differiscono per la catena laterale sita a livello del carbonio in posizione 3:
• il fillochinone o fitomenadione (vitamina K1) che possiede una catena laterale fitilica con venti atomi di carbonio con un solo doppio legame,
• i menachinoni (vitamina K2) la cui catena laterale è poli-insatura e possiede da 20 a 60 atomi di carbonio.
I menachinoni si distinguono per il numero n di gruppi isopreni (a cinque atomi di carbonio) della loro catena laterale.
Proprietà Fisico-Chimiche
Il fillochinone è un olio di colore giallo pallido.
È insolubile in acqua, poco solubile in alcol e molto solubile in etere, cloroformio, nonché nei grassi e negli olii.
Alcuni sali del menadione sono idrosolubili: menadione sodio bisolfito, sale tetrasodico del 2-metil-l,4-naftochinone.
Il fillochinone è lentamente degradato dall’ossigeno dell’aria e più rapidamente dalla luce.
È stabile al calore ma degradato dagli alcali.
Metabolismo
Esistono due fonti naturali di vitamina K: gli alimenti ed i batteri della flora intestinale.
Le verdure verdi contengono fillochinone ed i prodotti animali una miscela di fillochinone e di menachinoni.
I batteri della flora intestinale sintetizzano dei menachinoni.
II menadione non fa parte delle fonti naturali, ma è un derivato di sintesi.
Assorbimento
Il fillochinone ed i menachinoni sono assorbiti in modo diverso.
¦ Sede
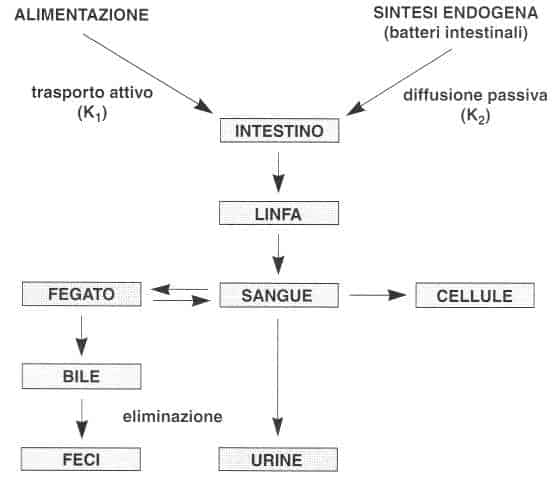
Il fillochinone è assorbito a livello dell’intestino tenue prossimale mentre i menachinoni sono sintetizzati dalla flora intestinale partendo dall’addo naftoico o dal fillochinone alimentare.
I batteri possono trasformare il fillochinone in menadione mediante degradazione della catena laterale, quindi sintetizzare i menachinoni (principalmente il menachinone 4) mediante rialchilazione.
I menachinoni sono assorbiti a livello del-Tintestino tenue e del colon. L’assorbimento richiede la formazione di micelle in presenza di bile e di succo pancreatico. La vitamina K viene quindi incorporata nei chilomicroni ed assorbita per via linfatica.
La vitamina contenuta negli alimenti è assorbita in percentuale dal 40% al 70%.
¦ Meccanismo
Il fillochinone è assorbito attraverso un meccanismo di trasporto attivo mentre i menachinoni si diffondono mediante un processo passivo.
Assorbimento della vitamina K
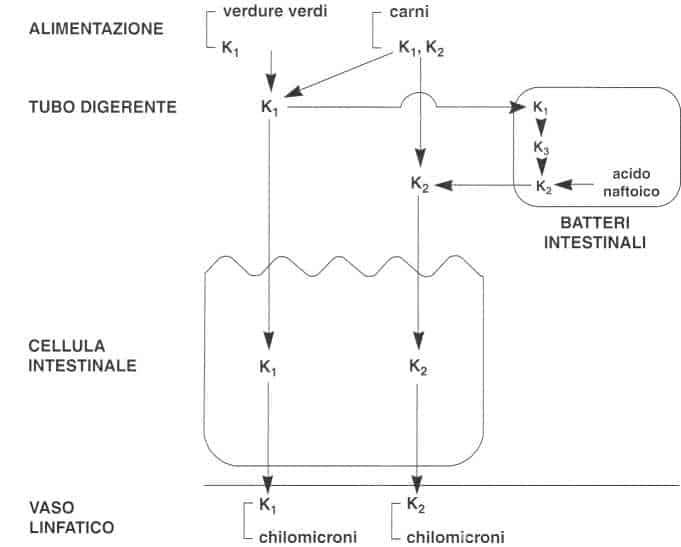
Distribuzione
La vitamina K si accumula rapidamente nel fegato, principalmente sotto forma di fillochinone e di menachinone 7 (trentacinque atomi di carbonio sulla catena laterale in C3) ma il turnover è molto rapido.
La principale forma circolante è il fillochinone il cui tasso ematico è da 0,24 ad l,f5 ng/ml. È trasportato dalle LDL e distribuito in tutti i tessuti.
Distribuzione della vitamina K
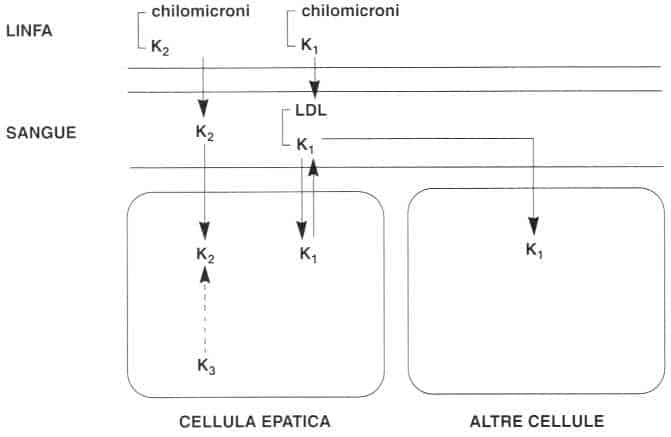
Gli organi piif ricchi sono il fegato, i surreni, i polmoni, il midollo osseo, i reni ed i gangli nervosi.
Tuttavia, il contenuto totale dell’organismo è molto basso (da 50 a 100µg) e le riserve sono sufficienti solo per otto giorni.
Studi sugli animali hanno dimostrato che, a livello della cellula epatica, il fillochinone si concentra nei microsomi e che i menachinoni possono essere sintetizzati partendo dal menadione.
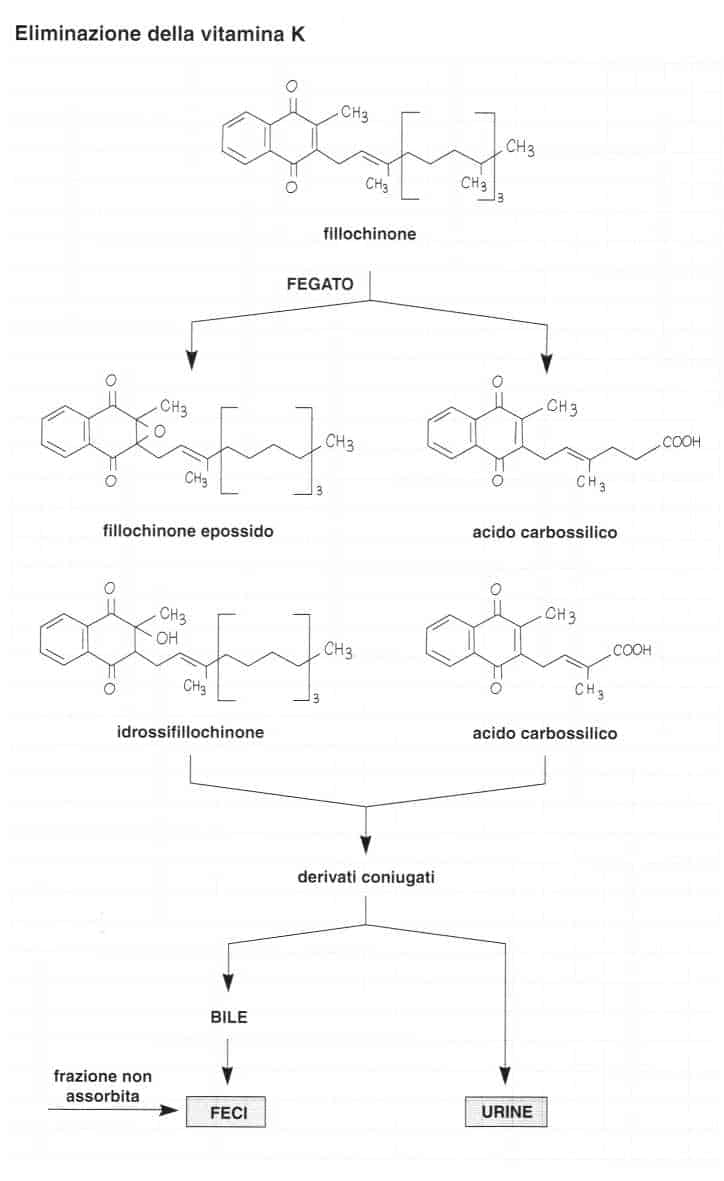
Eliminazione
La vitamina K viene eliminata nelle feci (dal 40% al 50%) e nelle urine (20%), sotto forma di metaboliti.
Il fillochinone subisce un accorciamento della catena laterale (cinque o sette atomi di carbonio) ed un’ossidazione che forma acidi carbossilici.
Questi sono coniugati all’acido glucuronico ed eliminati principalmente nella bile.
Il nucleo di naftochinone della vitamina K può anche essere ossidato dai microsomi epatici per formare un derivato epossidico o un derivato idrossilato. Anche questi composti sono degradati in metaboliti prima di essere escreti.
I menachinoni sembrano subire lo stesso catabolismo.
L’emivita della vitamina K è di circa trenta ore.
Fisiologia
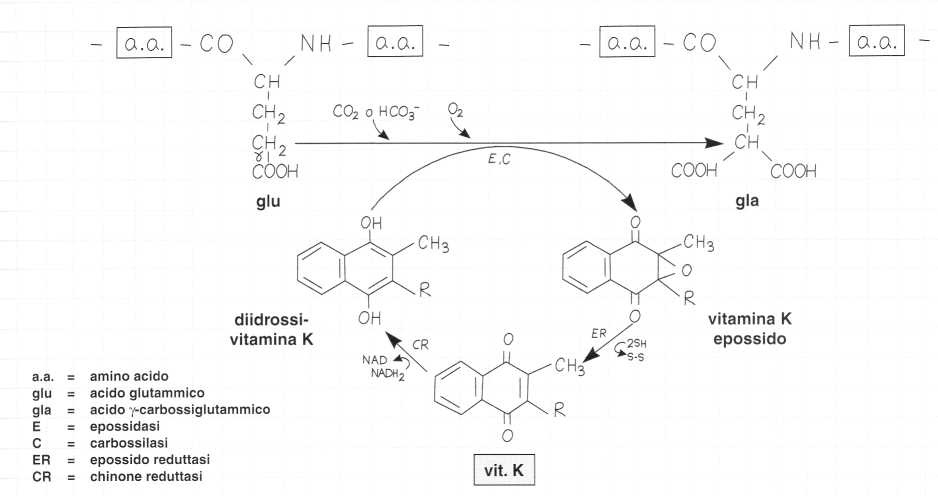
Meccanismo d’azione
La vitamina K è il cofattore di una carbossilasi microsomiale.
Questa provoca la ?-carbossilazione di residui glutammici (glu) di alcune proteine che sono quindi trasformate in acidi ?-carbossiglutammici (gla).
Meccanismo d’azione deiia vitamina K
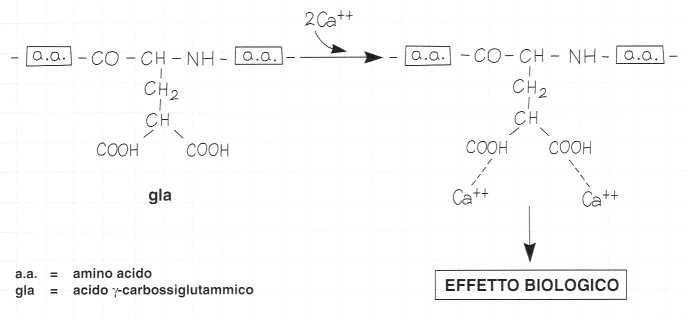
L’acido ?-carbossiglutammico è un aminoacido particolare che ha la proprietà di fissare il calcio e conferisce tale proprietà alla proteina di cui è costituente.
Fissazione dei caicio da parte delle proteine ?-carbossilate
La vitamina K subisce dapprima una riduzione catalizzata dalla chinoneredutta-si (CR):

È sotto questa forma che agisce come cofattore della carbossilasi dell’acido glutammico. Questa reazione avviene in due fasi.
• In un primo tempo, si ha formazione di un carbanione e la diidrossivitamina K viene trasformata in vitamina K epossido sotto l’azione di una epossidasi (E):
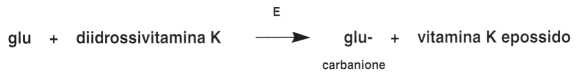
• Avviene in seguito formazione di acido ?-carbossiglutammico sotto l’azione della carbossilasi (C):
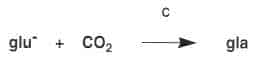
Quindi la vitamina K è rigenerata da un’epossidoreduttasi (ER):
![]()
Ruolo metabolico della vitamina K
Le carbossilasi vitamina K-dipendenti sono principalmente presenti nel fegato ma si trovano anche a livello del polmone, della milza, del rene, dell’osso, della placenta e della pelle.
Si conoscono attualmente circa dodici proteine il cui metabolismo richiede una ?-carbossilazione degli acidi glutammici. È possibile classificarle in tre gruppi.
• Le proteine trasportatrici di fosfolipidi. Questo gruppo comprende i fattori della coagulazione vitamina K-dipendenti nonché due proteine che inibiscono la coagulazione. Queste proteine sono presenti solo nel plasma.
• Le proteine trasportatrici di sali di calcio: l’osteocalcina presente nelle ossa e nel plasma, l’aterocalcina nel tessuto ateromatoso, e alcune proteine nei calcoli renali.
• Un gruppo di proteine meno ben definite che comprende la proteina Z presente nello sperma e nel plasma.
¦ I fattori della coagulazione
Quattro fattori della coagulazione sono vitamina K-dipendenti: fattore II o protrombina, il fattore VII o proconvertina, il fattore IX o antiemofilico B ed il fattore X o Stuart.
Il fattore IX è implicato nella via intrinseca la cui attivazione avviene per contatto con una superficie. Il fattore VII è implicato nella via estrinseca la cui attivazione avviene tramite fattori tissutali. I fattori X e II sono implicati nella via comune alle due vie.
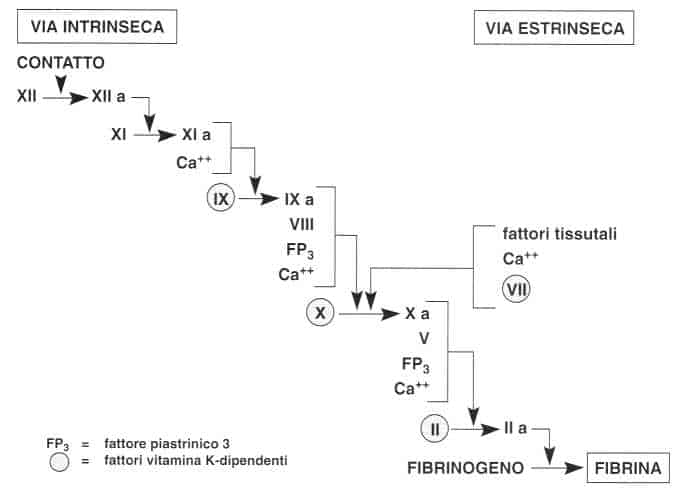
Per essere funzionanti, questi fattori devono fissare il calcio a livello degli acidi ?-carbossiglutammici (già).
I fattori attivati possono legarsi ai fosfolipidi di membrana, indispensabili alla loro attivazione.
Attivazione della protrombina
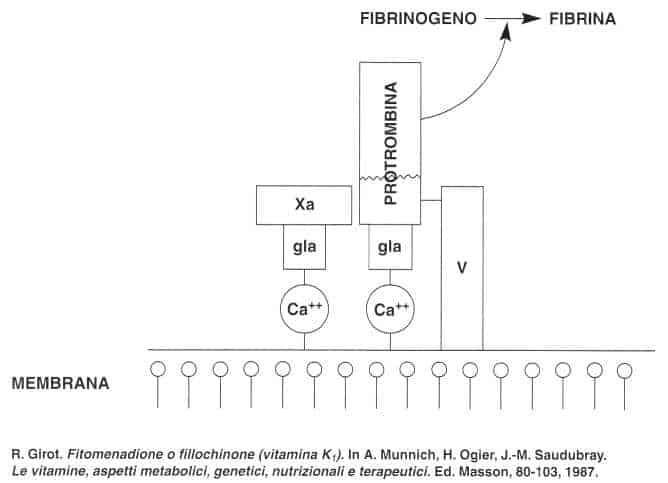
In assenza di vitamina K, vi è sintesi di fattori acarbossilati o PIVKA (Protein Induced by Vitamin K Absence or Antagonist) che sono inefficaci.
¦ Le altre proteine
Altre proteine, individuate più recentemente, presentano la stessa caratteristica di ?-carbossilazione degli acidi glutammici.
Si trovano in siti biologici molto diversi e le loro funzioni non sono sempre definite (vedere: ricerche attuali).
Fonti, Unità, Apporti, Stato
Fonti alimentari
La vitamina K è presente nella maggior parte degli alimenti in quantità variabile. Gli alimenti più ricchi sono i crauti, il cavolo (rosso, verde, di Bruxelles), il prezzemolo e gli spinaci. Vengono poi i cavolfiori, i broccoli e le insalate verdi.
La vitamina K si trova anche, ma in quantità minore, nella carne, nelle patate e nelle carote.
Altri alimenti ne contengono pochissima, in particolare le uova, la carne magra, il fegato (manzo, maiale), il prosciutto, i latticini, i cereali, i pomodori, parecchi legumi e la frutta.
| µg di vitamina K per 100 g | ||
|---|---|---|
| Crauti | 200 – 3.000 | |
| Prezzemolo | 600 – 900 | |
| Cavolo verde, rosso, Bruxelles | 200 – 600 | |
| Spinaci | 100-600 | |
| Cavolfiori, broccoli | 60 – 300 | |
| Insalate | 80 – 200 | |
| Carne, fegato | 20-150 | |
| Patate | 20-80 | |
| Uova | 20-50 | |
| Fagiolini | 10-50 Frutta 5 – 20 |
In recenti studi la ripartizione degli apporti di vitamina K tra le diverse fonti alimentari non è descritta.
Nell’alimentazione corrente, la carne e le verdure rappresentano le fonti principali. La vitamina K è sensibile alla luce, agli ossidanti ed agli ambienti basici, ma a causa delle difficoltà di dosaggio, non è ben nota la sua stabilità nelle preparazioni culinarie.
Unità
Le diverse forme della vitamina K hanno un’attività biologica similare, che viene espressa in microgrammi (µg) di vitamina Kj.
Apporto consigliato
In Francia, la commissione degli Apporti Nutrizionali Consigliati (ANC) del Centro Nazionale di Coordinamento degli Studi e Ricerche sulla Nutrizione e l’Alimentazione (CNERNA) ha proposto per la prima volta nel 1992, degli ANC di 10-45µg di vitamina K al giorno, secondo le fasce d’età.
| )ig/giorno | |
|---|---|
| Lattanti | 10 |
| Bambini da 1 a 3 anni | 15 |
| Bambini da 4 a 9 anni | 25 |
| Bambini da 10 a 12 anni | 30 |
| Adoiescenti e donne aduite | 35 |
| Uomini aduiti | 45 |
| Gravidanza | 45 |
| Allattamento | 55 |
Stato nutrizionale
Gli studi epidemiologici di carattere nutrizionale non prendono in considerazione la vitamina K. Non esistono quindi dati precisi relativi al livello degli apporti alimentari e al livello ematico di vitamina K dei gruppi di popolazione.
• Gli apporti alimentari bastano largamente a soddisfare il fabbisogno; un pasto normale può fornire da 300 a 400µg di vitamina.K.
• Le carenze sono eccezionali e non sono di origine alimentare ma molto spesso legate ad un difetto di assorbimento.
Carenza
Clinica
La carenza di vitamina K si manifesta con segni ematologici. Sul piano clinico, si hanno emorragie cutanee, nasali, urinarie o digestive (ematemesi, melena) che non costituiscono un segno specifico. Quando sono abbondanti, possono provocare anemia.
Nel corso della malattia emorragica neonatale si possono osservare emorragie digestive che compaiono classicamente nel secondo o terzo giorno di vita. Più raramente e più tardivamente possono sopravvenire emorragie cerebrali di prognosi infausta (mortalità 27%, postumi neurologici 47%).
Fisiopatologia – Epidemiologia
La carenza di vitamina K può risultare da due fattori principali:
• diminuzione dell’assunzione alimentare e della sintesi endogena,
• diminuzione dell’assorbimento.
¦ Paesi in via di sviluppo
Nei paesi in via di sviluppo, la carenza di vitamina K non riveste particolare importanza. Alcune parassitosi intestinali, in particolare la ascaridiosi, possono provocare malassorbimento e partecipare all’insorgere di una carenza.
¦ Paesi industrializzati
Nei paesi industrializzati, le manifestazioni cliniche carenziali sono rare nell’adulto, a causa della vasta distribuzione alimentare della vitamina K e dell’esistenza della sintesi batterica intestinale. Casi di carenza di apporto possono tuttavia essere osservati in alcune situazioni (malassorbimento, nutrizione parenterale non integrata,…).
Le carenze erano più frequenti nel neonato prima che fosse istituita la supple-mentazione sistematica.
• Le patologie digestive croniche
Le patologie che comportano un malassorbimento cronico costituiscono un rischio di carenza di apporto.
La patologia intestinale: malattia celiaca, sprue, malattia di Crohn, colite ulcerosa, diarree croniche, estese resezioni intestinali.
La patologia epatica e pancreatica: atresia delle vie biliari, pancreatite cronica (la bile ed il succo pancreatico sono necessari all’assorbimento).
La mucoviscidosi.
• La nutrizione parenterale non integrata
La nutrizione parenterale non integrata induce una carenza totale di apporto che può essere solo temporaneamente compensata in quanto le riserve epatiche sono modeste.
• Le terapie antibiotiche prolungate
La terapia antibiotica prolungata può ridurre la sintesi endogena per distruzione della flora intestinale. Non costituisce un rischio di carenza da sola ma è un fattore aggravante per qualsiasi situazione a rischio, particolarmente in caso di apporti alimentari insufficienti.
• Le interazioni farmacologiche
Alcuni farmaci interferiscono con l’assorbimento o il metabolismo della vitamina K (vedere: farmacologia).
• Le malattie genetiche
I deficit genetici combinati di fattori dell’emostasi vitamina K-dipendenti sono eccezionali. Si tratta di una mutazione del sistema enzimatico carbossilasi/epossidasi a trasmissione autosomica recessiva.
II quadro clinico comporta una sindrome emorragica, un deficit dei fattori vitamina K-dipendenti, la presenza di precursori acarbossilati nel plasma e l’assenza di deficit di vitamina K. Il trattamento con vitamina K è inefficace.
• Il neonato
La malattia emorragica del neonato è dovuta a due fattori principali: l’immaturità epatica (responsabile di un difetto di sintesi dei fattori della coagulazione) e la carenza di vitamina K.
• Questa carenza può avere tre elementi scatenanti.
– Il trasporto placentare della vitamina K è scarso: il tasso piasmatico del neonato è circa il 50% quello della madre. Inoltre, la capacità di deposito epatico è limitata.
– L’intestino tenue è sterile alla nascita e non avviene quindi una sintesi endogena.
– Il latte materno è povero di vitamina K, il che spiega come il rischio di questa malattia sia più elevato nei bambini allattati al seno.
Circa il 60% dei neonati non supplementati alla nascita ha tassi elevati di protrombina inattiva.
In uno studio condotto in Giappone sui neonati allattati al seno, lo 0,59% (1/1.700) è risultato carente di vitamina K e l’81% di questi presenta emorragie intracerebrali.
• Si osservano tre forme cliniche di malattia emorragica del neonato.
– La forma classica sopravviene dal secondo al terzo giorno di vita e si manifesta con un’emorragia digestiva. Se non viene istituito il trattamento, può sopravvenire improvvisamente un’emorragia cerebrale nella seconda o nella terza settimana.
– La forma precoce compare nelle prime ventiquaffro ore di vita e sopravviene tipicamente quando la madre ha preso un farmaco che interferisce con la vitamina K (antivitamina K, anticonvulsivante). Si tratta molto spesso di una forma grave che associa emorragie digestive, ombelicali, cutanee, cerebrali, toraciche, addominali.
– La forma tardiva compare tra il primo ed il dodicesimo mese e questi bambini presentano un’emorragia cerebrale improvvisa di prognosi infausta.
• Il prematuro
È soggetto ad un rischio di carenza più elevato del neonato a termine.
• Gli stati di carenza marginale
Un’ipoprotrombinemia che risponde alla somministrazione di vitamina K è stata osservata in persone anziane ospedalizzate.
Questa constatazione si correla bene con l’osservazione della grande sensibilità delle persone anziane al trattamento con farmaci antivitamina K.
Diagnosi di Carenza
Per la diagnosi di carenza di vitamina K si fa abitualmente ricorso ad un esame funzionale della coagulazione. È anche possibile un dosaggio diretto della vitamina K.
Esami funzionali
• Si usa abitualmente il tempo di Quick (o tempo di protrombina) che esplora la via estrinseca della coagulazione (fattori VII, X, V, II e fibrinogeno).
Questo valore è espresso in percentuale rispetto ad una retta di standardizzazione (diluizione di un plasma di controllo). Il valore normale è superiore o uguale a 70%. Quando il valore è inferiore al 20%, il rischio emorragico è rilevante.
• Lo studio può essere completato mediante i dosaggi separati del fattore II, dei fattori VII -I- X e del fattore V, il che consente di differenziare la carenza di vitamina K dall’insufficienza epatica, a fronte ad un tempo di Quick prolungato.
Diagnosi differenziaie

In caso di deficit di vitamina K, il primo fattore a diminuire è il VII (vale a dire quello che ha l’emivita più breve). È seguito nell’ordine, dai fattori IX, X e IL • Un altro test funzionale più recentemente messo a punto consiste nel dosare i prodotti accumulati a monte della reazione bloccata dalla carenza vitaminica: le PIVKA (Protein Induced by Vitamin K Absence or Antagonist) che sono i precursori non carbossilati dei fattori della coagulazione.
Il dosaggio immunochimico della PIVKA II (protrombina acarbossilata) è mille volte più sensibile del tempo di Quick, ma non è usato abitualmente.
Dosaggi diretti
Il fillochinone ed i menachinoni possono essere dosati nel plasma ma questi dosaggi non sono di uso corrente.
Il tasso piasmatico normale di fillochinone è da 0,24 a 1,15 ng/mi.
Diagnosi eziologica
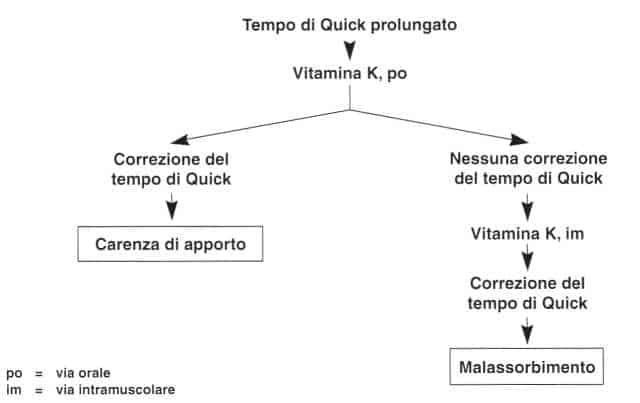
Si può disfinguere una carenza di vifamina K per difetfo di apporlo o per malas-sorbimento, misurando il tempo di Quick prima e dopo la somministrazione di 20-50 mg di vitamina K (test di Koller).
La carenza è di apporto in caso di correzione del tempo di Quick mediante la somministrazione orale.
In caso di fallimento della via orale e di efficacia della via parenterale, si tratta di un difetto di assorbimento.
Diagnosi eziologica della carenza di vitamina K
Farmacologia
Proprietà farmacologiche
Le proprietà biochimiche della vitamina K ai quantitativi nutrizionali sono ben definite, mentre non le si riconosce un’attività farmacologica specifica a dosaggi terapeutici.
Interazioni farmacologiche ed alimentari
Alcuni gruppi di farmaci interferiscono con la vitamina K: antivitamine K, cefalosporine, altre vitamine liposolubili, anticonvulsivanti, salicilati, ferro.
• Le antivitamine K (AVK)
I derivati della cumarina e dell’indandione
Per questi prodotti, si tratta evidentemente di un effetto farmacologico ricercato che è alla base del loro utilizzo.
Agiscono inibendo l’epossidoreduttasi (ER), il che provoca l’accumulo di vitamina K epossidata.
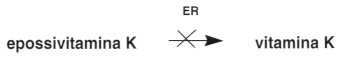
Tale accumulo impedisce la rigenerazione della forma coenzimatica attiva: la di-idrossivitamina K. Il warfarin (derivato cumarinico) è la più attiva delle antivitamine K.
Le interazioni alimentari
Durante un trattamento con antivitamine K, si consiglia cii limitare il consumo di alimenti molto ricchi di vitamina K. In pratica, è importante soprattutto evitare variazioni importanti degli apporti alimentari, particolarmente nei giorni che precedono i controlli biologici.
Classificazione dei più comuni alimenti secondo il loro contenuto in vitamina K (µg/l00 g)
| Latticini | Contenuto alto > 150 | Contenuto medio 50-100 | Contenuto basso <50 latte, formaggi, yogurt, burro |
|---|---|---|---|
| Altri prodotti di origine animale | carne, fegato (vitello) |
carne magra, fegato (manzo, maiale), uova, pesce | |
| Verdure | cavoli, cavolfiori, broccoli, spinaci, prezzemolo, insalate | carote, patate |
fagiolini, cetrioli, pomodori, piselli, asparagi, funghi,… |
| Frutta | mele, arance, fragole, pesche, banane,… | ||
| Cereali | grano, mais |
• Le cefalosporine di II e III generazione (CIIG e CIIIG): cefamandolo, cefoperazone, latamoxef.
Sono stati osservati casi di ipoprotrombinemia durante la somministrazione di questi antibiotici e questo non sembra dovuto unicamente alla distruzione della flora intestinale. Alcune CIIG e CIIIG provocano anche un’inibizione della carbossilasi (C) dell’acido glutammico (glu);
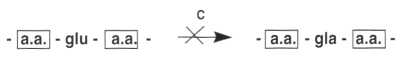
e. in grado minore, dell’epossidoreduttasi (ER). (Effetto cumarino-simile).
• Le vitamine A ed E
L’ipervitaminosi A cronica può provocare un’ipoprotrombinemia.
Analogamente, i problemi di coagulazione dei soggetti carenti di vitamina K possono essere esacerbati dalla somministrazione di dosi elevate di vitamina E.
Gli anticonvulsivanti: fenobarbitale e difenilidantoina
La somministrazione di questi prodotti nella donna gravida è stata ritenuta responsabile della malattia emorragica del neonato, a comparsa precoce (prime 24 ore di vita). Il meccanismo in causa non è stato stabilito.
• Gli altri farmaci: i salicilati, il ferro
I salicilati ad elevato dosaggio (> 6 g/giorno) e l’intossicazione da ferro possono provocare una ipoprotrombinemia di genesi ignota.
Incidenti e complicanze
• Il fillochinone (vitamina K1) è poco tossico. Sono stati descritti rari effetti secondari in caso di somministrazione parenteraie.
L’iniezione endovenosa rapida può provocare vampate di calore e dolore toracico con dispnea. Queste reazioni sarebbero dovute agli emulsionanti.
In caso di iniezioni intramuscolari di un dosaggio elevato della forma oleosa, può comparire una reazione locale (rash) da quattro a sedici giorni dopo (talvolta più tardi) e persistere sino a due mesi. In pazienti con insufficienza epatica sono stati descritti dei casi di sclerodermia localizzata.
Le reazioni allergiche sono eccezionali.
• Il menadione (vitamina K3) è più tossico.
La somministrazione di dosi elevate nel neonato è stata ritenuta responsabile di anemia emolitica con possibile complicanza di iperbilirubinemia e ittero nucleare. Queste complicanze sono più frequenti nei soggetti con deficit di G5PD o di glutatione-perossidasi.
In caso di somministrazione di dosi superiori al fabbisogno, la concentrazione dei fattori della coagulazione non può aumentare al di sopra della norma. Non esiste quindi un sovradosaggio che possa indurre un rischio di trombosi.
Indicazioni e Controindicazioni
Indicazioni
¦ Trattamento terapeutico
• L’ipovitaminosi K moderata può essere trattata con una dose unica per via orale.
– Adulti: da 10 a 20 mg.
– Bambini: da 5 a 10 mg.
La via intramuscolare deve essere evitata a causa del rischio di ematoma.
• In caso di emorragia dichiarata, si può utilizzare l’iniezione endovenosa lenta (massimo 1 mg/min) associata ai fattori II, VII, X e IX.
¦ Trattamento preventivo
La prevenzione si basa su un’alimentazione equilibrata che soddisfa facilmente il fabbisogno. Tuttavia, in alcune particolari situazioni, è giustificato un trattamento preventivo.
• Il neonato
La prevenzione del rischio di emorragia neonatale deve essere sistematica. La prevenzione diventa addirittura imperativa se esiste un fattore di rischio particolare: trattamento interferente con la vitamina K somministrato durante la gravidanza (AVK, antibiotico, anticonvulsivante), prematuri, lattanti nutriti esclusiva-mente al seno.
Il neonato senza fattori di rischio: vitamina Kj
– per via orale: da 1 a 2 mg al giorno per tre giorni o 5 mg in tre assunzioni, alla nascita, il giorno dopo e otto giorni dopo;
– per via intramuscolare: I mg alla nascita.
Il neonato di madre che ha ricevuto un trattamento interferente con la vitamina K, la dose deve essere aumentata o ripetuta.
Alcuni autori hanno proposto un’alternativa supplementando la madre (20 mg/giorno per via orale) negli ultimi quindici giorni di gravidanza.
• Il prematuro
II suo fabbisogno di vitamina K è piii elevato di quello del neonato a termine. Si valuta tra 5 e 20µg per 100 kcal per 24 ore.
• Il lattante
Lattante nutrito esclusivamente ai seno, vitamina K1 da 2 a 5 mg/settimana per \da orale. Tuttavia coloro che praticano una somministrazione per via intramuscolare alla nascita raccomandano piuttosto una seconda dose per via intramuscolare a tre mesi (da 0,5 a 2 mg) in caso di proseguimento del solo allattamento. Alcuni autori hanno anche proposto di integrare la madre in modo da arricchire il latte di vitamina K.
L’integrazione alimentare: gli alimenti per lattanti sono integrati con vitamina K.
• Malassorbimento cronico
In caso di malassorbimento cronico (atresia delle vie biliari, mucoviscidosi, intestino tenue corto, …) è giustificata la prevenzione. Saranno somministrate dosi parenterali regolarmente in funzione dei valori di emostasi.
• La nutrizione parenterale
È necessaria la prevenzione della carenza, vitamina K1 2µg/kg/giorno per via endovenosa, nell’adulto.
• La prevenzione preoperatoria delle complicanze emorragiche
La somministrazione di vitamina K1, il giorno prima dell’intervento, è raccomandabile nei pazienti a rischio.
Controindicazioni
L’uso della vitamina K, a dose terapeutica, per via endovenosa, è controindicato se non in casi di urgenza.
I derivati sintetici (vitamina K3) sono controindicati nel neonato ed in caso di deficit di G6PD o di glutatione perossidasi.
Ricerche attuali
Recenti ricerche hanno messo in evidenza diverse proteine il cui metabolismo richiede una ?-carbossilazione, simile a quella per i fattori II, VII, IX e X della coagulazione. Questi dati hanno indotto a studiare il ruolo della vitamina K sul metabolismo di queste proteine.
Vitamina K e ?-carbossilazione delle proteine
Sono state isolate delle proteine ?-carbossilate a livello dei loro acidi glutammici in diversi tessuti sani (sangue, sperma, osso, rene) o patologici (placca ateromatosa, calcoli renali). Queste proteine devono fissare il calcio a livello dell’ acido ?-carbossiglutammico (già) per essere funzionali.
Le proteine piasmatiche
• Le proteine C ed S
Queste due proteine hanno proprietà anticoagulanti ed agiscono in modo sinergico.
– La proteina C è attivata dal fattore IIa (trombina) e provoca una disattivazione dei fattori Va e VIIIa nonché una stimolazione della fibrinolisi. I soggetti carenti di proteina C hanno un maggior rischio di trombosi.
– La proteina S è presente nel plasma in forma libera e legata alla proteina di trasporto della frazione C4b del complemento. Essa stimola l’inattivazione del fattore Va da parte della proteina C e potrebbe svolgere un ruolo anche nel sistema del complemento.
• Le proteine M e Z
Queste due proteine sono presenti nel plasma ma la proteina Z è stata trovata anche nello sperma. Le loro proprietà fisiologiche non sono ben note.
La proteina Z possiede una forte affinità per i fosfolipidi e per la trombina. Potrebbe localizzare la trombina a livello della sede della lesione.
• Le otto proteine piasmatiche vitamina K-dipendenti (fattore II, VII, IX e X, proteine C, S, M e Z) presentano delle somiglianze strutturali a livello dei quaranta aminoacidi della loro estremità N-terminale. È sempre a questo livello che si trovano i residui dell’acido ?-carbossiglutammico.
Caratteristiche deiie proteine piasmatiche vitamina K-dipendenti
| II | VII | IX | X | C | S | M | Z | |
|---|---|---|---|---|---|---|---|---|
| Tasso plasmatico (µg/ml) | 100 | 1 | 3 | 20 | 10 | 1 | <1 | <1 |
| Peso molecolare (K dalton) | 72 | 46 | 55 | 55 | 57 | 69 | 50 | 55 |
| Numero di catene polipeptidiche | 1 | 1 | 1 | 2 | 2 | 1 | 1 | 1 |
| Numero di residui acido ?-carbossiglutammico | 10 | 10 | 12 | 12 | 11 | 10 | ? | 13 |
¦ La proteina ossea: osteocalcina
L’osteocalcina è una proteina sintetizzata dagli osteoblasti a livello delle regioni ossee a rapida crescita.
La sua sintesi è stimolata dall’ 1,25(OH)2D3 (vitamina D) e svolge un ruolo nella regolazione della mineralizzazione ossea.
Non ha la somiglianza strutturale delle altre proteine piasmatiche vitamina K-dipendenti.
È anche presente nel sangue ed i tassi pila elevati si trovano nell’adolescente ed in alcune patologie ossee (malattia di Paget, metastasi, osteodistrofia renale, iper-paratiroidismo).
Caratteristiche dell’osteocalcina

¦ La proteina renale
È stata isolata una proteina contenente dei residui di acido ?-carbossiglutammico a livello del rene. La sua sintesi è inibita dal paratormone e dalla vitamina D. Potrebbe avere un ruolo nella regolazione del calcio.
• Le proteine dei tessuti patologici calcificati
• L’aterocalcina
L’aterocalcina è stata scoperta nel tessuto calcificato ateromatoso.
Una ?-glutamilcarbossilasi è stata isolata dalle pareti arteriose mentre non è stata trovata a livello delle vene.
• La proteina dei calcoli renali
Una proteina ?-carbossilata è stata isolata anche in alcuni calcoli renali. 11 ruolo di queste proteine nella patogenesi di queste affezioni non è noto.
Vitamina K e metabolismo del calcio
Il ruolo della vitamina K nel metabolismo di alcune proteine che fissano i sali di calcio ha portato a studiare le influenze dello stato vitaminico sulla mineralizzazione ossea.
La prima constatazione è stata l’esistenza di malformazioni ossee (condrodispla-sia) nei neonati la cui madre aveva ricevuto delle AVK durante il primo trimestre di gravidanza.
Uno studio ha dimostrato che gli apporti alimentari di vitamina K sono correlati positivamente alla densità ossea.
Sono stati effettuati degli studi di integrazione con vitamina K (1 mg/giorno) nelle donne, prima, durante e dopo la menopausa. Questi studi hanno dimostrato una riduzione dell’escrezione di calcio nelle urine.
Attualmente sono in corso altri studi ma queste constatazioni pongono sin da ora il problema delle eventuali conseguenze dei trattamenti a lungo termine con le AVK nonché del valore degli apporti quotidiani consigliati che tengono conto soltanto della prevenzione delle complicanze emorragiche.
Conclusioni
La vitamina K ha un ruolo nella coagulazione ma anche in altri fenomeni biologici che implicano la fissazione del calcio.
Le manifestazioni emorragiche carenziali sono divenute eccezionali nel neonato dopo la somministrazione sistematica di vitamina K alla nascita.
Viceversa, sussiste un rischio in alcune particolari situazioni: malassorbimento cronico, nutrizione parenterale non integrata, bambini nutriti esclusivamente al seno.
Uno stato nutrizionale carente che non provoca alterazioni cliniche o biochimiche della coagulazione può ripercuotersi sul metabolismo del calcio.
Questa constatazione potrebbe portare a riconsiderare l’attuale nozione di apporti quotidiani consigliati nonché le conseguenze dei trattamenti a lungo termine con antivitamine K.
Indice delle monografie sulle Vitamine:
- Le Vitamine: generalità
- Vitamina A o Retinolo (beta-carotene)
- Vitamina B1 o Tiamina
- Vitamina B2 o Riboflavina
- Vitamina B5 (Acido Pantotenico)
- Vitamina B6 (Piridossina)
- Vitamina B8 o Vitamina B7 o Vitamina H (Biotina)
- Vitamina B9 (Acido Folico)
- Vitamina B12 (Cobalamina)
- Vitamina C (Acido Ascorbico)
- Vitamina D (Colecalciferolo)
- Vitamina E (Tocoferolo)
- Vitamina PP o Vitamina B3 (Niacina)

