Galega
Tratto da “Piante Medicinali – Chimica, Farmacologia e Terapa” di R. Benigni, C. Capra e P.F.Cattorini
(Galega officinalis L.- Fam. Leguminose/Galegee)
Galega- Ultimo aggiornamento pagina: 27/02/2018
Indice dei contenuti
- Generalità
- Componenti principali
- Proprietà farmacologiche
- Estratti e preparati vari
- Preparazioni usuali e Formule
- Bibliografia
Generalità

Etimologia – Galega, dal greco gala = latte e agw = io apporto, cioè che accresce la secrezione lattea.
officinalis, delle officine (farmaceutiche) .
Nome volgare – Avanese, Capraggine (Tosc.), Lavanese (Lomb.), Ruta capraria (Sic.).
Habitat – Europa centrale e meridionale, Asia occidentale. Comune in Italia nei luoghi umidi (fossi, fiumi, ecc.).
Pianta erbacea.
Parti usate – Tutta la pianta.
Componenti principali
L'alcaloide galegina C6H13N3, isolato da Tanret (1) dai semi della G. officinalis e considerato dallo stesso A. come una metilpirrolidina; Barger e White (2) e poi Spath (3) l'hanno identificato alla isoamilenguanidina; Spath (3) ne ha fissata la formula di struttura:
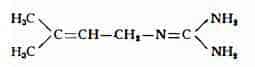
Contenuto di galegina: nella pianta seccata 0,065 % (4), nei semi freschi 0,6-0,65% (5), nei semi secchi 0,1-0,15% secondo Ferrari (5), meno di 0,1 % dopo un anno di magazzinaggio, secondo Markovic e Dittertovà (4).
La pianta contiene inoltre acido ascorbico (nelle foglie seccate g 0,491-1,028 %) (6), arginina, guanidina (7), acido pipecolico (8), nelle ceneri sono stati trovati ferro, rame e zinco (9).
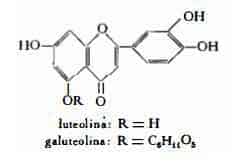
Nei semi, oltre a galegina, galuteolina, C21H20O11.3H2O, glicoside flavonico scindibile per idrolisi in glucosio e luteolina, C15H10O6 ( 5-7-3-4'-tetraossiflavone) (10); luteolina in forma libera (10), saccarosio, stachiosio (11), olio grasso 3,89% (12), saponine (13) (14).
Proprietà farmacologiche ed impiego terapeutico
La Galega era annoverata fra le piante commestibili e come tale veniva usata in alcune regioni d'Italia e specialmente in Lombardia. Sembra che tale uso derivi dai supposti vantaggi che si sarebbero ottenuti con l'impiego di questa pianta durante la terribile epidemia di peste che infierì in Lombardia nel 1576, impiego di cui si trova qualche accenno nelle opere di Fournier (15), di Hoefer (16), di Cassone (17) e di altri.
Il Selecki (18) al contrario, descrive casi di intossicazione verificatisi in pecore nutrite con Galega la quale provocò in esse, sintomi di tosse, lacrimazione, difficoltà respiratoria e morte per asfissia. Occorre ricordare a questo proposito che, secondo Leclerc (19) , la Galega diverrebbe tossica durante la fioritura e la fruttificazione per cui è soltanto la droga raccolta prima della fioritura che potrebbe essere eventualmente impiegata senza danno, nell'alimentazione.
L'azione galattagoga di questa pianta sarebbe stata scoperta alla fine del secolo scorso da Gillet-Damitte (21) il quale sperimentando la droga nelle mucche, concluse che essa possiede un valore nutritivo superiore del 33 % a quello del fieno di prato e che contiene tutti gli elementi atti a migliorare la secrezione lattea. Tale azione venne in seguito confermata da Carron de la Carrière (22) che sperimentò la droga nelle nutrici, ma venne poi negata da altri.
Lewis e Carlson (23), che sperimentarono su cani e su capre, giunsero alla conclusione che la Galega non ha alcuna azione sulla secrezione lattea e, secondo Vignes (24), la sua azione sarebbe incostante e legata, come quella di altre leguminose, al contenuto in azoto.
Più recentemente l'azione galattagoga della Galega venne negata anche dal Selecki (18) il quale dimostrò che, sia l’estratto della droga che il solfato di galegina, non esplicano alcuna azione in questo senso e nessuna influenza sull'attività estrogena, neppure dopo lungo trattamento.
Lo stesso Selecki (18) prima e in collaborazione col Rosival (25) successivamente, dimostrò che il solfato di galegina inibisce, in vivo, la coagulazione del sangue. Questo effetto sarebbe direttamente proporzionale alla dose: 10 mg/kg per via parenterale, nel cane, prolunga leggermente il tempo di protrombina (del 15-20 %) e il tempo di ricalcificazione (del 40 %). Somministrato per os il solfato di galegina resta senza effetto.
Sulla peristalsi intestinale questa sostanza avrebbe dimostrato un'attività inibitrice e un'azione miolitica nell'epilessia. A dosi elevate provoca la morte per paralisi respiratoria.
L’azione ipoglicemizzante della Galega e della galegina fu estesamente studiata sia sperimentalmente sugli animali che clinicamente sull'uomo, ma con risultati diversi o comunque incostanti, sia per ciò che si riferisce all'azione ipoglicemizzante, sia per ciò che concerne la tossicità. Questa discordanza di risultati e di opinioni che, come abbiamo già visto, esiste anche a proposito dell'azione galattagoga, può essere dovuta, almeno per quanto riguarda la droga, a diversi fattori. Il fatto che la Galega manifesti una diversa tossicità a seconda che la si raccolga prima o durante e dopo la fioritura, può far logicamente pensare ad una non indifferente variabilità nella sua composizione chimica. In secondo luogo potrebbe anche darsi che la galegina non rappresenti l'unico principio attivo contenuto nella droga, ma è verosimile che ne esistano altri il cui rapporto vari a seconda dell'epoca di raccolta. Occorre inoltre considerare che analogamente a quanto avviene negli animali, nei quali accanto ad un principio ipoglicemizzante, l'insulina, ne esiste un altro iperglicemizzante, il glucagone, anche nelle piante in cui è contenuto un principio ipoglicemizzante, non raramente ne è contenuto un altro ad azione contraria che dal primo non sempre riesce facile separare.
Nel caso della Galega quindi, oltre ad approfondire Io studio della sua composizione chimica, al fine di accertare l'esistenza o meno, di altri principi attivi ad azione ipoglicemizzante, sarebbe anche opportuno studiare la composizione chimica e l'attività farmacologica della pianta nei suoi diversi periodi vegetativi.
Per quanto riguarda l'azione ipoglicemizzante della galegina, questa venne indagata da diversi ricercatori fra i quali però non sembra esistere, come abbiamo già detto, un completo accordo e ciò può essere forse dovuto alle diverse condizioni sperimentali in cui essa è stata studiata.
Simmonet e Tanret (26) che studiarono l'azione ipoglicemizzante del solfato di galegina sul coniglio e sul cane, trovarono che questa sostanza somministrata alla dose di 75 mg/Kg, provoca nel coniglio una notevole riduzione della glicemia (50-60%) e crisi ipoglicemiche simili a quelle che si ottengono con dosi opportune d'insulina. L'effetto sembra essere indipendente dalla via di somministrazione e può manifestarsi precocemente dopo 1h, oppure più tardivamente dopo 4h.
Nel cane invece il solfato di galegina sembra essere più tossico e i risultati più incostanti. Con dosi di 4 mg/Kg è possibile ottenere una certa azione ipoglicemizzante che può giungere fino al 20% ma non rara è la comparsa di fenomeni tossici collaterali che si manifestano con vomito e diarrea mucoematica, come pure frequenti sono i casi di assuefazione a questa sostanza. Tanto nel coniglio quanto nel cane poi, la galegina avrebbe agito, in alcuni casi, aumentando la glicemia anziché diminuendola, fatto questo che, secondo gli AA., potrebbe essere dovuto ad un regime dietetico prevalentemente alcalino o ad abbondanti riserve di glicogeno epatico.
I risultati delle ricerche di Muller e Reinwein (27) confermarono soltanto in parte quelli ottenuti dai precedenti AA. Essi infatti non riuscirono a dimostrare un’azione ipoglicemizzante nel coniglio, nel quale piccole dosi di solfato di galegina (2-6 mg/Kg) si dimostrarono assolutamente inattive. Dosi medie (12-30 mg/Kg) determinarono intensa iperglicemia, fenomeni tossici e, non raramente, la morte dell’animale.
Nel cane invece i risultati furono più costanti. La dose di 4 mg/kg anche secondo questi AA. risulterebbe, per lo più, ipoglicemizzante, mentre le dosi elevate (25-45 mg/Kg) sarebbero risultate iperglicemizzanti e tossiche. Risultati favorevoli sarebbero stati ottenuti anche in due cani pancreasectomizzati, nei quali il solfato di galegina avrebbe determinato una certa diminuzione della glicemia e della glicosuria.
Gli AA. spiegano l’azione ipoglicemizzante della galegina con un effetto eccitante del pancreas endocrino, attraverso il parasimpatico e l'azione iperglicemizzante con un’eccitazione del simpatico, ciò che sarebbe provato oltre che dai risultati di ricerche farmacologiche sull'occhio enucleato di rana, sulla pressione arteriosa, sull’intestino isolato e sul preparato di rana secondo Trendelenburg, anche dall’effetto antagonizzante dell’adrenalina sull’iperglicemia da galegina.
Questa infatti, somministrata al cane o al coniglio dopo ergotamina, determina forte ipoglicemia (fino allo 0,29%) con crampi e morte dell'animale. Nell’uomo normale la galegina alla dose di 2-4 mg/Kg determina, secondo Simmonet e Tanret, Muller e Reinwein, una netta riduzione della glicemia che inizia dopo 3-4h e raggiunge il suo massimo dopo circa 9h. L’iperglicemia da carico è pure sensibilmente influenzata dalla galegina ma si è osservato che questa, anche nell'uomo può dar luogo ad assuefazione e che non è esente da azioni secondarie le quali a volte si manifestano con disturbi dispeptici, con nausea, con vomito ecc.
Sul diabetico invece, secondo il Reinwein (28), l'azione sarebbe più evidente. Questo A. ha potuto infatti dimostrare che, in molti casi è possibile ottenere una sicura azione terapeutica che si manifesta anche sulla tollerabilità degli idrati di carbonio. Con la dose di 25 mg di solfato di galegina, ripetuta più volte al giorno, fino a raggiungere complessivamente i 2 mg/Kg, è possibile secondo l’A. sostituire 20-30 U. d'insulina, senza che si manifestino azioni secondarie dovute ad eccitazione simpatica o a disturbi dispeptici. Non sembra tuttavia che i risultati siano sempre così favorevoli.
Rathery e Levina (29) constatarono in alcuni casi un peggioramento della glicosuria e dell’acetonuria, peggioramento che a volte si manifestava anche dopo un miglioramento iniziale.
Questi AA. consigliano pertanto una certa prudenza nell'impiego di questa sostanza.
Eliassow (30) osservò invece una buona, seppure debole azione della galegina nella terapia del diabete insipido.
Stirnadel (31) raccomanda come coadiuvante nella terapia del diabete, il thè preparato coi semi e con la pianta di Galega, la quale secondo l’A. agirebbe come ipoglicemizzante, non solo per il suo contenuto di galegina ma anche per la presenza di saponina e di sostanze tanniche nella sua composizione.
Parturier e Hugonot (32) sperimentarono l'azione ipoglicemizzante di un estratto fluido di Galega contenente il 3% di galegina, in 7 casi di diabete semplice o acidosico, con risultati discreti ma transitori. Gli AA. somministrarono l'estratto alla dose di LXXX-C gocce in due volte nella giornata, alternando 8 giorni di somministrazione con un ugual periodo di riposo. Essi notarono che, alle dosi impiegate, la Galega non ha le controindicazioni della sintalina, che è priva di azioni collaterali nocive e che, più che la glicemia e la glicosuria, essa influenza favorevolmente la chetonuria. La Galega secondo questi AA. può essere impiegata utilmente nel diabete leggero, nel diabete insulinoresistente e, associata con l'insulina, come medicamento di risparmio atto a facilitare l'utilizzazione dei glucidi e ad attivare il metabolismo dei grassi e dei lipidi.
Più recentemente il Golder (33) ha sperimentato l'azione della Galega somministrata sotto forma di thè, in 26 diabetici e pur avendo notato una riduzione della glicemia (15-25%) e della glicosuria in 1/5 dei malati trattati, non sembra favorevole ad un vasto impiego di questa droga nella terapia del diabete. Secondo Peplau e Seel (34) invece, l’azione terapeutica della Galega non sarebbe così debole in quanto, nei casi leggeri di diabete, sarebbe possibile riportare la glicemia al valore normale ed eliminare la glicosuria con la sola somministrazione di un infuso della droga preparato con due cucchiai da thè colmi, in 200-250 g di acqua e ripetendo la somministrazione per 4 volte al giorno. La sperimentazione sugli animali dimostrò agli AA. che l’estratto di Galega è privo di tossicità.
Evidentemente l'azione della Galega può manifestarsi in maniera diversa anche a seconda delle diverse forme di diabete nelle quali essa viene impiegata e, per quanto riguarda il suo meccanismo d’azione, l’Erspamer (35) lo ritiene molto simile a quello già noto per i preparati guanidinici sintetici, ma con il vantaggio di una migliore tollerabilità. La costituzione chimica della galegina e i risultati delle ricerche sino ad ora eseguite, dimostrano infatti l'innegabile esistenza di un’analogia chimico-farmacologica fra la galegina e i preparati guanidinici.
Interessanti e approfondite ricerche sul meccanismo col quale la galegina manifesta la sua azione ipoglicemizzante, sono state eseguite più recentemente dal Siliprandi (36), il quale ha studiato l’azione di questa sostanza sulla glicemia di vari animali (cane, coniglio, ratto) normali e diabetici. Egli ha notato che, mentre nel cane e nel coniglio normali, la galegina non manifesta alcun effetto ipoglicemizzante, nel coniglio diabetico e nel ratto sia normale che diabetico, essa esplica un’azione ipoglicemizzante a volte cospicua.
L'abbassamento glicemico determinato dalla galegina negli animali diabetici è costantemente accompagnato da un innalzamento del Q.R. e, nei ratti diabetici, da un lieve ma significativo aumento del glicogeno epatico, il che dimostrerebbe secondo l’A., che la galegina determina nell'animale diabetico, un aumento dell’utilizzazione centrale e soprattutto periferica dei glucidi e che agirebbe quindi secondo un meccanismo insulinosimile.
Questa interpretazione tuttavia andrebbe accettata secondo l’A., con qualche riserva poiché, come egli stesso ha potuto notare nel corso delle sue ricerche, la dose utile di 20 mg/Kg nei ratti, è risultata molto vicina alla dose tossica (40-50 mg/Kg), per cui egli crede di non poter escludere che già alla dose adottata nei suoi esperimenti, la galegina possa manifestare una certa azione tossica che va tenuta presente nell’interpretazione critica dei risultati.
In considerazione di ciò l’A. ritiene che la galegina anche se dotata di azione insulinosimile, difficilmente potrà essere impiegata terapeuticamente, a meno che, apportando opportune modificazioni alla sua molecola, non si riesca a diminuire la sua tossicità lasciando inalterata l’azione ipoglicemizzante.
L’A. trova inoltre che l’azione della galegina nella glicemia si svolge in maniera diversa a seconda della specie animale e che il ratto è l’animale che meglio si presta per studiare l’azione ipoglicemizzante di questa sostanza.
Citeremo infine le più recenti ricerche di Sendrail e coll. (37) i quali avendo studiato l'azione sulla, formula cellulare, delle isole pancreatiche, di alcuni principi vegetali ad azione ipoglicemizzante, comparativamente con quella della N-1-sulfaniI-N-2-n-butilcarbamide, hanno trovato che la Galega provoca una sensibile ipergenesi delle cellule b, correlative alla depressione glicemica.
Riassumendo brevemente possiamo concludere che l’azione galattagoga della Galega è negata dalla maggior parte degli AA. che la studiarono. Tuttavia, un’azione favorevole sulla secrezione lattea, dovuta forse ad un miglioramento delle condizioni circolatorie e quindi del trofismo della ghiandola mammaria, anziché ad un’azione specifica, potrebbe non essere completamente esclusa.
Per quanto riguarda invece l’azione ipoglicemizzante della galegina si può affermare che questa realmente esiste, anche se il fatto di essere stata studiata in condizioni sperimentali diverse, ha condotto gli AA. a conclusioni piuttosto discordanti.
Sembra accertato che la galegina agisca come ipoglicemizzante con un meccanismo insulinosimile e che possa agire favorevolmente in alcuni casi di diabete leggero, sia isolatamente che in associazione all’insulina come farmaco di risparmio.
Un più vasto impiego di questa sostanza nella terapia del diabete sembra ostacolato dal suo coefficiente terapeutico non troppo elevato, anche se superiore a quello di altri derivati guanidinici.
Estratti e preparati vari
a) Estratto fluido (1 = XXXVII gtt).
Dosi: ½-1 cucchiaino pro dose, quattro volte pro die.
b) Estratto molle acquoso (1 p. = 5 p. circa di droga).
Dosi: g 0,3 pro dose quattro volte pro die.
c) Estratto secco acquoso (1 p. = 8 p. circa di droga).
Dosi: g 0,2 pro dose quattro volte pro die.
Preparazioni usuali e formule galeniche
Tintura
Estratto fluido galega g 20
Alcool di 20° ……………………………………………………………… g 80
(a cucchiai)
Sciroppo
Estratto fluido galega……………………………………………… g 20
Sciroppo semplice F.U………………………………………. g 80
(a cucchiai)
Elisir galattagogo
Estratto fluido galega………………………………………….. g 40
Alcool di 60°……………………………….. . . ………………. g 160
Sciroppo arancio……………………………………………………. g 500
Acqua finocchio…………………………………………………………. g 100
Vino Marsala…………………………………………………………….. g 200
(un bicchierino dopo i pasti)
Pillole galattagoghe
Estratto molle acquoso galega…………………………… g 0,3
Sciroppo di altea ed eccipiente q. b. per 1 pillola
(4-10 pillole pro die)
BIBLIOGRAFIA
(1) TANRET. Compì, «iwd.. MS, 1182, 1426, 1914 – (2) BARGER e WHITE, Blochcm. J-, 17, 827, 1923 – (3) SPATH, Ber., 57, 474, 1924; JS, 2273, 1925 – (4) MARKOVIC O. e DITFERTOVA’ V„ Chem. ZvestI, 9, 576, 1955; Chem., Abs., 50. 8137 d, 1956 – (5) FERRARI G„ Il Farmaco, 5, 544, 1950 – (6) GtÌNTHER e coll., Pharmaiie, 7, 32, 1952 – (7) MOURGUE M. e DOKHAN R„ Compì. Read., Ut. 1434, 1954; Chem., Abs., 49, 5588 d, 1955 • (8) KOLOUSEK Chem. listy, 47. 473, 1953; Chem. Abs., 48, 3633 (, 1954 – (9) PLETICHA R,, Fharmazie, I2. 131, 1957; Chem. Abs., 51, 17616 a, 1957 – (IO) BARGER e WHITE, Blochem. J-, 17. 836, 1923 – (11) TANRET, Compt. Rend., 155, 1526, 1912 – (12) GRIMME, Chem. Rev. Feti. u. Harz – Ind., 18. 77, 1911 – (13) GRESHOFF, Kew Bull., 397, 1909 – (14) ROBERG, Arch. Fharm., 275, 84, 1937 – (15) FOURNIER, Plantes Médìclnales de France, voi. II, p. 208, Lechevalier edlt., Paris 1948 â– (16) HOEFER, Dlcllonalre de Botanlque, p, 307, Dldol Frires edit„ Paris 1850 . (17) CASSONE, Flora medlco-Farmaceullca, voi. Il, p, 95; G. Cassone edlt., Torino 1847 – (18) SELECKI F. V„ Dtsch. Ap. Zig., 96, 5, 90, 1956; Farmacia, 24, 198, 1955 • (19) LECLERC H,, cil: da DECAUX in Rev. de Phylolhér., 18, 146, 165-168, 1954 – (20) KLEIN e SCHLOGL, cit. da MADAUS in Hand, d. Blologlschen Hellmittel II, p. 1406, G. Thleme, Leipzig 1938 – (21) GILLET-DAMITTE, cit. da DECAUX ibid. – (22) CARRON DE LA CARRIÈRE, Bull, et mém. Soc. Méd. prat. de Paris 1891; cit. da DECAUX, ibid. – (23) LEWIS e CARLSON, J.A.M.A., 68, 1570, 1917 – (24) VIGNES H., Rev. de Phytolhér., numeri 46- 47, 1943, cit. da DECAUX 1. c. – (25) SELECKI F. V. e ROSIVAL V„ Biologia 11. 480-485. 1956; Chem. Abs., 53071, 1957 – (26) SIMMONET H. e TANRET O., C. R. Acad. Sci., 189, 1600, 1927; Bull. Soc. Chìm. Blol.. 10, 796, 1928; cit. da ERSPAMER V. in Droghe e principi ipogllcemizzanti vegetali. Quaderni di Fitoterapia, n. 5, p. 23-26, Inverni ft Della BeRa, edlt. Milano, 1943 – (27) MULLER e REINWEIN, Arch. exp. Path. u. Pharmakol., 125, 212, 1927 – (28) REINWEIN H., MUnch. Med. Woch., n. 42, 1794, 1927, cit. da ERSPAMER, ibidem. – (29) RATHERY e LEVINA, Bull. Soc. Chim. Blol., 10, 743, I92ls (Discussione sulla comunicaz. di Slmmonet e Tanret) eli. da ERSPARMER. ibidem. – (30) ELIASSOW, ,4rWi. / Verdauungs- krankh., 42, n. 4, 1928 (cit. da MADAUS 1. c. (20) – (31) STIRNADEL M„ Ther. d. Gegemv., 75, 565, 1934; (eli. da ERSPARMER, Ibidem.) – (32) PARTURIER G. e HUGONOT G„ Presse Méd., 1. 258. 1935 (cit. da ERSPAMER, ibidem.) – (33) GOLDER W„ Dtsch. Med. IFoch., 20, 804, 1939 e HIppokrates, 11, 287. 1940 (cit. da ERSPAMER, ibidem.) – (34) PEPLAU G. e SEEL H., HIppokrates n. 29, 757, 1941 – (35) ERSPAMER V., 1. c. (25) – (36) SILIPRANDI N., Il Farmaco, 5, 5, 536-543, 1950 – (37) SENDRAIL M.. VINCENT D., SENDRAIL-PESQUE M. e MAHOUX M., Presse Méd., 65, 67, 1508, 1957.

