Olivo
Tratto da “Piante Medicinali – Chimica, Farmacologia e Terapa” di R. Benigni, C. Capra e P.F.Cattorini
La specie Olea europaea L. comprende gli Olivi selvatici (ogliastri o oleastri) – Olea europaea a oleaster L. (sin. – Olea silvestris Mill.) e gli Olivi coltivati (che si distinguono in olivastri, olivi mezzani e olivi frantoiani – Olivi domestici) – Olea europaea b sativa (DC.) Hoffmg. et Lk.
L’Olivo selvatico ha i rami spinosi. Gli olivi frantoiani sono le piante che forniscono i frutti più grossi, dai quali si ricava l'olio.
Le varietà di Olea sono circa 300: quelle coltivate in Italia superano le 200.
Olea europaea a oleaster L. – Fam. Oleacee/Oleoidee.
Olea europaea b sativa (DC.) Hoffgm. et Lk.
Olivo- Ultimo aggiornamento pagina: 27/02/2018
Indice dei contenuti
- Generalità
- Componenti principali
- Proprietà farmacologiche
- Estratti e preparati vari
- Preparazioni usuali e Formule
- Bibliografia
Generalità

Etimologia – Olea, dal greco elaia da elaion = olio, cioè: che dà l'olio.
europaea – dell’Europa.
oleaster – dal greco elaios = agrielaia = olivo selvaggio.
olivastro – dal greco elaioeidhs = elaiwdes = olivastro.
Nomi volgari – Ulivo, olivastro (tosc.), uivo, ueive (lig.), pognoris (selvatico, Mentone), ramoliva (piem.), olivo (lomb.), liva (abr.), auliva (nap.), termite, agriddu (selvatico) (pugl.), olivaru, agghiasstru (selvatico) (calab.), auliva, aulivastru (selvatico) (sic.), olia, ollastru (selvatico) (sard.).
Oliver (fr.), olive tree (ingl.), Olivebaum (ted.), zeytoune (arab.), zebbùg (selvatico) (arab.), zeitun, zag et ter = sterco di uccello, per i piccoli frutti (selvatico) (Libia), oliveira (olivastro), oliveira brava (ogliastro) (port.), olivo, aceituno (spagn.), olìvkovoie dièrevo (russo).
Habitat – L’Olivo selvatico è originario dall’Oriente (Siria, Palestina, Belucistan). Alligna nella regione mediterranea [Mezzodì della Francia, Algeria, Marocco (Atlante)], Madera, Canarie.
Coltivato in tutta l’Europa meridionale, Egitto, Libia e altre regioni dell’Africa sett., America centrale, U.S.A. (California), America nel sud. In Italia gli Ogliastri o Oleastri si trovano in Sicilia, Calabria, Puglia. Le specie coltivate: Olivastri, in Sicilia, Calabria, Puglia, Liguria, Toscana – Mezzani, in Sicilia, Calabria, Puglia, Liguria, Toscana – Frantoiani, Toscana, Puglia, Basilciata, Calabria, Sicilia, Sardegna.
Arbusti o alberi (2-10 m.).
Parti usate – Le foglie.
Componenti principali
Sostanza amara, già studiata da diversi ricercatori (1-6) ed esaminata più recentemente da Shasha e Leibowitz (7a) (7b.) e da Panizzi, Scarpati e Oriente (8) (9). Già Cruess e Alsberg (4) avevano rilevato la natura b-glucosidica del principio amaro denominato oleuropeina e la presenza in esso di ossidrili orto-difenolici. Panizzi, Scarpati e Oriente (9) hanno poi confermato la natura b-glucosidica della oleuropeina. Essi, per idrolisi con b-glucosidasi, ne hanno prodotto la scissione con liberazione di glucosio e dell’aglucone di carattere o-difenolico e per idrolisi acida hanno ottenuto una molecola di glucosio e, in luogo dell’aglucone, due nuove sostanze, identificate con l’alcool b(3,4-diossifenil)etilico, C8H10O3, e con un acido C11H14O6 rispettivamente. Secondo Panizzi, Scarpati e Oriente (9), l’oleuropeina ha la formula centesimale C25H32O13 e la formula di struttura I.
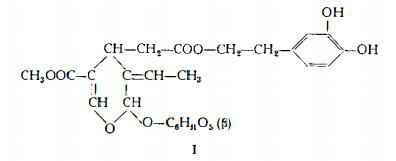
L’oleuropeina è stata estratta dalle foglie fresche in quantità pari all’1,5-2%, secondo i saggi recenti di Panizzi, Scarpati e Oriente (9). Bourquelot e Ventilesco (1) e Jardon (5) ne avevano separate quantità minori: 0,75% e 0,1% rispettivamente.
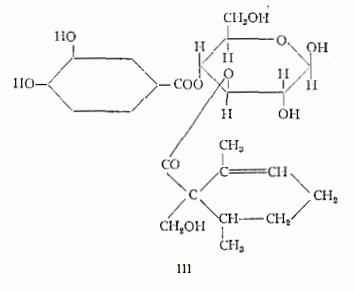
Shasha e Leibowitz (7a) (7b) hanno denominato oleuropeina un estere doppio del glucosio con l’acido protocatechico e con un nuovo acido, acido oleuropeico, C10H16O3, a cui essi hanno assegnato la struttura (ll) di acido 1-ossimetil-2,6-dimetilcicloes-2-encarbonico-1. Per l’estere oleuropeina gli stessi AA. (7b) hanno proposto la formula grezza C23H30O11 e lo schema strutturale III. Successivamente Mechoulam, Danieli e Mazur (7c) hanno determinato per l’acido oleuropeico, C10H16O3, la struttura Ila, confermata mediante confronto con il prodotto sintetico:

L'oleuropeina di Shasha e Leibowitz (7b) si può estrarre dalle olive verdi, raccolte durante i mesi estivi e dalle foglie, dai fusti e dalle radici dell’Olivo durante tutto l’anno. E’ stata ricavata dagli stessi AA. (7b) dalla polpa verde del frutto nella quantità dello 0,6 % del materiale essiccato e con resa del 6 % dalla corteccia delle radici.
Altri componenti:
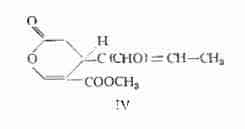
— un lattone insaturo, elenolide, C11H12O5 è stato ottenuto mediante distillazione sotto vuoto dei componenti acidi, presenti in estratti di foglie dell’Olivo (14). Questo lattone per azione dell’acqua fornisce un acido, C11H14O6, (14), che Panizzi, Scarpati ed Oriente (9) hanno identificato con un prodotto di degradazione della oleuropeina e precisamente con l’acido, avente la stessa formula grezza, C11H14O6, da essi stessi ricavato dall’idrolisi dell’oleuropeina. All’elenolide Beyerman, van Dijck, Levisalles, Melera e Veer (14a) hanno assegnato la formula strutturale IV:
— n-pentatriacontano (10).
— acido oleanolico, C30H48O6, l'alcool triterpenico (V) così denominato da Power e Tutin (2), che l’estrassero dalle foglie dell'Olea europea. E’ stato isolato da numerose altre piante e gli sono state assegnate perciò parecchie altre denominazioni — cariofillina, taraligenina, araligenina, guagenina, momorgenina — in relazione al nome della pianta da cui è stato estratto.
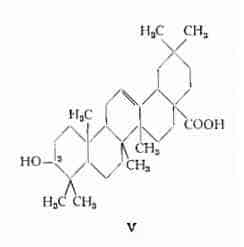
Dalle foglie essiccate dell’Olivo è stato estratto ca. il 2 %, sino al 3 % di acido oleanolico (11).
— oleasterolo, C20H34O, oleastranolo, C25H42O21, e omo-oleastranolo, C27H46O2 (2). L'esistenza delle due prime sostanze non è stata confermata da studi più recenti. E’ probabilmente da identificarsi con l'omo-oleastranolo, una sostanza neutra, ottenuta recentemente dall’estratto di foglie di Olivo, cui sembra sia da attribuirsi struttura triterpenica (11a).
— un chinone vitamina — K2 — simile con catena laterale isoprenoide. (0,02% nelle foghe secche), avente la formula di struttura VI, equivalente a quella di un dimetilbenzochinone con una catena laterale di 9 gruppi isoprenici (12) (13).
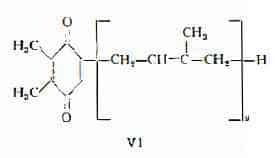
— acidi malico, tartarico, glicolico, lattico (15) e due acidi di formula C14H28O4 e C15H30O4 rispettivamente (16).
— glucosidi di struttura chimica non definita: oleoside (6), steroleoside, C32H50O11, (17); saponosidi presenti secondo Jardon (5), assenti secondo Daniel-Brunet e Oliviero (17).
— enzimi: lipasi, perossidasi (5), emulsina (1).
— colina, trovata da Samuelsson (18), assente nelle foglie fresche, secondo Panizzi, Scarpati e Oriente (9).
— altri componenti vari: tannino pirogallico (5) (17), glucosio, saccarosio (5), mannitolo (2) (5) (17), olio etereo (2), sostanze antiossidanti di natura chimica non identificata, presenti negli estratti eterei delle foglie ( 19).
La ricerca del lignano fillirina, già trovato in altre Oleacee (ved. Chionanthus virginica), ha dato risultati negativi per la presenza di questa sostanza nelle foglie di Olivo (19a).
Proprietà farmacologiche ed impiego terapeutico
L’Olivo come pianta medicinale, era noto a tutti i popoli del bacino del Mediterraneo dai quali fu in ogni tempo estesamente coltivato come pianta oleifera.
Gli Egiziani, gli Ebrei, gli Arabi, i Greci e i Romani, attribuivano molte proprietà terapeutiche all’Olivo che, sotto forma di olio o di preparati ottenuti dalle foglie, veniva impiegato nella terapia di diverse malattie, come astringente, tonico, febbrifugo e, esternamente, l’olio era usato nella terapia delle ferite, delle ustioni, come antireumatico, come immunizzante nelle morsicature di serpenti velenosi ecc.
Attualmente i preparati delle foglie di Olivo trovano impiego nella terapia delle varie forme di ipertensione ma riuscirebbe piuttosto difficile stabilire a quale epoca risalga l'uso empirico della droga a questo scopo.
E' noto che i contadini di alcune regioni dell’Italia centrale e dell'Umbria in particolare, si servono di queste foglie per la preparazione di tisane che da tempo e con successo impiegano nella terapia dei disturbi che accompagnano gli stati ipertensivi.
Non sembra tuttavia che le proprietà terapeutiche delle foglie di Olivo fossero note soltanto nella nostra medicina popolare poiché, come le ricerche eseguite dal De Nunno (20) in Italia nel 1947, furono ispirate dalla conoscenza del loro uso empirico, la stessa origine hanno avuto quelle eseguite dal Mazet nel 1938 (21) e da Daniel-Brunet e Oliviero nel 1939 (22) in Francia e dallo Stamatiadis nel 1946 ( 23) in Grecia.
Sembra anzi che il merito di aver segnalato per primo l’azione ipotensiva delle foglie di Olivo, note allora soltanto per la loro azione febbrifuga, spetti proprio al Mazet, medico di Nizza, il quale avendo avuto in cura una paziente di 60 anni di età, affetta da una forma di ipertensione, non era riuscito a ottenere in essa alcun miglioramento, pur essendo intervenuto coi più diversi e più noti trattamenti.
Egli riferì di essere rimasto sorpreso per aver in seguito constatato nella sua paziente, una riduzione della pressione e un miglioramento generale, senza poter attribuire questo risultato ad un cambiamento di regime o a nessun'altra causa che lo giustificasse. Soltanto più tardi egli apprese che la paziente, consigliata da una sua fittavola, si era curata assumendo quotidianamente e per il periodo di una ventina di giorni, una tisana di foglie di Olivo.
Il Mazet volle allora sperimentare su più vasta scala questa terapia e cominciò col trattare 38 pazienti ipertesi, somministrando loro un alcoolaturo oppure una decozione ottenuta facendo bollire 20 g di foglie di Olivo in 300 cc di acqua e prolungando l'ebollizione sino a ridurne il volume a 200 cc.
In 30 dei 38 pazienti così trattati, l’A. riferì di aver ottenuto un sodisfacente e durevole miglioramento. Egli notò che l'ipotensione non era dovuta ad un’azione deprimente sul cuore, la cui attività veniva anzi piuttosto migliorata.
La pressione minima veniva ridotta contemporaneamente alla massima e, specialmente all'inizio del trattamento, la diuresi veniva notevolmente aumentata. L’A. notò inoltre che gli ipertesi luetici si dimostravano assolutamente refrattari a questa terapia.
I risultati ottenuti da Mazet vennero in seguito confermati da Leclerc (24) e da altri: Daniel-Brunet e Oliviero, trovarono che la spiccata azione ipotensiva dell'estratto totale di foglie di Olivo é dovuta ad una vasodilatazione periferica e, d’accordo con Mazet, escludono che ad essa partecipi un’eventuale depressione dell'attività cardiaca. Essi insistono anzi sulla perfetta tollerabilità dei preparati da essi usati e affermano di non aver mai osservato azioni tossiche apprezzabili né a carico dell'attività respiratoria, né di altri organi e sistemi.
Le ricerche di De Nunno (20) confermarono in linea di massima questi risultati e permisero all'A. di constatare che l’effetto ipotensivo compare dopo 20-30' dalla somministrazione ed aumenta gradatamente sino a determinare la scomparsa dei disturbi dovuti allo stato ipertensivo. L’A. osservò anche che l’azione ipotensiva dei preparati ottenuti dalle foglie di Olivo, si manifesta in maniera più marcata e più durevole negli ipertesi, mentre i soggetti normali e gli ipertesi diabetici sarebbero meno sensibili e l'azione ipotensiva sarebbe in questi casi, meno evidente e più transitoria.
Capretti (25) studiò sperimentalmente e clinicamente l’azione di infusi di foglie di Olivo a varia concentrazione e poté constatare un’azione ipotensiva negli animali (conigli) cui venivano somministrati. Tale azione conseguirebbe ad una vasodilatazione che anche secondo questo A. sarebbe dovuta prevalentemente ad un effetto miolitico che si esercita sulle fibre muscolari liscie delle pareti vasali. Il fatto che tale vasodilatazione si manifesti anche sulle coronarie, dimostrerebbe appunto la natura muscolare e non nervosa di questa azione.
L’intensità dell'effetto coronarico sarebbe tale da far ritenere all'A. che l'uso dell'Olivo sia indicato anche in quei malati nei quali il determinarsi di uno stato ipotensivo, potrebbe aggravare eventuali difficoltà di irrorazione cardiaca, poiché la diminuita pressione arteriosa sarebbe in questi casi compensata dall'aumentata ampiezza del letto coronarico.
Con altre ricerche eseguite sperimentando su organi isolati a muscolatura liscia e sulla circolazione e secrezione renale, Capretti (26) potè confermare che l'azione ipotensiva é dovuta ad un'azione deprimente sulle fibre muscolari liscie vasali, con esclusione di influenze neurovegetative parasimpatiche determinate da stimoli di tipo acetilcolinico o di altro tipo. Degna di attenzione sarebbe anche, secondo l'A., l'azione che l'Olivo svolge sulla fibrocellula muscolare liscia bronchiale e sulla circolazione e secrezione renale.
Successivamente lo stesso A. (27) riferì i risultati di uno studio clinico eseguito sperimentando l’azione dell'Olivo somministrato sotto forma di infuso al 3-5 % alla dose di 100 cc pro die, su 25 pazienti affetti da ipertensione di varia natura. La cura venne protratta per 15-20-25 giorni a seconda dei casi e l’A. potè notare una notevole azione ipotensiva tanto nei casi di ipertensione renale quanto in quelli di ipertensione essenziale, da menopausa e da arteriosclerosi. In alcuni pazienti fu necessario ripetere il trattamento a breve scadenza al fine di consolidare gli effetti ottenuti. Nei soggetti iperazotemici, l’A. notò una moderata ma costante riduzione dell’azoto non proteico, riduzione che non si notò invece, in individui sani o normoazotemici.
In 14 casi appartenenti alle varie categorie di ipertesi fu notata anche una discreta azione diuretica. In tutti i pazienti i sintomi subiettivi scomparvero o si attenuarono e non furono mai notati fenomeni tossici secondari o da intolleranza.
L'A. consiglia di ripetere periodicamente il trattamento, a distanza di tempo, tanto più che non sembra possano verificarsi fenomeni dovuti ad assuefazione.
Anche più recentemente Capretti e Bonaconza (28) eseguirono altre ricerche sull’azione dell’infuso al 3 % e del decotto al 5 % di foglie di Olivo, sul ricambio e su alcune costanti chimico-fisiche del sangue (viscosità, tensione superficiale). Tali ricerche hanno permesso agli AA. di concludere che la somministrazione delle suddette preparazioni, determina un sensibile aumento della diuresi, una diminuzione del tasso dell’acido urico e, spesso della colesterolemia. Gli AA. concludono attribuendo alla droga un’azione renale, con miglioramento della funzione glomerulare e con aumento dell’eliminazione dei cataboliti azotati e dei sali.
Altre ricerche cliniche e sperimentali furono eseguite in Italia da Cavanna e Pirona (29) i quali impiegando i preparati totali della droga, giunsero a conclusioni analoghe a quelle cui erano pervenuti gli AA. precedentemente citati. Essi infatti concludono che l’estratto idroglicerico di foglie di Olivo, somministrato al cane per via endovenosa alla dose di cc 0,5/kg, determina un abbassamento durevole della pressione arteriosa. Sul ritmo cardiaco e respiratorio e sulla zona reflessogena senocarotidea, gli AA. non hanno osservato alcuna modificazione e la tossicità del preparato impiegato è da essi ritenuta praticamente nulla. Soltanto a dosi elevate insorge bradicardia, bradipnea e l’animale muore con arresto del cuore in diastole.
L’azione ipotensiva si manifesterebbe però a dosi minime; sarebbero sufficienti infatti, dosi di cc 0,1 diluiti in 10 cc di liquido di Ringer, iniettati endovena, per ottenere un notevole effetto ipotensivo. La dose di cc 1,5/kg del suddetto estratto, induce nella cavia un effetto ipotermizzante di breve durata.
Dal punto di vista clinico l’azione dell’estratto preparato dagli AA., venne studiata su di un gruppo di 40 malati affetti da ipertensione essenziale, o da arteriosclerosi o da glomerulonefrite cronica e subcronica. Gli AA. osservarono che la tollerabilità del preparato è ottima, che non dà luogo ad azioni secondarie dannose o sgradevoli: che riduce nettamente sia la pressione sistolica che la diastolica e che i malati sottoposti al trattamento avvertono un notevole miglioramento che si manifesta parallelamente al ridursi della pressione massima, la quale subisce una diminuzione media di 20-30 ed anche 50 mmHg.
Ricerche sull’attività delle foglie di Olivo in casi di ipertensione di
diversa origine, furono eseguite anche da Mainoli (30) il quale avendo sperimentato su 25 pazienti, ottenne risultati positivi in 17 casi, parziali in 2 e nulli in 6.
In particolare, su 10 casi di ipertensione da arteriosclerosi ottenne 6 risultati favorevoli; 8 risultati favorevoli su 8 casi di ipertensione da menopausa; su 3 casi di ipertensione essenziale ottenne un risultato favorevole, un miglioramento parziale e uno negativo e su 4 casi di ipertensione renale ottenne 2 risultati favorevoli, uno parziale e uno negativo.
La completa risoluzione di un caso di emiparesi da probabile spasmo vasale ha indotto l’A. a supporre che l’azione ipotensiva dell’estratto impiegato, sia dovuta a vasodilatazione periferica conseguente a rilasciamento della muscolatura liscia vasale, ipotesi questa che concorderebbe con quella già formulata dagli AA. precedentemente citati e da Couceiro (31) il quale anche ritiene che la droga agisca sulla pressione ematica con un punto di attacco periferico, sulla muscolatura liscia vasale e indipendentemente da una qualsiasi azione neurovegetativa.
Altre ricerche sono state eseguite in seguito al fine di stabilire a quale dei principi attivi contenuti nella droga debba essere attribuita l’azione ipotensiva.
Samuelsson (32) ritiene, contrariamente alle conclusioni cui giunsero gli AA. precedenti, che il principio responsabile dell’azione ipotensiva delle foglie di Olivo, sia la colina. Egli basa tale sua affermazione sui seguenti fatti: la soluzione acquosa di estratti eterei e petroleterei, cloroformici e benzenici, non hanno effetto sulla pressione arteriosa.
Piccole variazioni del pH su estratti acquosi, non modificano l’effetto ipotensivo.
L’effetto dell’estratto acquoso viene diminuito dall’atropina ma non è influenzato trattando l’estratto prima dell’iniezione, con siero di sangue o scaldandolo con alcali.
Dopo acetilazione dell’estratto acquoso, seccato sotto vuoto, si osserva un forte aumento dell’attività ipotensiva, aumento che viene antagonizzato dall’atropina.
L’aumento dell’attività dovuto all’acetilazione, scompare dopo trattamento con siero di sangue o ebollizione con alcali.
L’ipotesi che l’attività della droga sia dovuta alla presenza di colina, sarebbe confermata dal fatto che l’A. ha potuto ottenere la colina dall’e
Anche Janku e coll. (33) che hanno analizzato l’azione di un estratto dializzato di foglie di Olivo, ritengono che tale azione sia dovuta ad una sostanza colinosimile, ma non a colina pura.
Che alla presenza nelle foglie di Olivo, di qualche estere (non acetilico) della colina, possa essere attribuita un’azione coadiuvante, può essere anche ammesso, in base ai risultati delle ricerche di Samuelsson e di Janku e coll., ma certamente non può essere data a queste sostanze un’importanza determinante, soprattutto se si considera che le foglie fresche, la cui attività è forse superiore a quella delle foglie essiccate (24), non contengono colina
(19) e d’altra parte, le ricerche di Kosak e Stern (34) dimostrano che la colina può non essere considerata come il principio ipotensivo delle foglie di Olivo. Questi AA. hanno sperimentato l’azione di un infuso della droga su ratti nei quali un aumento della pressione era stato determinato con renina o con arterenolo o con ambedue queste sostanze somministrate contemporaneamente. Essi notarono che l’ipertensione indotta da queste sostanze era abbassata dal suddetto infuso, in maniera più pronta, più durevole di quanto era possibile ottenere con solfato di idrazinoftalazina, con solfato di 1-4 diidrazinoftalazina o con reserpina, mentre la pressione normale non era influenzata.
Balansard e Delphaut (6) che hanno isolato dalle foglie di olivo due glicosidi, l’oleoeuropeoside (oleuropeina) e l’oleoside (ved. parte chimica), attribuiscono l’azione ipotensiva immediata e diretta della droga, all’oleoside, mentre un’azione indiretta e lontana viene attribuita dagli AA. alla depurazione determinata dall’attività epato-renale (diuretica e coleretica) di cui sarebbe dotato l’acido glicolico. All’europeoside viene invece attribuita l’attività blandamente ipoglicemizzante di cui è dotata la droga.
Esperienze cliniche con esito favorevole sono state riferite anche da Esdorn (35-36), da Schwarz (37), da Scheller (38), da Stegmann (39), da Luibl (40) e da Rossier (41) il quale ultimo sperimentò su di un gruppo di pazienti ipertesi, un preparato risultante dall’associazione dell’Olivo con esanitroinosite e Rauwolfia (estr. secco di foglie di Olivo g 0,05, esanitroinosite g 0,02, Rauwolfia serpentina g 0,0015, silicio g 0,02), constatando che nella maggior parte dei casi la pressione veniva abbassata o notevolmente migliorata, mentre contemporaneamente si osservava la regressione dei sintomi secondari (cefalea, vertigini, insonnia, stato ansioso, ronzii auricolari, dispnea).
Una teoria sul probabile meccanismo dell’azione ipotensiva dell’Olivo è stata recentemente formulata da Kosak e Stern (42) i quali hanno sperimentato sui ratti, l’azione sul metabolismo del sodio e del potassio serico e urinario e sul metabolismo del rame nel cervello, nel fegato e nel siero, di un estratto acquoso di foglie di Olivo. Particolare attenzione è stata rivolta dagli AA. all'azione del suddetto estratto sul metabolismo del rame, in considerazione delle correlazioni esistenti fra gli enzimi ossidanti contenenti rame e le catecolamine (adrenalina e noradrenalina).
Gli AA. hanno notato che, mentre l’estratto acquoso di foglie di Olivo non altera il metabolismo del Na e del K, diminuisce notevolmente il contenuto del rame nel cervello, nel fegato e nel siero di ratto.
Gli AA. ritengono che mediante una inibizione dell’attività dei suddetti enzimi, prodotta dalla diminuzione del contenuto del rame nell’organismo, si giunga ad una riduzione della biosintesi delle catecolamine e, conseguentemente, all’azione ipotensiva.
Dopo trattamento con estratto acquoso di foglie di Olivo, l’aumento della pressione arteriosa prodotto nei ratti da una dose uguale di DOPA (3,4-diossifenilalanina), risulta molto inferiore a quello che si ottiene di solito con somministrazione di DOPA in animali non pretrattati col suddetto estratto.
Anche questo risultato dimostrerebbe secondo gli AA., una inibizione della biosintesi delle catecolamine come conseguenza della diminuzione della concentrazione del rame nell'organismo.
Alle foglie di Olivo viene attribuita anche un'azione ipoglicemizzante evidenziabile sia sperimentalmente che clinicamente [Jardon (43), Manteau e coll. (44), Scheller (45)],
Anche l’olio di Olivo, largamente usato nell’alimentazione, trova impiego in terapia soprattutto come moderato lassativo nei casi non gravi di stipsi cronica e specialmente quando questa sia dovuta ad alimentazione irrazionale,
Eccita le contrazioni della colecisti determinando quindi un’azione colagoga e per tale sua azione colecistocinetica viene impiegato anche a scopo diagnostico.
Sotto forma di clistere, alla dose di 150-500 cc, scaldato alla temperatura corporea, è frequentemente usato per facilitare l’espulsione delle feci e per risolvere alcuni stati di stasi fecale dei segmenti inferiori dell’intestino.
Estratti e preparati vari
a) Estratto fluido (g 1 = XXXII gtt).
Dosi: g 3-5 pro die.
b) Estratto secco acquoso (1 p. = 8 p. circa di droga).
Dosi: g 0,4-0,6 pro die.
Preparazioni usuali e formule galeniche
Tintura
Estratto fluido olivo……………………………………………………… g 20
Alcool di 20°………………………………………………………………… g 80
(g 15-25 pro die).
Sciroppo
Estratto fluido olivo…………………………………………………. g 10
Sciroppo semplice F.U………………………………………………… g 90
(30-60 g prò die).
Pozione
Estratto fluido olivo…………………………………………………. g 15
Estratto fluido biancospino……………………………………….. g 5
Estratto fluido arancio dolce alcool-idrosolubile……….. g 5
Sciroppo semplice F.U………………………………………………… g 30
Acqua q. b. a……………………………………………………………….. g 150
(3 cucchiai pro die).
BIBLIOGRAFIA
(1) BOURQUELOT E. e VENTJLESCO J., Compì, rend., 147, 533, 1908; J. pharm. chim., 28. 303, 1908; ibid.. I, 292, 1910 – (2) POWER F. B. e TUTIN F., Pharm. J.. 27, 714, 1908; /. Chim. Soc., 93. 891, 1908 – (3) VANZETTl B. L., Rend. Accud. Lincei, 2. 188, 1909 – (4J CRUESS W. e ALSBERG C. L„ J, Am. Cbem. Soc., 56, 2115, 1934 – (5) JARDON P., Thése Docl. Pharm., Strasbourg, 1938 – (6) BALANSARD J. e DELPHAUT J., Rer. * Phyiothér., 17, 19 e 35, 1953 – (7a) SHASHA S. e LEIBOWITZ
Bull. Res. Council Israel. A 8, 92. 1959; Nature. 184, 2020, 1959 • (7b) SHASHA S. e LEIBOWITZ J„ J. Org. Chem., 26. 1948, 1961; Chem. Abs.. 55, 24640g, 1961 – (7c) MECHOULAM R„ DANIELI N. e MAZUR Y., Teirahedron Lellers, 709, 19 6 2 • (8) PANIZZl L., SCARPATI M. L. e ORIENTE G., Ricerca Sci, 28, 994, 1958 – (9) PANIZZl L„ SCARPATI M. L. e ORIENTE G-, Gazz. Chim. Ita!., 90, 1449, 1960 – CIO) KARRER P, Konstilution und Vorkommen der organischen PflanzenslDfle, 1958, p. 19 – (11) BAUMGARTEN G„ Pharmazie, 13, 378, 1958 – (11 a) HUNECK S„ Naiurwiss.. 48, 73, 1961; Chem. Abs., 55, 23581, 1961 – (12) KOFLER M., LANGEMANN A., RUEGG R., CHOPARD-DIT-JEAN L. H„ RAYROUD A. e ISLER O., Helv. Chim. Acla, 42, 1283, 1959 – (13) KOFLER M., LANGEMANN A., RUEGG R., GLOOR U., SCHWIEIER U., WUERSCH J., WISS O. e ISLER O., Helv. Chim. Acla, 42, 2252, 1959 – (14) VEER W. L. C, GERRIS V., RIBBERS J. E., OUD P. J„ VAN REE P.J., BEYERMAN H. C. e BONTEKOE J. S.. Ree. Trav. Chim., 76, 839, 1957; Chem. Abs., 52, 3258 h, 1958 – (14a) BEYERMAN H. C., VAN DIJCK A., LEVISALLES J„ MELERÀ A. e VEER W. L. C„ Bull. Soc. Chim. France, 1812, 1961; Chem. Abs., 57, 7096, 1962 – (15) BALANSARD J. e BERNARD P., Bull. soc. pharm. Marseille, n. 2, 28, 1952 – (16) PASSERINI M., RIDI M. e RAPINI P„ Ann. chim., 43, 201, 1953; Chem.
Abs., 48, 10587Ì, 1954 – (17) DANIEL-BRUNET A, L. F. e OLIVIERO M„ Buli. Acad. Mid., n. 28,
191, 1939 • (18) SAMUELSSON A. G., Farm. Revy, 50, 229, 1951; Collecl. Pharm. Suec., voi. VI, 1951 –
(19) VASQUEZ RONCERO e MAZUELOS VELA F.. Grasas y aceiles, 8, 247, 1958; Chem. Abs., 52, 12030 1, 1958 – (19a) STEINEGGER E. e JACOBER H., Pharm. Acla Helv., 34, 591, 1959 – (20) DE NUNNO R., Riv. di din. Med., 506 e 511, 1947 – (21) MAZET, Gaz. Méd, de Plance 1“ gennaio 1938 • (22) DANIEL-BRUNET A. e OLIVIERO M., Bull, de i’Acad. de Mid., 122, 191, 1939 – (23) STAMA- TIADIS A., O Ellen Esperantistes, 139, 1779, 1946 – (24) LECLERC H„ DECAUX F. e VALERY- LECLERC R„ Rev. de Phylolhir., 18, 7, 1954 – (25) CAPRETri G., Giorn. di Clin. Med., 29, 4, 394, 1948 – (26) CAPRETri G., ibid., 29, 5, 491, 1948 – (27) CAPRETTI G„ ibid., 29, 8, 856, 1948 – (28) CAPRETTI G. e BONACONZA E„ ibid., 30, 630, 1949 – (29) CAVANNA D. e PIRONA M., Boli chim. farm., 89, 3. 1950 – (30) MAINOLI S., Min. Med., 42, 751, 1951 – (31) COUCEIRO P., Sistole, 2, 39, 1951 – (32) SAMUELSSON G., Collec. Pharmac. Sueclca, 6, 1951; Farmaceullsk Revy, 50, n. 15, 14 aprile 1951 – (33) JANKU J., RASKOVÀ H.. MOTL O, e BLAZER Z., Arch. iniern. pharmacod. et de
Ihér., in, 342, 1957 – (34) KOSAK R. e STERN P„ Acla Pharm. lagosi, 6, 121, 1956 – (35) ESDORN }.,
Pianta Med., n. 5, 145, 1954 – (36) ESDORN J„ Acla Phylolher., I, Ì0, 13, 1955 – (37) SCHWARZ F. K. TH„ Medizinische, n. 41. 1387, 1954 – (38) SCHELLER E. F., Med. Klln., n. 8. 327, 1955 – (39) STEG- MANN K., Landarzi, n, 15, 375, 1955 – (40) LUIBL E„ Med. Monaischr., 12, 181, 1958 – (41) ROSSIER M., Proxir, n. 48, 1135, 1956 – (42) KOSAK R. e STERN P., Arzneim. Forsch., 12, 919, 1962 – (43) JARDON P., ThSse fac. Pharm. Univ. Lyon 1942 – (44) MANCEAU P., NETIEN G. e JARDON P.. Conip. rend. soc. hiol., 136, 810, 1942 – (45) SCHELLER E. F., Med. Klln., 50. 327, 1955.

