Papavero (da Oppio)
Tratto da “Piante Medicinali – Chimica, Farmacologia e Terapa” di R. Benigni, C. Capra e P.F.Cattorini
(Papaver somniferum L. – Fam, Papaveracee/Papaveroidee/Papaveree) [Sin. – Papaver somniferum b hortense Hussenot (non Huds. = Hudson)]
Papavero (da Oppio)- Ultimo aggiornamento pagina: 27/02/2018
Indice dei contenuti
- Generalità
- Componenti principali
- Proprietà farmacologiche
- Estratti e preparati vari
- Preparazioni usuali e Formule
- Bibliografia
Generalità

Etimologia – Papaver (ved. P. Rhoeas).
somniferum, da somnus fero = che fa dormire.
Il Papaver somniferum L. non si può affermare che esista allo stato spontaneo: coltivato da secoli, sfugge alle colture e può trovarsi naturalizzato nelle località del sud/Europa, dove viene coltivato.
Si ritiene che derivi dal Papaver setigerum DC., spontaneo nella Regione Mediterranea (Spagna, Algeria, Corsica, Grecia, Cipro) ed anche in Italia nella Regione Tirrenica (Liguria, Toscana, provincie meridionali, Isole). L’indicazione «originaria dall'Oriente» è discutibile perchè, se è esatta la deduzione dei Botanici, la coltura deve essere stata iniziata in Europa e, forse, nell’Africa settentrionale (così A. De Candolle).
Il Papaver setigerum DC. si distingue per le foglie inciso-dentate, a denti stretti, terminati da una setola, pelose nel resto, peduncoli e sepali setolosi (da ciò il nome setigerum o saetigerum = saeta (setola) e gero (porto) = setoloso).
Considerata Papaver somniferum L. la pianta coltivata, si elencano le varietà:
Papaver somniferum var. a album (Mill.) DC.
Papaver somniferum var. b nigrum DC. (sin. – P.s. var. glabrum Boiss.).
Tutte queste varietà sono utilizzate per l’estrazione dell’Oppio (dal opos = succo).
La più coltivata è, generalmente, la var. album (Mill.) DC., la var. nigrum DC. o glabrum Boiss. è coltivata particolarmente per i semi da olio.
La var. album (Mill.) DC. ha le cassule grosse, indeiscenti (senza pori substimmatici), con semi bianchi o giallicci, talvolta soffusi di violaceo. Le cassule sono di due forme: a) oblunga (ovoide, affusolata, da cm. 5 X 2,5 a cm. 6-8 x 2-2,5) – b) depressa (il diametro trasversale supera il longitudinale e può raggiungere i 10-12 e più cm. su 5-6 cm.). Lo stimma è sessile a forma di disco radiato, a lobi corti, ottusi o un po’ acuti, poco rilevati, portante 10-12 strie stimmatiche radiali, rugose, bruniccie, rilevate. La superficie è liscia, con solchi appena accennati corrispondenti ai setti interni incompleti, color giallo/grigiastro e grigio/verdastro, sovente punteggiata di bruno.
La var. nigrum DC. o glabrum Boiss. ha le cassule più piccole globuloso/sferiche, con solchi esterni più pronunciati, deiscenti, per mezzo di opercoletti, piccole aperture dovute all’allungamento delle lamine che uniscono le placente seminifere (trofospermi – dal greco trefw = nutro e sperma = seme) agli stimmi. Al disotto dello stimma, che non è depresso, ma ha i segmenti rilevati, obliqui e curvi, lacerandosi e ripiegandosi la membrana, si formano delle piccole aperture substimmatiche corrispondenti ciascuna ai setti incompleti interni, dalle quali fuorescono i semi, bruni o ceruleo-neri.
Le cassule nelle due varietà variano di forma e di volume. Esistono razze con semi bleu, rossi, grigi, gialli.
Nel Papaver setigerum DC. la cassula è glabra, deiscente, subglobosa, del volume di una noce.
Tutti i «capi o teste di papavero» hanno un residuo di stelo più o meno lungo, resistente, duro.
La var. album (Mill.) DC. è coltivata in India (Behar, Benares, Bolkar, Labore, Ghazipur), Persia (Iran), Turchia, Asia Minore (Anatolia, distr. di Ghiveh, Amasia, Balukissar, Karahissar (afium = arab. oppio) (Karahissar = la montagna dell'oppio). Trasgiordania, Armenia, Egitto, Grecia (Macedonia, Tracia), Egitto, Marocco (Rabat, Marrakech, Rharb.), Cina (Manciuria, Mongolia), Belgio, Francia n/, Jugoslavia, Bulgaria, Ungheria.
Nelle stesse località è anche coltiva la var. nigrum DC. o glabrum Boiss. Per i semi da olio, in Belgio, Francia n/(Amiens), Olanda, Germania, Ungheria.
Il Papaver setigerum DC. è coltivato come pianta ornamentale nel sud/Europa. In Belgio, Francia n/, Olanda per i semi da olio: in Turchia anche per l’oppio.
Nomi volgari – Papavero domestico, papavero indiano (tosc.), adormia (lomb,), papagno de la suonno (nap.), cucuzzeddi (le cassule) di sonnu (sic.), papaveru medicinali (sard.), ecc.
Pavot blanc, pavot des jardins (fr.), white poppy (ingl.), Weisser Mohn, Schlafmohn (ted.), dormidera (spag.), slaaphruid, heul (oland), wit tammeheul (belg ), mak (ungh.), Boù-en-noum (che procura il sonno) o Tuhfat-al-ahbàh (per il tintinnio (arab. tahashus) che producono i semi nelle cassule agitate), ing-tse-sou, ing-sou-hoa (cinese).
Parti usate – Le cassule.
Componenti principali
Morfina e gli altri alcaloidi, che si trovano nell’Oppio, per la cui identità e composizione chimica rimandiamo alla consultazione della parte riguardante l’Oppio.
Contenuto di morfina
Esperimenti d’estrazione della morfina dalle capsule mature e secche del Papaver somniferum L. sono stati fatti sin dal 1823 da Tilloy (1). Poco dopo Petit (2) ottenne dai fusti e dalle foglie verdi del Papavero una certa quantità di morfina. Successivamente numerosi altri AA. cercarono di estrarre la morfina e gli altri più importanti alcaloidi, invece che dall’Oppio, dalle capsule del Papavero (3-18a) (19a-20).
E' stata studiata anche la possibilità di estrarre morfina dai fusti. Kabay (19) riprese gli studi degli AA. precedenti (1)(2) e nel 1933 pubblicò brevetti di preparazione della morfina dalla «paglia» del Papavero con rese dello 0,07-0,08%. Da analisi di Papavero di Jugoslavia, precisamente di Macedonia, Ristic (19 a) e Akacic (19b) hanno rilevato che la parte superiore dello stelo, 10 cm circa sotto la capsula, contiene una quantità di morfina pressapoco uguale (0,26%) a quella delle capsule stesse e che essa è quindi la sola parte dello stelo, da cui l’estrazione della morfina sia redditizia, poiché il rimanente ne contiene una quantità molto inferiore (circa 8 volte più bassa rispetto alle capsule).
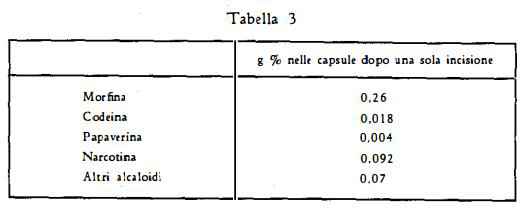
Per l’estrazione degli alcaloidi è ovviamente molto più redditizio l’uso delle capsule non incise (ved. tabella 2). Resa buona danno le capsule di Jugoslavia e, precisamente di Macedonia, dalle quali l'Oppio si estrae solitamente con una sola incisione. Vi si sono trovati 0,26% di morfina base e 0,914% di altri alcaloidi (ved. tabella 3) (19a). E’ stato notato che il migliore rendimento di alcaloidi è dato dalle capsule raccolte poco prima della maturazione. Tuttavia, poiché in generale si vogliono utilizzare anche i semi maturi, é necessario raccogliere le capsule a piena maturazione, curando di eseguire l’estrazione degli alcaloidi rapidamente.
Wùest e Frey (12), che hanno analizzato campioni di droga di diversa provenienza, hanno trovato titoli varianti dallo 0,18 allo 0,9% di morfina ed hanno concluso che è possibile disporre di capsule mature secche, aventi una media dello 0,3-0,5 % di morfina.
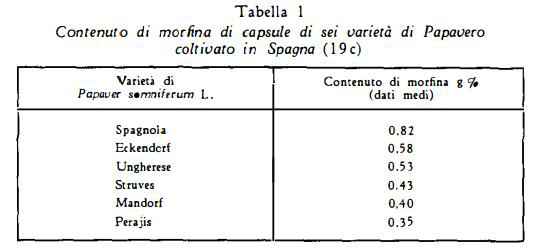
Nelle capsule il contenuto di morfina varia quindi entro larghi limiti ed é stato stabilito che esso dipende da caratteri ereditari, cosicché con una accurata selezione delle diverse varietà di Papavero é possibile innalzare notevolmente le rese. Ricerche per selezionare varietà di Papavero, adatte alla produzione della morfina, sono state fatte in diversi paesi (13-18). In Germania Kussner (13) ha ottenuto da capsule di due selezioni dallo 0,257% allo 0,544% di morfina e dallo 0,011% allo 0,029% di codeina rispettivamente. In Romania Kopp (17) (18) ha raggiunto rese medie pari all’1 % di morfina. In Francia Lécat (15 a), dopo selezione di quattro anni, ha avuto una popolazione omogenea di Papaver somniferum L. (var. nigrum) con capsule contenenti in media 0,735% di morfina. In Cecoslovacchia Voskerusa (18a) in capsule di Papavero selezionato ha trovato come titolo massimo 0,469 % di morfina. In Australia Barnard e Finnemore (15b) dalle capsule di due varietà di Papavero hanno ricavato 0,29-0,39% e 0,26-0,30% di morfina e dalla pianta intera 0,09-0,16% e 0,12-0,18% di morfina rispettivamente.
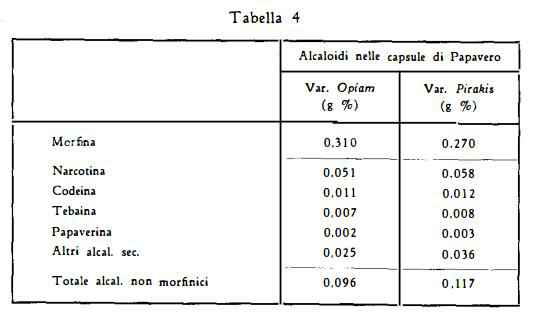
In Italia nella zona di Broni (Pavia), dal Papaver somniferum var. Opiam e var. Pirakis, Rovesti (16) ha avuto un’alta resa di morfina per ettaro (kg 2,356 e kg 2,376 per ettaro rispettivamente) con un contenuto di 0,31% e 0,27% di morfina e di 0,096% e 0,117% di altri alcaloidi non fenolici, rispettivamente, nelle capsule delle due varietà saggiate. Lo stesso A. ha notato un aumento delle rese, sia in morfina, sia in quantità di capsule, per le piante coltivate ad altitudine sino ai 600 m s.m. Valente (16a) ha ottenuto risultati più bassi 0,0798%, 0,0776%, 0,0921% e 0,1012%, rispettivamente, nell'analisi della morfina delle capsule secche del Papavero spontaneo di Bari, Brindisi e di Taranto e di quello coltivato nel territorio di Bari.
La quantità di morfina nelle capsule dipende, oltre che da caratteri ereditari, anche dalle condizioni ambientali, specialmente climatiche (precipitazioni atmosferiche, esposizione al sole ecc.), in cui è cresciuta la pianta. I migliori risultati in zona rumena sono stati ottenuti in clima caldo, non molto umido (17) (18). Il clima molto secco agisce sfavorevolmente sul contenuto di morfina, specialmente durante la crescita e la fioritura (20).
L’influenza degli elementi minerali dei concimi sembra sia nulla sul titolo di morfina delle capsule del Papavero. Solo l’azoto, in dosi moderate, provoca un aumento significativo del peso dei semi e delle capsule vuote (15 a).
Contenuto di alcaloidi nelle capsule e nelle altre parti della pianta
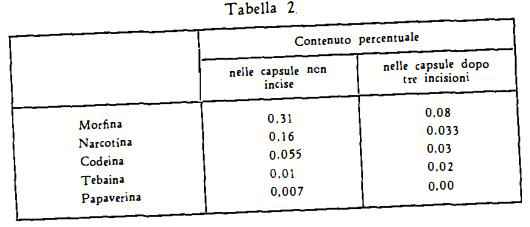
Nelle capsule non incise l’analisi quantitativa dei più importanti alcaloidi ha dato i risultati raccolti nella I colonna della tabella 2. Dopo tre incisioni per ricavarne il lattice, il titolo si è abbassato ai valori indicati nella II colonna della stessa tabella (21).
Nelle capsule di Jugoslavia (Macedonia) dopo una sola incisione sono stati trovati i seguenti titoli (19 a):
Dosando gli alcaloidi contenuti nelle capsule di Papavero var. Opiam e Pirakis, coltivato in Italia, si sono avuti i risultati seguenti (16):
La ripartizione degli alcaloidi nelle varie parti della pianta subisce notevoli mutamenti nel corso del ciclo vegetativo (21-26) e della giornata (26b). Gli alcaloidi, che accompagnano la morfina in tutte le parti della pianta durante la crescita, raggiungono nelle capsule un massimo che si avvicina a quello della morfina, ma il loro contenuto subisce maggiori variazioni durante la crescita della pianta (26c). Nella tabella 5 sono indicati i valori trovati durante i tre principali stadi di crescita per il contenuto di morfina di vari organi del Papaver somniferum L. (17).
Le capsule del Papavero rappresentano quindi l’organo più ricco di alcaloidi. Alla fine del ciclo vegetativo vi sono stati trovati sino al 70 %
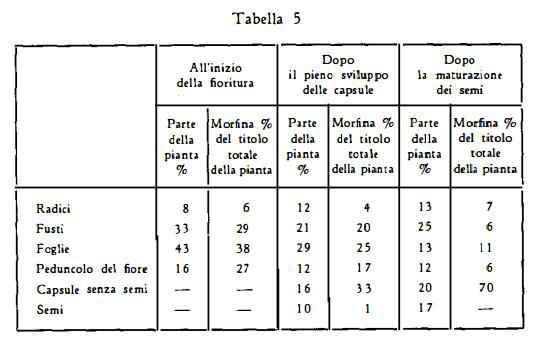
della quantità totale di morfina, (17) (22a), circa l’80% delle quantità totali di narcotina e di papaverina e circa il 60 % delle quantità totali di codeina e di tebaina contenute nella pianta intera (22a).
Nelle capsule già pienamente sviluppate (senza semi) di Papavero coltivato in Romania, è stato trovato un titolo di morfina pari allo 0,45%, aumentato successivamente sino al massimo dello 0,64% (17). Il contenuto di morfina nelle capsule diminuisce poi con la maturazione. Da prove eseguite in Cecoslovacchia è risultato cha da un contenuto di morfina di 0,208-0,235 % per le capsule immature si scende ai valori 0,188-0,131 % per le capsule pienamente mature, dopo l’allontanamento dei semi (22b). Nei fusti, nelle radici e nelle foglie (essiccate all’aria) all'inizio del periodo vegetativo è stato determinato lo 0,11%, 0,12% e 0,10 % di morfina rispettivamente, mentre, nel periodo del pieno sviluppo dei semi, non ancora maturi, 0,19%, 0,08% e 0,19% di morfina rispettivamente. Nei semi immaturi 0,04% e nei semi maturi assenza di morfina (17). Nelle piante giovani è stato trovato un contenuto di morfina pari allo 0,07%, titolo aumentato poi gradualmente fino ad un massimo dello 0,20 % nel periodo della caduta dei petali e rimasto tale per circa due settimane per diminuire poi allo 0,09% durante la maturazione delle capsule (26a).
Nelle radici in generale è contenuta una quantità di codeina superiore a quella del resto della pianta. Negli steli invece è principalmente localizzata la tebaina, mentre la morfina e la narcotina si trovano in massima parte nelle capsule. Tuttavia si è notato che, quando un alcaloide compare in qualche parte della pianta, si trova contemporaneamente in tutti gli altri organi della pianta stessa (27).
Tanto nelle parti vegetative che negli organi riproduttivi, predominano gli alcaloidi del gruppo del fenantrene; degli alcaloidi del gruppo dell’isochinolina prevale la narceina (26c).
Altri componenti delle capsule
Glucidi: in un estratto acquoso di capsule di Papavero di origine jugoslava sono stati identificati glucosio, fruttosio, saccarosio, sedoeptulosio, mannoeptulosio ed un poliosio complesso, che per idrolisi acida produce arabinosio, xilosio, ramnosio, glucosio, galattosio, un acido uronico, probabilmente acido galatturonico, ed un componente non indentificato (28).
Amminoacidi: acido aspartico, acido glutammico, lisina, arginina, glicina, serina, asparagina, glutammina, treonina, alanina, acido 7-amminobutirrico, prolina, acido pipecolico, valina, leucina, fenilalanina sono presenti in forma sia libera che combinata; tirosina si trova in tracce in forma libera, in quantità maggiore in forma combinata; istidina è pure presente in tracce in forma libera, assente in forma combinata (29).
Enzimi: una ossidasi ed una perossidasi, cui Annett e Singh (30) e Abraham e Rae (31) hanno attribuito il processo di alterazione della morfina nell’Oppio; secondo Nilow, Nilowa e Trotschenko (32) sarebbero una perossidasi ed una invertasi i responsabili della perdita della morfina, che oscillerebbe tra il 7 ed il 35 % nel lattice fresco del Papavero, mentre, secondo Schenck e coll. (33), nel lattice, come enzima ossidante, si troverebbe soltanto una fenolossidasi, che, in presenza degli acidi fenolici, acido caffeico o cumarico, determinerebbe l’ossidazione della morfina con degradazione di questa sino ad un valore del 15%. Questo processo di alterazione avviene durante la preparazione ed il magazzinaggio dell’Oppio.
Altri componenti delle capsule: gli acidi caffeico (20,4 mg % nella droga secca), p-cumarico (3,3 mg % nella droga secca), ferulico, p-ossibenzoico, esculetina (33) (33a), meconina (34), cera costituita da esteri degli acidi palmitico e cerotico con alcool cerilico (35).
Componenti (oltre agli alcaloidi) delle altre parti della pianta
Nei semi: olio 40-60 % secondo la provenienza. L’olio è ottenuto industrialmente mediante pressione, fatta in due tempi, la prima pressione a freddo, che dà l’olio bianco di uso commestibile, la seconda a caldo, che dà un olio essiccativo (olio rosso), usato industrialmente.
L’olio di semi di Papavero contiene gliceridi di acidi grassi costituiti dal 65 % di acido linoleico, 5 % di acido linolenico, 30 % di acido oleico; vi è stato trovato anche acido palmitico (7%) (36).
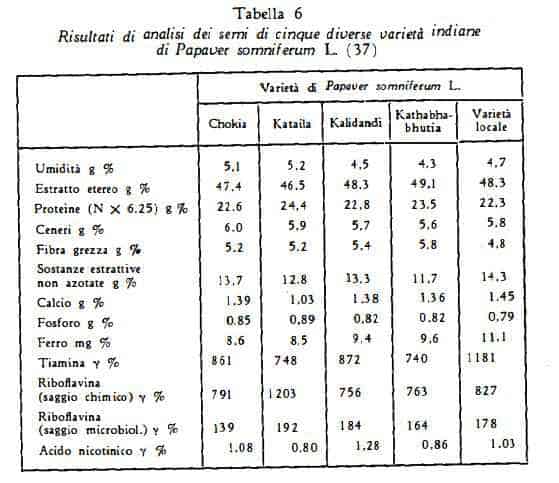
Nei semi sono stati trovati inoltre enzimi [diastasi, emulsina, lipasi, nucleasi] (38), proteine 20% ca., glucidi 15%, lecitina 0,25-5,5%, vitamina B1 1,36 mg %, vitamina B2 24 g %, sitosterolo. Valore calorico dei semi: 5,500 cal/kg (39).
Dai fusti, dopo l’estrazione degli alcaloidi, è stata ottenuta una frazione estrattiva idrosolubile, in cui sono stati identificati i seguenti componenti: p-ossibenzaldeide, vanillina, p-ossistirene, meconina e gli acidi fumarico, dl-lattico, benzoico, p-ossicinnamico, p-ossibenzoico, 2-ossicinconinico, vanillico, ftalico, emipinico e m-emipinico, tre sostanze non ben
definite Fx p.f. 271°-2°, Wx p.f. 310° (dec.) e Q p.f. 260° ed un acido carbossilico insaturo (sostanza «I») (40) identificato con l’acido 11-metossi-12,13-diossi-ottadeca-9,16-dien-1-carbossilico, C19H34O5 (41).
Nella pianta del Papavero è stato trovato anche acido chelidonico, combinato con basi organiche o come sale di calcio (42); inoltre uno sterolo (papaveristerina) (43), probabilmente identificabile con il b-sitosterolo (44).
Nelle foglie vitamina C: sino a 121 mg % nella droga fresca (pari a 600 mg % nella droga secca) (45).
Proprietà farmacologiche ed impiego terapeutico
Sedativo e leggero ipnotico anche oggi erroneamente usato sotto forma di decozione, nella medicina popolare e familiare, come ipnotico e per calmare gli stati di agitazione, specialmente notturna, nei bambini; pratica assolutamente da sconsigliarsi sia per la notevole sensibilità dei bambini di fronte agli alcaloidi dell’Oppio (morfina), sia per la variabilità del contenuto percentuale in morfina nelle capsule di Papavero. Sono stati descritti numerosi casi di avvelenamenti gravi e anche mortali nei neonati.
Come ipnotico e sedativo si usa sotto forma di sciroppo o per clistere, specialmente nei casi di insonnia nervosa. Usato anche per gargarismi e per colluttorio ad azione anodina ed emolliente.
Estratti e preparati vari
Estratto fluido (Titolo chimico inferiore allo 0,05 di morfina) (g 1 = XL gtt).
Dosi: XXX-XL gtt pro dose, 3-4 volte pro die.
Preparazioni usuali e formule galeniche
Tintura
Estratto fluido papavero………………………………………………………… g 20
Alcool di 20°…………………………………………………………………………. g 80
(g 2,5-5 pro dose).
Sciroppo
Estratto fluido papavero ……………………………………………………….. g 5
Sciroppo semplice F.U. ……………………………………………………… g 95
(un cucchiaino 2-3 volte pro die).
BIBLIOGRAFIA
(1) TILLOY, Extrait des registres des délibérations de VAcadémie des Sciences, Arts et Belles-Lettres de Dijon, riportato nel J- de Pharm., 13. 317, 1827 – (2) PETIT P. H., /. de Pharm., 13. 170, 1827 – (3) WINCKLER F. L., Reperiorium fur die Pharmacie, 39, 468, 1831 • (4) WINCKLER F, L., Repertorium fUr die Pharmacie. 59, 1, 1837 – (5) MERCK cit. da WINCKLER F. L., loc. cir – (6) TROMSDORFF J. B., Neues J. der Pharmacie, 17, 256. 1828 – (71 THOMS H.. Arbeiten a. d. Pharmaz- InstUut Beriin, 4. 204, 1907 e Ber., 17, 4, 1907 – (8) ALLAN MALIN PUNKALAIDUN, Arheiten a.d. Pharmaz. Institut Berlin, 4. 250. 1907 e Ber,, 17, 60, 1907 – (9) HEIDUSCHKA A. e PAUL M. Arch. Pharm.. 255, 172, 1917 – (10) BUCHNER, Arch. Pharm., 121. 323. 1852 – (11) GORIS A., BuH. sci. pharm., 45. 265, 1938; 46, 376, 1939 – (12) WUEST e FREY, Pharm. Monats., Il, 73 (C/iem. Ahs., 24, 3322, 1930; 25, 2518, 1931); Ber. unR. pharm. Ges., 12, 387, 1936; Hungarian Pat„ 109.788 {Chem., Ahs.. 28, 5182, 1934); British Pat.. 406.107; German Pai., 524,964; U.S. Pat., 2.009,181 – (13) KUESSNER, Merck's Jahresb., 54. 29, 1940; Chem. Abs., 35. 8203, 1941 – (13 a) HEEGER E. F., Forschungsdienst, 8, 508, 1939; Phar- mazie, 12. 287, 1957 – (13 b) KLEINSCHMIDT G. e MOTHES K„ Pharmazie. 13. 357, 1958 – (14) GUILLAUME e FAURE, Ann. pharm. fran^.. 4. 160, 1946 – (15) VAN ITALLIE, Ann. pharm. frane., 4. 156, 1946 – (15 a) LECAT P., Ann. pharm. frane., 14, 714, 1956; Presse Méd., 64. 1979, 1956 – (15 b) BARNARD e FINNEMORE, Repts. Council Sci. Ind. Res. Australia. 1941-2, 1942-3; J. Council Sci. Ind. Res, Aust., 18, 277, 1945 – (16) ROVESTI P., Riv. ital. ess. prof.. 36, 211, 1954 – (16 a) VALENTE M„ Boll. chim. farrn,, 90, 223, 1951 – (17) KOPP E. Pharmazie. 12. 614, 1957 – (18) KOPP E., KOTILLA E., CSEDO K e MATYAS S,, Pharmazie. 16, 224, 1961 – (18a) VOSKERUSA VON J., Pharmazie, 15, 552. 1960 – (19) KABAY J.. Ungar. Patent., 109.788, 1 maggio 1934 – E.P. 406.107. 9 novembre 1932; Chem. Zbl„ II, 1162, 1934 – (19a) RISTIC V., Relaz. alla XIV Assemblea Generale della Fédération Internationale Pharmaceutique • Roma 23-29/7/1951 > (19b) AKACIC e coll, Acta Pharm. Jugosh, 1, 3, 1951 • (19c) URGUELLES L. D., Anales fac. qu'tm. farm., Univ. Chile, 8, 309, 1956; Chem. Abs., 54, 113781, 1960 – (20) FELKLOVA M. e MIKULECKA J., Sbornik Ceskoslov. Acad. Zemedei. Ved. Rostlinà vyroba 4 (31). 149, 1958; Chem. Abs., 52, 12090, 1958 – (21) KLYATCHKINA B. A. secondo la relazione di GORIS A., Buil. sci. pharm.. 46, 380,1939>(22) MUELLER A.. Arch. pharm.. 252. 280, 1914 – (22a) NIKONOV G. K., BhII. stup., 10. n. 1. 22, 1958 – (22b) KUCERA M.. Ceskoslov. farm.. 4. 308, 1955 – (23) POETHKE W. e ARNOLD E., Pharmazie, 6 . 406, 1951 – (24) WEGNER E., Pharmazie, 5. 33. 1950: 6. 55 e 420. 1951 • (25) SARKANY S. e DANOS B., Acta Boian. Acad. Sci. Hung.. 3, 293, 1957; Chem. Abs., 52, 10300, 1958 • (26) MIRAM R, e PFEIFER S., Naturwiss., 45, 573, 1958; Chem. Abs., 53, 11523 f, 1959; Sci. pharm., 27, 34, 1959; 28, 15, 1960; PFEIFER S„ Pharmazie, 17, 107, 536, 1962 – (26a) ROEMISCH H., Pharmazie, 13, 769, 1958 – (26b) HEYDENREICH K. e PFEIFER S„ Sci. pharm„ 30. 164, 1962 – (26c) AKSANOWSKI R„ JURZYSTA M., KRACZKOWSKA J. e WIErZ- CHOWSKl Z„ Dissert. Pharm., 14, 58, 1962 – (27) PFEIFER S„ Pharmazie, 15, 271, 1960 – (28) ELI OTTESTAD, BINAR BROCHMANN HANSSEN, DAGRUN OISETH e ARNOLD NORDAL, J. Pharm. Phartracol., 11. 689, 1959 – (29) KLEINSCHMIDT G., Pianta Med., 8, 114. 1960 – (30) ÀNNETI H. E. t SINGH H. D., Pharmac. 1. Pharmacist, 109, 304, 1922 • (31) ABRAHAM A. C. e RAE J., Pharmac. 1. Pharmacist, 117, 32, 1926 .(32) NILOW W. I., NILOWA W. P. e TROTSCHENKO A. T.. Biochìmila, 1, 165, 1936 – (33) SCHENCK O., FROEMMING K. H.. WIECHULA W. e SCHWALB E., Arch. pharm., 293, 312, 1960 – (34) WINCKLER, Buchn. Reperì. Pharm., 9, 1, 1837; WEHMER C, Die Pflanzenslofle, II ed., p. 384 – (35) HESSE O-, Ber., 3. 637, 1870- (36) PERROT E., Matières Usuelles du Règne Végélal, Paris, 1944-1955, pp. 880-881 – (37) SATYANARAYANA M. N.. LAKSHMINARAYAN RAO M. V., SRINIVASAN M. e SUBRAHMANYAN V.. J. Sci. ìnd. Research (India), J5C, 211, 1956; Chem. Abs., 51. 3924 c, 1957 – (38) WEHMER C., Pflanzenstoffc. II cd„ p. 382 – (39) KOPP E.. Pharmazie, 15, 4a I960 – (40) KARRER P. e SCHMID H., Helv. Chim. Acta. 28, 722, 1945 – (41) KARRER P. e SCHMID H., Neh. Chim. Acta. 28. 1187, 1945 – (42) LERCH J. U.. Lieb. Ann.. 57. 273, 1846 – (43) BURES E. e FUCIK S., Chem. Zbi. II, 3926, 1935 – (44) GEORG A.. Arch. Sci. 7, 52. 1954; Chem. Abs., 49, 8324 c, 1955 – (45) GUENTHER E., HEEGER E. F. e ROSENTHAL C.. Pharmazie, 7, 29. 1952.

