Se hai un abbonamento attivo ACCEDI QUI
Chelidonia
Tratto da “Piante Medicinali – Chimica, Farmacologia e Terapa” di R. Benigni, C. Capra e P.F.Cattorini
(Chelidonium majus L. – Fam. Papaveracee/Papaveroidee /Chelidoniee) N.B. – Il Chelidonium minus o Celidonia minore è la Ficaria verna Huds.
(sin. Ranunculus Ficaria L. – Ficaria ranunculoides Roth, delle Ranunculacee, il Favagello, che non ha alcuna analogia nè di classe, nè di famiglia)
Chelidonia- Ultimo aggiornamento pagina: 27/02/2018
Indice dei contenuti
- Generalità
- Componenti principali
- Proprietà farmacologiche
- Estratti e preparati vari
- Preparazioni usuali e Formule
- Bibliografia
Generalità

Etimologia – Chelidonium, dal greco celidon = rondinella, perchè si credeva che la rondine si servisse del latice di questa pianta per rafforzare la vista ai nidiacei (da ciò l’antico nome di Hirundinaria major Lobel). Ma è più verosimile che derivi dal fiorire di questa pianta al ritorno delle rondini. Il vocabolo greco corrisponde forse anche all’arabo khard-doun = succo-giallo.
majus – dal latino: comparativo neutro di magnus = più grande.
Nome volgare – Irundinaria, Cinerognola, Erba dei porti, ecc.
Habitat – Tutta l’Europa, Asia settentrionale (Siberia), America del Nord. Pianta erbacea bienne o perenne.
Parti usate – Le parti aeree.
Componenti principali
Alcaloidi: a-omochelidonina, C21H23O5N (1) (2) (3), cheleritrina, C21H17O4N-H2O (2) (3) (4), chelidonina C20H19O5N (5) (6), sanguinarina (j-cheleritrina) C20H13O4N-H2O (6) (7) (8) ed
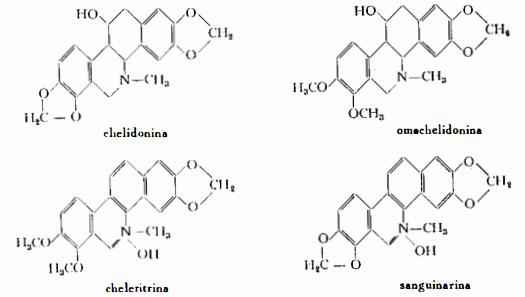
i meno importanti ossichelidonina C20H17O6N (9), metossichelidonina C21H21O6N (9) e ossisanguinarina C20H13O5N ( 10), a- e b-allocriptopina C21H23O5N (11), protopina C20H19O5N (12), coptisina C19H15O5N (13) (14), dl-tetraidrocoptisina (= dl-stilopina) C19H17O4N (15), l-tetraidrocoptisina (= l-stilopina) (15) C19H17O4N (15). Inoltre berberina (16) e sparteina (17).
Gli alcaloidi chelidonina omochelidonina, cheleritrina, sanguinarina, ossichelidonina, metossi-chelidonina e ossi-sanguinarina appartengono al gruppo della naftofenantrina; la a- e b-allocriptopina e la protopina al gruppo della protopina; la coptisina e la tetraidrocoptisina al gruppo delle protoberberine.
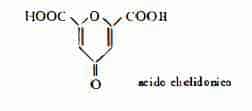
Il contenuto di alcaloidi [0,48-1,04% (18)] nella Chelidonia aumenta sino al termine della crescita della pianta ed è maggiore nelle radici rispetto alle altre parti della pianta stessa (18) (19): nelle radici da 0,61 % a 1.195 %, nelle foglie da 0,11 % a 0,255 % di alcaloidi (19). Si trova inoltre acido ascorbico, il cui titolo più elevato è stato trovato nelle foghe (834 mg %) durante il periodo di fioritura ed il più basso (241 mg % ) durante il periodo della caduta dei frutti (18). Altri componenti: un flavonolo non identificato (20), acido chelidonico (= acido g-pirondicarbonico) (21) (22), resina (23), olio etereo (0,0127 % nelle parti erbacee) (24), una saponina neutra debolmente emolitica (24a).
Proprietà farmacologiche ed impiego terapeutico
La Chelidonia è una delle piante medicinali di antichissimo uso popolare, ma fu soltanto nel secolo scorso (1818) che venne eseguito dall’Orfila (25) uno studio farmacologico vero e proprio su questa droga. Risultò da tale studio che un preparato ottenuto dalla droga in toto (contenente quindi tutte le sostanze che entrano nel suo fitocomplesso attivo) manifestava nei cani cui veniva somministrato, un’azione caratterizzata da nausea o vomito per le dosi più elevate, da ottundimento della sensibilità sino all’anestesia, da difficoltà di movimento, da iperemia della mucosa gastrica e bronchiale.
Successivamente il Ley (26) studiò l’azione della chelidonina, notando un certo parallelismo fra l’azione di questo alcaloide e quella della morfina. Secondo l’A. la chelidonina agirebbe sui centri nervosi superiori con narcosi ma senza riduzione dei riflessi, ottundimento della sensibilità e anestesia che l’A. attribuì a paralisi delle terminazioni nervose periferiche, poiché l’eccitabilità dei centri midollari non veniva alterata. Sarebbero sufficienti poche gocce di una soluzione al 5 % di chelidonina per provocare, secondo l’A, anestesia della cornea con fenomeni irritativi locali e bradicardia. Negli animali a sangue freddo la chelidonina determinerebbe una paralisi simile a quella dovuta alla morfina, non preceduta da una fase di eccitazione.
Il Meyer (27) riprese due anni dopo, lo studio della chelidonina e i risultati da lui ottenuti confermano in linea di massima, quelli emersi dalle ricerche del Ley,
Il Meyer oltre l’azione farmacologica della chelidonina, studiò anche quella della sanguinarina e della cheleritrina. La sanguinarina, secondo l’A., sarebbe un attivo eccitante dei centri midollari. Nella rana dà luogo a contrazioni stricnosimili, alle quali segue, per le dosi più elevate, completa paralisi. Anche i centri bulbari respiratorio e vasomotore, vengono eccitati dalla sanguinarina con conseguente aumento della pressione arteriosa che, per dosi tossiche, subisce un notevole abbassamento. Anche la salivazione e la peristalsi intestinale verrebbero eccitate. A dosi tossiche la sanguinarina è un veleno per i muscoli volontari e, applicata localmente, produce irritazione seguita da anestesia locale: Secondo Little (28) la sanguinarina sarebbe dotata di un’azioné carioclasica analoga a quella dovuta alla colchicina.
La cheleritrina, sugli animali a sangue caldo e a sangue freddo agisce paralizzando i centri respiratorio, vasomotore e cardiaco ed eccitando le terminazioni nervose sensitive.
Analogamente il Tonton (29) trovò che la cheleritrina applicata localmente sulla cute vi esplica un’azione irritante e flogogena. L’a-omochelidonina e la b-omochelidonina, sono ambedue dotate di una debole azione narcotica e manifestano sul cuore una tossicità inferiore a quella della chelidonina. La b-omochelidonina è dotata di una notevole attività anestetica locale ed è esente dall’azione irritante caratteristica della sanguinarina. L’a-omochelidonina sarebbe sotto questo aspetto, meno attiva (30).
Secondo Lewin (31) le piccole dosi di preparati di Chelidonia, provocherebbero nausee e disturbi gastrici.
L’Hanzlich (32) mise in evidenza le analogie chimico-farmacologiche esistenti fra chelidonina e papaverina. La chelidonina agisce infatti diminuendo il tono dei muscoli lisci dell’intestino, dell’utero, dei bronchi dei vasi ecc. e per ciò l’A. ne consiglia l’impiego nella terapia dell’angina pectoris, dell’asma e, soprattutto, come antispastico.
Anche l’Alkan (33) e Schmaltz e Daniel (34) riconoscono alla chelidonina un’azione antispastica, ma inesatto appare l’accostamento che ne fanno all’azione dell’atropina poiché, mentre l’azione di questa si manifesta paralizzando gli accettori colinergici, la chelidonina agisce mediante un punto d’attacco muscolare e quindi essenzialmente diverso.
Il Kreitmair (35) studiò l’azione di estratti di Chelidonia su rane, topi e ratti ed osservò che essi determinano lieve ottundimento del sensorio ma non narcosi pronunciata, azione antispastica sui muscoli bronchiali, azione ipotonica sull’intestino tenue e aumento delle contrazioni dell’utero; inoltre, attivazione della funzione cardiaca, aumento della pressione arteriosa e dilatazione delle coronarie. La frazione dell’estratto esente, da alcaloidi, dimostrò di essere dotata di un’azione ipoglicemizzante, sia se somministrata per via parenterale che per os e, secondo l’A., a questa frazione sembrerebbe doversi attribuire anche l’azione cardiovascolare.
Il Seel (36) studiò comparativamente l’azione della chelidonina e degli estratti totali (fluidi e secchi) di Chelidonia. Sul cuore isolato di rana la chelidonina, alla dose di mg 0,05 (minima attiva), aumenta l’attività cardiaca e sulla rana preparata secondo Trendelenburg, agisce determinando una vasocostrizione, azione questa che tuttavia, risultò inferiore a quella ottenuta con soluzioni di estratto secco.
L’utero isolato di rana reagisce all’estratto secco di Chelidonia con una contrazione durevole, mentre la chelidonina provoca una reazione del tutto opposta. Sull’intestino tenue di ratto, tanto l’estratto secco quanto la chelidonina, manifestano un’azione ipertonizzante, mentre su segmenti di intestino crasso la chelidonina determina una diminuzione del tono e l’estratto secco, un’azione paralizzante.
Con altre ricerche gli stessi AA. dimostrarono che sul cane cui era stata praticata una fistola biliare, gli estratti di Chelidonia aumentano la secrezione biliare.
Powell e Chen (37) hanno studiato l’azione farmacologica della cheleritrina e trovarono che essa abbassa, nel gatto e nel cane, la pressione arteriosa, abbassamento che si manifesta dopo un transitorio aumento iniziale. L’aumento dell’ampiezza e della frequenza respiratoria è invece preceduto da un breve periodo di blocco respiratorio.
L’attività motoria dell’intestino e dell’utero isolati di coniglio e di cavia, viene stimolata dalla cheleritrina, ma le dosi ripetute si dimostrano meno attive. Somministrata endovena, la cheleritrina provoca una secrezione oculare acquosa chiara, nei ratti ed in altri roditori (criceti).
Azione batteriostatica
L’azione batteriostatica degli estratti di Chelidonia fu osservata dallo Stikl (38) e dal Daniel (39) su culture di Str. viridans, di Str. Hemolyticus e di stafilococchi.
De Franciscis e Aufiero (40) sperimentarono estratti acquosi di Chelidonia su cavie infettate con bacillo di Kock e trovarono che mentre il periodo medio di sopravvivenza delle cavie non trattate si aggirava intorno ai 60 giorni, quello delle cavie trattate con estratto di Chelidonia raggiungevano i 129 giorni.
Da ricerche eseguite presso il nostro laboratorio dalla Mela (41) risulta che gli estratti di Chelidonia manifestano una marcata attività batteriostatica su colture di E. Coli, di Staph. aureus, di Staph. album, di Staph. di Oxford, di Diploc. Vitelli, di Strept. Vitelli e di B. Anthracis.
Secondo Bersch e Dopp (42) gli alcaloidi della Chelidonia non avrebbero che una debole attività tubercolostatica in vitro e sarebbe poco probabile, secondo questi AA., che i buoni risultati ottenuti da alcuni Autori con l’impiego di questi alcaloidi, siano dovuti a tubercolostasi.
Alkiewiez e Coll, (43) riferiscono sul notevole effetto micostatico di estratti, freschi e di decotti di Chelidonia, sul Trichophyton, crateriforme, sul Tricophyton gysepseum e sull’Epidermophyton Kaufmann Wolf. Fatto interessante notato dagli AA. è che gli alcaolidi chelidonina, cheleretrina e sanguinarina, presenti nelle preparazioni usate dagli AA. per le loro ricerche, non possiedono tale attività.
Il Bodalski e la Rzadkowska (44) sperimentarono l’effetto tossico del lattice di Chelidonia sugli infusori e trovarono che tale azione tossica è dovuta agli alcaolidi chelidonina, cheleritrina e sanguinarina che furono sperimentati sotto forma dei loro cloridrati. Il cloridrato di sanguinarina si è dimostrato il più tossico sugli infusori i quali son distrutti in 7’ con una soluzione all’1:5000, mentre soluzioni all’1:10.000 inibiscono i movimenti lineari e rotatori in 10-15′.
Bel’tyukova (51) ha sperimentato 55 sostanze sintetiche costituite da diversi esteri dell’acido tiosulfonico, analoghe alla pseudoallicina e alcune sostanze derivate da piante superiori fra le quali l’omochelidonina, trovando che tutte arrestano la proliferazione di batteri fitopatogeni a diluizioni comprese fra 1:1000 e 1:1.000.000. Tale azione antibatterica sarebbe caratterizzata da una notevole selettività e, in generale, risulterebbe essere batteriostatica e battericida.
Più recentemente Dobrot’ko e coll. (52) sperimentarono una preparazione ottenuta dalla Chelidonia, contenente gli alcaloidi grezzi cheleritrina e omochelidonina, trovando che essa inibisce la crescita dei germi gram-positivi in vitro.
Azione antiblastica
Questa azione venne notata sin dal 1896 dal Denissenko (45) il quale riferì di aver osservato la regressione parziale o totale di epiteliomi, seguire al trattamento orale o parenterale con preparati di Chelidonia.
In senso ugualmente favorevole si espressero altri AA. [Robinson (46), Andrew (47)] ma ulteriori ricerche di Schoemaker, di Winter e di Freudenberger (48) sembrerebbero dimostrare che i preparati di Chelidonia non abbiano alcuna azione specifica sui carcinomi, pur riuscendo a migliorare le caratteristiche dei secreti e a limitare le emorragie. Più recentemente lo Stikl (49) affermò che gli alcaloidi della Chelidonia possono rallentare l’accrescimento dei carcinomi sperimentali del topo e influenzarne favorevolmente il decorso.
Che un’azione di questo tipo possa essere attribuita agli alcaloidi della Chelidonia, potrebbe essere provato dai risultati delle già citate ricerche del Little (28) a proposito dell’azione colchicinosimile della sanguinarina.
Impiego terapeutico
I preparati di Chelidonia sono indicati, secondo Daniel (39) nella terapia di alcune malattie del fegato e delle vie biliari, quali l’ittero catarrale e l’ittero infettivo di Weil, nelle colecistopatie, nella colelitiasi, nella cirrosi epatica iniziale, nelle epatopatie, negli stati susseguenti a colecistectomia, nella gastroenterite e nel tenesmo vescicale. Il Wetter (50) che ha estesamente sperimentato l’attività terapeutica dei preparati di Chelidonia, annovera fra le principali indicazioni, le affezioni croniche dello stomaco, dell’intestino e del fegato. Attualmente i preparati di Chelidonia vengono impiegati soprattutto come spasmolitici nelle malattie del fegato e delle vie biliari e molto spesso in associazione con altre droghe ad azione coleretica e colagoga, quali il Carciofo, il Boldo, la Curcuma, il Combretum, il Tarassaco ecc.
Estratti e preparati vari
a) Estratto fluido per tintura (g 1 = LIII gtt).
Dosi: g 0.5-2 pro die. ‘
b) Estratto fluido per sciroppo (g 1 = XXXV gtt).
Dosi: come sopra.
c) Estratto secco acquoso (1 parte = 7 p. circa di droga).
Dosi: g 0,07-0.3 pro die.
Preparazioni usuali e formule galeniche
Tintura
Estratto fluido chelidonia per tintura g 20
Alcool di 60° g 80
(2-3 g pro die)
Sciroppo
Estratto fluido chelidonia per sciroppo g 2,5
Sciroppo semplice F. U. q. b. a g 100
(a cucchiaini nei disturbi epato-biliari)
Pozione nelle epatiti
Estratto fluido chelidonia per sciroppo g 50
Estratto fluido cascara sagrada per sciroppo g 20
Sciroppo menta…………………………. g 60
Acqua……………………………………….. g 300
(a cucchiaini)
BIBLIOGRAFIA
(1) SCHMIDT e SELLE, Areh, Pharm,, 228, 441» 1890 – (2) GAPAMER. Areh. Pharm., 257, 298, 1919; 258, 160» 1920 – (3) SPÀTH e KUFFNER» Ber., 64, 1123» 1931 – (4) PROBST Ann. Pharm., 29, 113, 1839 â–º (5) BRUCHHAUSEN e BERSCH» Ber., 63, 2520, 1930; 64, 947, 1931 – (6) SPÀTH e KUFFNER, Ber., 64, 370» 1931 – a) SCHMIDT, Arch. Pharm., 239, 405. 397» 1901 – (8) SPÀTH e KUFFNER, Ber., 64, 2034, 1931 – (9) GADAMER e THEYSSEN» Arch. Pharm., 257, 298» 1919 – (10) SPÀTH e colL, Ber., 70, 1677, 1937 – (II) GADAMER. DIETERLE, STICHEL, THEYSSEN e WINTERFELD, Arch. Pharm., 262, 249, 1924 â– (12) WINTGEN, Arch. Pharm., 239, 438, 1901 – (13) ARWE, Arznelm.-Forsch., 2. Ì87, 1951 –
(14) SPÀTH e POSEGA, Ber., 62. 1029, 1929 – (15) JIRI SLAVIK, Chem. U.uy, 48, 1382 c 1557, 1954; Chem’. Abs., 49, 10986 1 e 11673 b, 1955 – (16) GADAMER, Apoth. Zeii, 39, 1569, 1924 – (17) SPÀTH e KUFFNER, Ber., 64, 1127, 1931 – (18) SIMM Kh. A., Izvest. Akad. Nauk, Eston. S.S.R., 1954, n. 3, 435; Chem. Abs., 50. 5989 b. 1956 – (19) KRELL G., Diss. Mùnch., 1937 – (20) KWASNIEWSKI V., Arzneim.- Forsch., 8. 245, 1958 – (21) KWASNIEWSKI V,, Arznelm.-Forsch., 5. 90, 1955 – (22) RAMSTAD E.. Pharm, Aera Nelv.. 28. 45, 1953 – (23) GADAMER, MEYER e NEUGEBAUER, dt, da BERGER F.. Handbruch der Drogenkunde, IV, Wlen, 1954, p. 128 – (24) HAUSEL, AporA. Ztf,. 23,119, 1908-(24a) KWASNIEWSKI V., Arch, Pharm,. 291/63, 209, 1958 – (25) ORFILA, Aììey Toxìkoìogìc, 3, 72, 1818 – (26) LEY C., Dìssert, Vnlvers. Marburg 1890 – (27) MEYER H, Arch. f. exp. Path, u. PharmakoL. 29, 397 e 420. 1892 – (28) LIITLE, Science, 21 agosto 1942 – (29) TONTON, Beìtrag. Bìoì. Pfiam, 19, 1, 1931 – (30) STARKESTEIN, Heffter-Heubner, Handbuch d. exp. Pharmakoi v, 2“, p. 1098 – (31) LEWIN» Neben Wlrkungen d. Arznel- mluel, 1899 – (32) HANZLICH P. J.. /. of Pharmacot. a. exp. Therap,, 7. 99. 1915 e 75. 63, 1921 – (33) ALKAN L., Arch. Verdauungs-Krankh., 43, 46. 1928 – (34) SCHMALTZ D. e DANIEL K., Pharmaz- Zentraìh.. n. 48, 738, 1936 – ()5) KREITMAIR H., Jahresber. Merck, 50, 114, 1936 – (36) SEEL H. e coll, Hippokrates. 50. 1281-87, 1939 – (37) POWEL C. E. e CHEN K. K., J.A.Ph.A., 44. 4, 196, 1955 – (38) STIKL O., Ztschr. ì. nygìene m. InUktìonskht.. WS. 567, 1928 – (39) DANIEL K„ Dar Schóllkralut. Stuttgart 1939 (40) DE FRANCISCIS P. e AUFIERO C.. Boti. Soc. It. Bioi Sper., 25. 1. 1949 – (41) MELA C.. Fltote rapia. n, 2, 1950 – (42) BERSCH H. W. c DOPP W., Arznelmlttel-Forsch.. 5. 2» 77-78. 1955 – (43) ALKIE WIEZ e coll., Zbi. Haut. Geschi. Krank.. 91, 7, 379, 1955 – (44) BODALSKI T. e RZADKOWSKA H., Med. Acad. Wrociaw. Poland.. 9, 266-71, 1957 – (45) DENISSENKO, Vrach. Petersburg 1896» cU. da MADAUS in Lehrbuch der Blologlschen Hellmlttel. voi. 2**» p. 920; Leipzig 1938 – (46) ROBINSON, Bit/l. de la Soc. ThérapeullQùe, 1896 – (47) ANDREW, J.A.M.A., 1897 – (48) Citati da LECLERC: Preda de Phyloher , p. 225, Pairgi 1935 – (49) STIKL, Wirchows Arch. Path. Anatom., 270, 3. 1929 – (50) WEITER O.» Pianta Medica. 3, 33. 1955 – (51) BEL’TYUKOVA K. L, Izbrannye Dokay 2-go Soveshchanpo Probleme Fltontsidov. Lenìngrad. Gosudarst. Unlv. im. A.A. Zhdanova, Kiew^ 10^18, 1956; Chem. Abs,, 53, 82281, 1959 – (52) DOBROT’KO V. G., RASHBA E. Ya., AIZENMA B. E.. ZELEPUKHA S. I.. NOVIKOVA S. I. e KAGANSKAYA B. M.. Antlblotikl, 22-30, 1958; Chem, Abs., 53. 13» 12589d» 1959.

