Gelsemio
Tratto da “Piante Medicinali – Chimica, Farmacologia e Terapa” di R. Benigni, C. Capra e P.F.Cattorini
(Gelsemium sempervirens (L.) Persoon, Ait. – Fam. Loganiacee/Gelsemiee) (Sin. – Gelsemium nitidum Michaux.)
Gelsemio- Ultimo aggiornamento pagina: 27/02/2018
Indice dei contenuti
- Generalità
- Componenti principali
- Proprietà farmacologiche
- Estratti e preparati vari
- Preparazioni usuali e Formule
- Bibliografia
Generalità

Etimologia – Gelsemium, da Gelseminum (Jasminum) dal greco eusmos = odorifero o derivante dall'ebraico Samin = profumo, arabo = jsmjn, perchè i fiori del Gelsomino hanno grato odore e profumano i luoghi dove la pianta vegeta.
sempervirens, per le foglie sempre verdi, persistenti.
nitidum, idem (lucente).
Nome volgare – Yellow Jasmine, Evening Trumpet, Gelsomino della Carolina.
Habitat – America del nord, Virginia, Florida, Texas, Messico, America centrale, Carolina.
Parti usate – Rizoma e radici.
Componenti principali
0,5 % circa di alcaloidi: gelsemina, sempervirina, gelsemicina, gelsedina e gelseverina.
La gelsemina fu isolata in forma cristallina da Gerrard nel 1883 (1), mentre un principio alcaloidico amorfo era già stato estratto sin dal 1870 da Wormley (2). La formula centesimale attualmente accettata è la, C20H22O2N2, stabilita da Moore (3), mentre la formula di struttura non è stata sinora definita. Gli schemi, con cui è stata rappresentata, Sono tuttora in discussione (4) (5) (6) (7) (8). Attualmente si raffigura secondo la seguente formula (4):
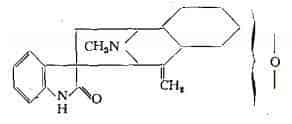
La sempervirina, isolata in forma cristallina da Sayre e Stevenson (9) ed identificata da Hasenfratz (10) alla sempervina ottenuta da Chou (11), ha la composizione centesimale C19H16N2 (10). Si tratta di un alcaloide appartenente al gruppo dell'indolo, la cui struttura chimica è stata formulata in base ai più recenti studi di Goutarel, Janot e Prelog (12) (13), di Edwards e Marion (14) e di Woodward e coll. (15) (16). Sono state proposte le seguenti due formule in equilibrio:
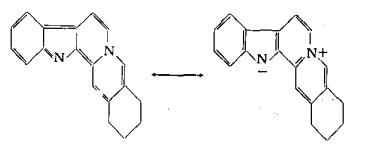
La gelsemicina, ottenuta da Chou (11), presenta caratteristiche chimiche e fisiche che rispondono a quelle degli alcaloidi indolici. La formula grezza di Chou (11), C20H25O4N2, è stata modificata in C20H26O4N2 (17) (18).
La gelsedina, C19H24O3N2, è stata identificata in un primo tempo alla gelsemicina (19), ma fu poi riconosciuta come nuovo alcaloide (20). La struttura parziale nota la indica quale derivato del N-metil-a-ossi-indolo.
La gelseverina, C21H24O3N2 oppure C21H26O8N2, con struttura chimica sinora non chiarita, è stata isolata da Schwarz e Marion (20).
Con il nome di gelsemina spesso si denomina in commercio la gelseminina, prodotto alcaloidico del Gelsemio, non definito, che dà sali non cristallizzabili. E’ da notarsi che con il nome di gelsemina sono stati indicati anche alcaloidi amorfi (21) (22), probabilmente miscele di diversi alcaloidi.
Dal Gelsemio, oltre agli alcaloidi, sono stati estratti resina 3,8%, olio etereo 0,5%, un fitosterolo (ipuranolo) (22), olio grasso 7,4% nelle radici, 5,6% nei rizomi (23) e scopoletina (etere metilico della esculetina), identificata all'acido gelsemico dai precedenti ricercatori (22) (24).
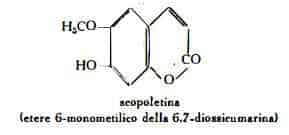
Nell'estratto fluido del Gelsemium sempervirens (L.) Ait., Uhlenbroock e coll. (25) hanno rilevato la presenza di sostanze fenoliche (b-naftolo, pirogallolo, resorcina, idrochinone) e di purine (adenina e guanina).
Proprietà farmacologiche ed impiego terapeutico
Il Gelsemio venne coltivato per la prima volta in Europa agli inizi del 1600, epoca in cui il Tradescant (26) recò in Inghilterra i semi della pianta dal Messico.
Ma è soltanto alla metà del secolo scorso che si può far risalire il primo impiego terapeutico della radice di Gelsemio, che nel 1860 venne inscritta nella «Secondary Lyst» della Farmacopea americana.
L'azione dei preparati di Gelsemio (estr. fluido, tintura) si manifesta principalmente sul sistema nervoso centrale e, in particolare, sui centri midollari che vengono inizialmente stimolati, poi depressi.
Negli animali superiori prevale l'azione deprimente sui centri cerebrali mentre questa sarebbe meno marcata sui centri spinali. Le piccole dosi, secondo Cohen (27) deprimono il tono vagale con conseguente aumento della frequenza cardiaca ma senza rilevanti ripercussioni sulla curva emodinamica. Le forti dosi deprimono notevolmente l'attività cardiaca con effetti inotropi e cronotropi negativi. La pressione ematica viene notevolmente abbassata sia per un’azione depressiva cardiaca che per un ottundimento dell'eccitabilità dei centri vasomotori. Alla somministrazione di dosi letali consegue fibrillazione, paralisi quasi completa e arresto respiratorio.
L’azione degli estratti di Gelsemio sui muscoli lisci è stata studiata da Uhlenbroock e coll. (25) sulla vescicola seminale di cavia, valutandone l’effetto adrenolitico comparativamente con il tartrato di ergotamina. Dai tali ricerche risultò intanto, che l'attività farmacologica dell'estratto totale non è dovuta soltanto agli alcaloidi, ma anche alle sostanze fenoliche e puriniche contenute nella droga e che l’estratto totale sarebbe) più attivo dei singoli alcaloidi isolatamente considerati e fatti agire alla stessa concentrazione in cui si trovano nella droga.
L’azione spasmolitica sulla vescicola seminale di cavia, capace di antagonizzare l’effetto adrenalinico, sarebbe piuttosto debole.
I fenoli e le purine agirebbero quanitativamente in maniera diversa fra i fenoli, il b-naftolo, alle concentrazioni sperimentate, è risultato inattivo e debolmente attivo è risultato l’idrochinone. La resorcina e il pirogallolo hanno manifestato invece una netta attività.
Fra le purine, l’adenina è risultata la più attiva; la guanina, sotto forma di cloridrato, sarebbe inattiva.
Tanto l’azione del Gelsemio quanto quella dei suoi principi attivi; è reversibile dopo lavaggio.
Al Gelsemio venne attribuita da diversi AA. [Klemperer e Rost (28), Heffter e Heubner (29), Reko (30)] un’azione analgesica per la quale si hanno però scarse e incomplete dimostrazioni sperimentali.
Sulla tossicità dei preparati totali di Gelsemio e degli alcaloidi isolati si hanno dati molto contradditori. I campioni di gelsemina sperimentati dai diversi AA. differivano infatti per caratteristiche chimiche e quindi anche biologiche. Eichler e coll. (31) hanno sperimentato la tossicità di tre campioni di gelsemina ed hanno trovato per il I (p.f. 175°), una DL50 pari a 49 mg/Kg nel topo per via ipodermica; per il II (p.f. 162-163°), una DL50 pari a 343 mg/Kg e per il III (p.f. 164°), una DL50 pari a 300 mg/Kg circa. Secondo alcuni AA. [Cushny (32), Dixon (33), Risi
(34), Schindler (35)] la gelsemina sarebbe dotata di una tossicità molto debole mentre la gelsemicina risulterebbe altamente tossica. Alcuni AA. ritengono anzi che l’attività della gelsemina sarebbe in parte dovuta ad impurezze costituite probabilmente da gelsemicina [Schindler, Marion (36)]. Ciò non sarebbe in accordo però con i risultati ottenuti da Eichler e coll, i quali trovarono invece che il campione di gelsemina a più elevato punto di fusione e quindi più puro, era anche il più attivo.
L'azione della gelsemina è qualitativamente simile a quella della gelsemicina, ma quantitativamente più debole ed è dotata di un'azione deprimente cardiaca che sembra mancare alla gelsemicina [Chou (37)]. Raymond-Hamet (38) trovò che la gelsemina paralizza le terminazioni periferiche vagali e che, analogamente alla sparteina, è capace di sensibilizzare gli animali all'azione adrenalinica.
Sull'intestino isolato di cavia la gelsemina determina un arresto delle contrazioni peristaltiche mentre le contrazioni di segmenti isolati di utero, verrebbero eccitate [Henderson e Chen (39)].
La DL50 per via endovenosa, determinata dagli stessi AA. nel topo, corrisponderebbe a 4 mg/Kg per la gelsemina (cloridrato).
Per quanto riguarda l'azione analgesica, per la quale i preparati di Gelsemio e la gelsemina trovano qualche applicazione terapeutica, è stata studiata da Eichler e coll. (31) col metodo della stimolazione elettrica delle terminazioni nervose degli incisivi di coniglio, proposto da Fleisch e Dolivo (40) ed estesamente descritto da Hertle e coll. (41). Secondo i risultati ottenuti dai suddetti AA., confermati statisticamente e con prove in bianco, la gelsemina somministrata oralmente e per via endoperitoneale, sarebbe dotata di una marcata azione analgesica anche a dosi inferiori a quelle capaci di provocare fenomeni di tossicità acuta. I campioni di gelsemina di diversa provenienza, studiati dagli AA., hanno dimostrato di possedere un'attività uguale qualitativamente ma quantitativamente diversa. Anche l'azione della tintura di Gelsemio differirebbe da quella dell'alcaloide isolato.
Risultati analgesici più favorevoli sono stati ottenuti dagli AA. con l'associazione di salicilamide e fenacetina, con gelsemina la quale ultima avrebbe dimostrato, nelle condizioni sperimentali suddette ed entro certi limiti di dosaggio, un'azione anche superiore a quella della morfina.
Sul sistema nervoso vegetativo la gelsemina sembrerebbe agire in maniera simile a quella dell'atropina.
Raymond-Hamet (42) ha infatti potuto constatare che la gelsemina, nei cani, alla dose di 48 mg/Kg inverte l'azione dell’acetilcolina sul cuore e sulla pressione arteriosa, nonché gli effetti cardioinibitori della stimolazione elettrica del moncone periferico del vago. La risposta pressoria all'azione della nicotina non verrebbe invece abolita (Linegar e coll. (43)].
Sul cuore isolato di rana la gelsemina determina un effetto depressivo che sarebbe antagonizzato dal bario e dall'adrenalina, ma non dall'atropina [Moisset de Espanes (44)].
La deidrogelsemina preparata per riduzione catalitica della gelsemina è dotata della stessa azione farmacologica, quali- e quantitativa, della gelsemina.
La frazione alcaloidica denominata gelsemoidina è stata poco studiata. Secondo Christensen e Gramling (45) sarebbe dotata di un'azione emetica.
Una seconda frazione alcaloidica denominata gelsemidina, secondo gli stessi AA., sarebbe invece priva di questa azione.
La gelsemicina sembrerebbe essere il principio attivo più importante del Gelsemio; la sua azione verrebbe tuttavia modificata nella droga, dalla presenza degli altri alcaloidi (37). La dose letale per il ratto è di circa 0,06 mg/Kg e la morte avverrebbe più per paralisi dei centri motori cardiaci che per azione sul centro respiratorio bulbare (46),
La sempervirina sul cane cloralosato e bivagotomizzato, annulla secondo Raymond-Hamet (47), l’effetto dell'eccitazione elettrica del moncone periferico, rinforza l’azione ipertensiva dell'adrenalina e ne prolunga gli effetti inibitori sull’intestino.
Sui vasi dell'orecchio di coniglio manifesta un’azione vasocostrittrice [Rothlin-Raymond-Hamet (48)], diminuisce gli effetti dell’acetilcolina e dell'adrenalina nella vescicola seminale (49) e sull’intestino di cavia (50).
Vincent e Lagreu (51) trovarono che la sempervirina è dotata di una intensa attività sulla colinesterasi la quale verrebbe inibita totalmente alla concentrazione di 10-4 M. e nelle proporzioni del 50 % alla concentrazione 10-6 M. sul siero.
La gelsemina e la gelsemicina sarebbero dotate di un’attività inferiore di 200-500 volte e la colinesterasi nervosa sarebbe meno sensibile all'azione della sempervirina di quella del siero. L'azione anticolinesterasica della tintura di Gelsemio sarebbe proporzionale al suo contenuto di sempervirina e la presenza in essa di gelsemina non aggiungerebbe che un effetto proporzionalmente molto debole.
Il fatto che questa attività colinesterasica notata da Vincent e Lagreu, tenda ad avvicinare l'azione della sempervirina a quella dell'eserina, ciò che non si accorderebbe coi risultati ottenuti dagli AA. precedentemente citati, ha indotto il Le Hir (52) a riprendere l’argomento ed a studiare gli effetti di quest'alcaloide sul sistema nervoso autonomo e cardiovascolare.
Le esperienze sono state eseguite sul cane cloralosato, bivatogotomizzato e in respirazione artificiale.
Contrariamente a quanto osservato da Raymond-Hamet, il Le Hir trova che l'effetto ipertensivo dell'adrenalina è poco modificato o addirittura diminuito, anziché potenziato, dall'azione della sempervirina e ritiene che l’azione di questa derivi da un effetto sinaptolitico parasimpatico, inibitore sui centri vasocostrittori simpatici e da un potenziamento dell'effetto muscarinico dell’acetilcolina. Il Le Hir spiega l'azione potenziante dell'effetto adrenalinico sulla pressione, ammettendo la probabilità che in certi animali, in cui il tono vagale é fisiologicamente elevato, la soppressione della bradicardia riflessa adrenalinica, sia sufficiente ad indurre, un aumento dell'ipertensione.
Impiego terapeutico – L’estratto fluido di Gelsemio alla dose di 1-2 gocce é impiegato nelle nevralgie in generale e particolarmente in quella del trigemino, nelle cefalgie nervose, nell’ipertensione cerebrale e nell’isterismo: occorre ricordare però che non tutte queste applicazioni sono fondate su di una sicura base farmacologica.
I preparati di Gelsemio istillati nell’occhio determinano midriasi, accompagnata però da forte irritazione [Sollmann (53)].
Holman (54) usa, come antispastico, la tintura di Gelsemio nel trattamento dei postumi della poliomielite, somministrandola ogni due ore, durante il giorno e la notte e in dose sufficiente a mantenere un elevato livello terapeutico. La durata del trattamento ha raramente superato i 12-14 giorni, durante i quali il paziente era sottoposto a stretta sorveglianza, sia per regolare il dosaggio in base alle modificaizioni respiratorie, sia per rilevare prontamente eventuali sintomi di intossicazione che non raramente si verificano, essendo il coefficiente terapeutico dei preparati di Gelsemio piuttosto basso.
L’A. afferma che la droga è efficace se la diagnosi può essere fatta precocemente e prima che il sistema nervoso subisca danni irreversibili.
Tossicologia – Anche piccole dosi di Gelsemio possono dar luogo ad effetti tossici che a volte si manifestano non immediatamente ma dopo un certo periodo di latenza. Fra i segni di avvertimento sono da annoverarsi la ptosi palpebrale, la midriasi, l'ambliopia, l’astenia e la depressione. A dosi più elevate consegue prostrazione generale, riduzione della frequenza del polso e respiratoria. Se lo stato di intossicazione è grave, questi sintomi si intensificano.
Fra i sintomi più caratteristici dell’avvelenamento grave da Gelsemio, sono da annoverarsi la ptosi della mandibola, le manifestazioni oculari e il rilasciamento muscolare generale.
Negli avvelenamenti letali, la morte avviene nello spazio di 2-8 ore per arresto respiratorio. Grammi 3-4 di estratto fluido possono essere sufficienti a provocare un avvelenamento mortale e cc 1,77 possono essere dannosi. Sono stati descritti casi di avvelenamento mortale di bambini per dosi di 0,70 cc di estratto fluido o per 35 gocce di tintura.
La terapia dell’avvelenamento consiste nell’evacuazione dello stomaco e dell'intestino, se l'intervento terapeutico è immediato. Ad assorbimento avvenuto, la terapia è sintomatica. Assoluto riposo in posizione orizzontale, somministrazione di analettici respiratori e cardiovascolari: pel caso di ipotermia, provvedere al riscaldamento esterno del corpo. Se necessario, si pratichi la respirazione artificiale e inalazione di una miscela di ossigeno e anidride carbonica (al 7%). Alcuni AA. consigliano anche atropina alla quale si potrà ricorrere ove il quadro sintomatologico ne indichi la necessità.
Estratti e preparati vari
Estratto fluido (Titolo chimico; 0,5 % di alcaloidi), (g 1 = LIII gtt).
Dosi: I-VI gtt pro die.
Preparazioni usuali e formule galeniche
Tintura
Estratto fluido gelsemio………………………………………. g 10
Alcool di 60° g 90
(X-XX gtt pro dose, sino a LX gtt pro die)
Sciroppo
Tintura di gelsemio……………………………………………. g 5
Glicerina ………………………… ………………………… . . . g 5
Sciroppo semplice F.U. …………………………………… g 90
(1/2-1 cucchiaino pro dose 2-3 volte pro die)
Tintura composta
Tintura gelsemio
Tintura colchico……………………………………………………….. ana g 5
Estratto fluido valeriana per sciroppo………………………. g 20
Alcool di 95° e glicerina………………………………………… ana g 10
Sciroppo semplice F. U. e acqua q. b. a………………….. g 200
(un cucchiaino tre-quattro volte pro die)
BIBLIOGRAFIA
(1) GERHARD A., Pharm. 113, 641.1883; Jahreiber., 1353. 1883 – (2) WORMLEY T. G.. Am. J. Pharm., 42, 1. 1870; Chem. Zbl., 678, 1870 – (3) MOORE C. W„ I. Chem. Soc.. 97. 2223, 1910; 99, 1231, 1911'r (4) GIBSON M. S. e ROBINSON R„ Chem. Ind„ 93. 1951 – (5) GOITrAREL R., JANOT M., PREtOO V., SNEEDEN R. P. A, e TAYLOR W. I,. Helv. Chim. Aera, 34, 1139 e 1963, 1951 – (6) MARION L. e HABGOOD T.. Cari. J. Chem., 33, 604. 1955; Chem. Abs„ 49, 10984 d, 1955 – (7) LOVEIX F. M.;- PEPINSKY P, e WILSON A. J. C.. Tetrahedron Lettere, 1, 1959; Chem. Ab.i., S3, 22033 f, 1959 – (8) CON-, ROY H. e^HAKRABARTI J. K.. Tetrahedron Uttere, 6, 1959; Chem. Abe.. 33, 22033 i, 1959 – (9) SAYRB
L. E. e STEVENSON A, E.. J.A.Ph.A., 4, 60 e 1458, 1915 – (10) HASENFRATZ V., Compt. Read., 196, 1530, 1933 – (11) CHOU T, Q., CMneee J. Phyelol. 5, 131 e 295, 1931 – (12) GOUTAREL R„ JANOT M.
M. e PRELOG V, Experlentia, 4, 24, 1948 – (13) PRELOG V.. Hely. Chim. Aera, 31, 588, 1948 – (14) EDWARDS O. E. e MARION L., 1. Am. Chem. Soc., 71. 1694. 1949 – (15) WOODWARD R. B. e WITKOP B„ ]. Am. Chem. Soc„ 71, 397, 1949 – (16) WOODWARD R. B. e McLAMORE W. M„ /. Am. Chem. Soc., 71, 379, 1949 – (17) FORSYTH N. G. G., MARRIAN S. F. e STEVENS T. S„ 1. Chem. Soc., 579, 1945 – (18) SCHWARZ H. e MARION L., Con. 1. Chem., 31, 958. 1953 – (19) JANOT M.. GOUTAREL R. e FRIEDRICH. Ann. Pharm. Fran(.. 9, 305, 1951 – (20) SCHWARZ H. e MARION L., 1. Am. Chem. Soc., 73, 4372, 1953; Can. J. Chem., 31, 958, 1953; Chem. Abe.. 48, 100281 e 12130 d, 1954 – (21) IHOMPSON, Pham. J„ 17, 805, 1887 – (22) MOORE C. W., 1. Chem. Soc., 97. 2223, 1910; 99. 1231, 1911 – (23) INGHAM, Amer. 1. Parm., 235. 1897 – (24) SCHMIDT E., Arch. Pharm, 236, 324, 1898; SERA R. e KALLER P., Ber.. 64, 909, 1931; FISCHER R. e EHRLICH H., Arch. Pharm, 274, 268, 1936 . (2$) UHLENBROOCK K., SCHWEER M. e MASCHMANN L., Armelm.-Forech., 4, 419, 1959 . (26) TRA- DESCANT, cit. da MERKEL W. IH Pharmacle. ». 4. 349, 1935 – (27) COHEN, C. R. Aead. Sci, 206, 280, 1938 – (28) KLEMPERER e ROST, Handb. Ar>;neivetordo.-Lhete – (29) HEFFTER e HEUBNER, Handb. Bd. 2 Gl, Sprlnger, Berlio 1924; Diaon W, E. aCelsemkima) – (30) REKO V .A„ Deut. Z. serlehti. Med, 21, 9, 1933 – (31) EICHLER O, HERTI.E F. e STAIB J.. Aruteim-Forech., 7, 6. 349-355, 1957 – (32) CUSHNY A. R„ Are*, exp. Path. u. Pharmakol., 31, 49, 1893 – (33) DIXON W. E.. clL da HEFFTER e HEUBNER 1. c. . (34) RISI A., Zelt. Blol, 99, 446. 1939 – (35) SCHINDLER H., cit. da EICHLER e coll. 1. c. – (36) MARION L.. idem – (37) CHOU. Chineee 1. Phyelol., 3, J31, 1931 – (38) RAYMOND- HAMET, C.R. Soc. Blol., 126, 690, 1937 – (39) HENDERSON e CHEN, J.AFh.A., 32, 178, 1943 – (40) FLEISCH A. e DOLIVO M.. Helv. Phyelol. Acia, 11, 305, 1953 – (41) HERTI.E F., SCHANNE G e STAIB J„ Artnelm.-Forech, 7, 311, 1957 – (42) RAYMOND-HAMET, C. R. Soc. Blol, 131, 31-34, 1957 . (43) LINEGAR, KOPPANYI e BARTIMO, Fed. Proc, 2, 86, 1943 – (44) MOISSET DE ESPANES E., C. R. Soc. Blol, 127, 1433, 1938 – (45) CHRISTENSEN e GRAMLING, J.A.Pli.A., 27, 1208, 1938 • (46) CHEN K. K. e CHOU. CHtreee 1. Phyelol, 14, 319, 1939 – (47) RAYMOND-HAMET. C.R. Soe. Blol, 126, 690, 1937 – (48) ROTHLIN E e RAYMOND-HAMET, Ibld, 117, 754, 1934 – (49) ROTHUN E. e RAYMOND-HAMET, lUd, 117, 859. 1934 – (50) ROTHLIN E. e RAYMOND-HAMET, Ibld, 133, 478, 1941 – (51) VINCENT D. e LAGREU R.. Ibld, 143, 348, 1951; Soc. de Pharm. de Toulouee 13 fen- nak) 1952 – (52) LE HIR M. A., Ann. Pharnu Frane, 13, 5, 368-372, 1955 – (53) SOLLMANN W, B., A. Manual ol Pharmacology – Phyladelfia-London 1950 – (54) HOLMAN, lowa Siate M. Soc, 36, 477, 1946.

