Jaborandi
Tratto da “Piante Medicinali – Chimica, Farmacologia e Terapa” di R. Benigni, C. Capra e P.F.Cattorini
(Fam. Rutacee/Cuspariee)
Con questo nome, nell’America del sud, si indicano parecchie piante del genere Pilocarpus.
a) Pilocarpus pinnatifolius Lemaire, detto del Paraguay o di Rio (Paraguay, Brasile s/ovest, Argentina) con la var. selloanus Engler.
b) Pilocarpus Jaborandi Holmes (sin. – Pilocarpus ofìicinalis Pohl) detto di Pernambuco. (Nord e nord/est del Brasile, particolarmente nella regione di Pernambuco). Il primo conosciuto in Europa.
c) Pilocarpus microphyllus Stapf., detto di Maranham, Brasile (Parà, Maranao, Parahyba).
d) Pilocarpus trachylophus Holmes, detto di Cearà (Brasile or.).
e) Pilocarpus spicatus St., Hil., detto di Acarahy (nord/est e sud del Brasile).
f) Pilocarpus racemosus Vahl, detto delle Antille (Cuba, Guadalupa, Martinica) .
La droga da preferirsi è quella ricavata dal Pilocarpus microphyllus Stapf. perchè il contenuto in p.a. è più alto. Buona anche quella ricavata dal Pilocarpus pennatifolius Lemaire e dal Pilocarpus Jaborandi Holmes.
Jaborandi- Ultimo aggiornamento pagina: 27/02/2018
Indice dei contenuti
- Generalità
- Componenti principali
- Proprietà farmacologiche
- Estratti e preparati vari
- Preparazioni usuali e Formule
- Bibliografia
Generalità
Etimologia – Pilocarpus, dal greco pileos o pilos = cappello, feltro e karpos
= frutto per la forma del frutto, coperto di peli.
microphyllus – per le piccole foglioline
pennatifolius – per le foglie pennate con 3-5-7 foglioline.
Nomi volgari – Jaborandi, jamborandi, janguarandy, jamquarandi, sono nomi coi quali, nell’America del sud, si indicano parecchie droghe aromatiche, sudorifere e scialagoghe, appartenenti a diverse famiglie, ma specialmente alle Rutacee e Piperacee.
Arbusti o alberelli.
Parti usate – Le foglie.
Componenti principali
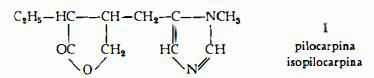
Alcaloidi appartenenti al gruppo dell’imidazolo, quattro dei quali — pilocarpina (1-4) (5), isopilocarpina (6) (7), pilocarpidina (8) (9) e pilosina (10-12) — sono chimicamente definiti.
Oltre a questi alcaloidi Petit e Polonovski (13) hanno estratto dal Pilocarpus spicatus A. St. Hil due alcaloidi, y-pilocarpina e y-jaborina, amorfi, non identificati. Parodi (14) ha riferito di avere isolato, da un campione di «Jaborandi del Paraguay», una base debole «jaborandina», C20H12O6N2, e Harnack e Meyer (15) una base «jaborina» da foglie commerciali di Jaborandi, ma l’esistenza di entrambe le sostanze non è stata confermata da altri AA. In «jaborina», ottenuta da Merck, Jowett (7) ha dimostrato la presenza di isopilocarpina, pilocarpidina e probabilmente anche di pilocarpina.
La pilocarpina, C11H16O2N2, il principale alcaloide dello Jaborandi, fu isolato per la prima volta da Gerrard (1-4) e da Hardy (5) indipendentemente. Lo stereoisomero della pilocarpina, isopilocarpina, è stato messo in evidenza da Petit e Polonovski (6) e cosi denominato da Jowett(7). La conoscenza della struttura chimica dei due alcaloidi si deve principalmente ai lavori di Jowett (16) e di Pinner (17). La formula di struttura I è stata successivamente confermata per sintesi (18).
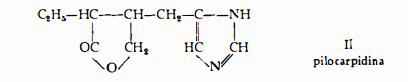
La pilocarpidina, C10H14O2N2, è stata ottenuta per la prima volta dallo Jaborandi da Merck (8) (9) ed è stata studiata da Harnack (19) (20) (21) e poi da Jowett (7). Secondo quest’ultimo A. (7) la pilocarpidina non si troverebbe nelle foglie del Pilocarpus microphyllus, nè in quelle del P. Jaborandi. Per opera specialmente degli studi di Burtles, Pyman e Roylance (22) e di Spàth e Kunz (23) ne è stata ammessa la formula di struttura II, accertata poi per sintesi (18).
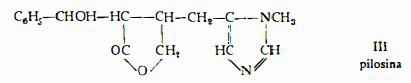
La pilosina, C16H18O3N2, isolata dal Pilocarpus microphyllus da Pyman (10), è stata ottenuta indipendentemente anche da Léger e Roques (11) (12), che l’hanno denominata «carpilina». La formula di struttura III fu proposta da Pyman (10).
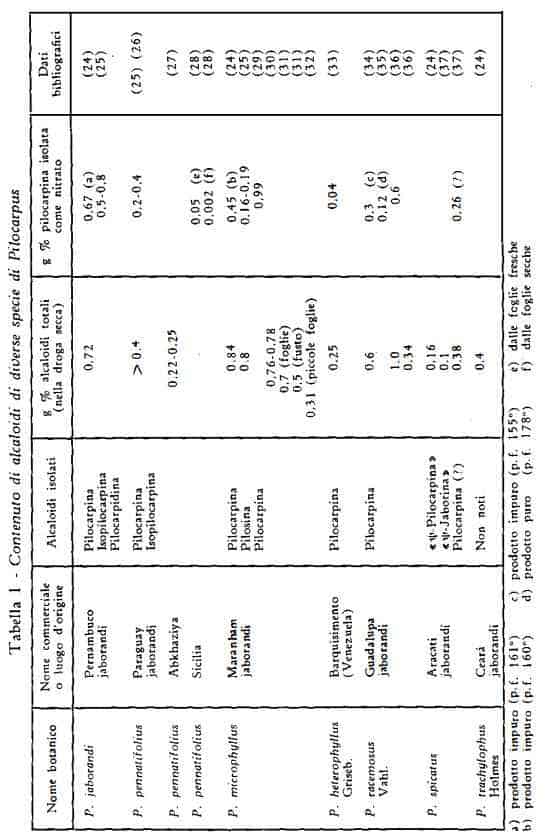
La tabella 1 raccoglie i dati reperibili in letteratura per il contenuto di alcaloidi totali e dei singoli alcaloidi delle diverse specie di Pilocarpus, che costituiscono la droga commerciale (23a).
In Pilocarpus pennatifolius cresciuto in Sicilia, secondo i risultati delle analisi di Imbesi (38), il maggiore titolo alcaloidico è stato trovato nella corteccia delle radici (g 0,138% di pilocarpina calcolata come nitrato); seguono, in ordine di contenuto decrescente, le foglioline (g 0,055%), i semi (0,046%), i piccioli delle foglie, i giovani rami, i pericarpi, i fiori ed infine la corteccia dei rami (ved. la tabella 2).
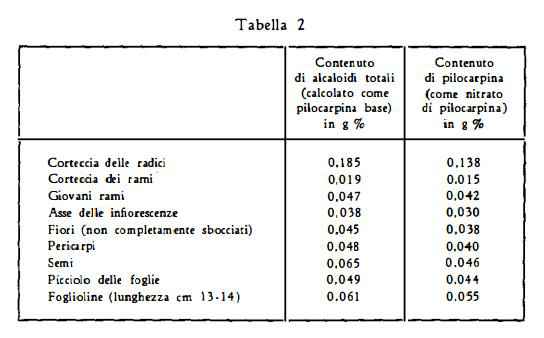
Le foglioline giovani contengono una quantità percentuale di alcaloidi maggiore di quella delle adulte e delle vecchie: il contenuto nelle foglioline delle giovani piantine diminuisce durante l’accrescimento della pianta (38). L’eliminazione delle infiorescenze provoca un aumento (20% circa) del tenore alcaloidico delle foglie; come pure un aumento, minore e poco duraturo, è causato dalla concimazione chimica (38).
La proporzione degli isomeri pilocarpina e isopilocarpina varia nelle differenti parti della pianta; i piccoli rami contengono una maggiore quantità di isopilocarpina rispetto alle foglie (6). La pilocarpina nelle foglie si isomerizza facilmente trasformandosi in isopilocarpina (6) ed è questa certamente la causa delle elevate discordanze nei risultati ottenuti dai diversi AA. nella titolazione dei due suddetti alcaloidi. La isopilocarpina può costituire infatti dal 5 al 75% degli alcaloidi totali (6).
L’alcaloide minore pilosina è stato trovato nelle foglie in quantità pari allo 0,007 % (10). E’ stato inoltre stabilito che nelle foglie, dopo la separazione di pilocarpina, isopilocarpina e pilosina, non sono presenti altri alcaloidi in quantità superiore allo 0,003% (10).
Oltre agli alcaloidi nelle foglie di Jaborandi è stato trovato olio essenziale:
— in foglie di Pilocarpus Jaborandi sono state determinate quantità di olio essenziale variabili dallo 0,2 all’1,1% a seconda se le foglie erano fresche o secche (39).
— da foglie di jaborandi commerciale, consistenti principalmente di P. microphyllus e inoltre di P. spicatus, è stato ricavato lo 0,24% di olio essenziale (39).
La composizione chimica dell’olio essenziale di jaborandi non è bene nota. Hardy (5) ne ha isolato un idrocarburo, probabilmente un terpinene o dipentene, e l’ha denominato pilocarpene. Più tardi Schimmel e Co. (40) hanno separato dall’olio essenziale di foglie di jaborandi un idrocarburo non definito, composti identificabili probabilmente con idrocarburi olefinici, metil-nonil-chetone (20,6%), probabilmente anche metil-eptil-chetone, ed inoltre 26,4% di alcooli totali, determinati come C10H16O.
Proprietà farmacologiche ed impiego terapeutico
Lo jaborandi deve le sue proprietà farmacologiche principalmente al contenuto del suo più importante alcaloide, la pilocarpina, la cui azione è fondamentalmente simile a quella dell’acetilcolina di cui possiede tutte le proprietà muscariniche. Essa agisce pertanto, con una spiccata elettività sui ricettori colinergici innervati dalle fibre post-gangliari parasimpatiche e da quelle post-gangliari simpatiche che innervano le ghiandole sudorifere. Su tali ricettori la pilocarpina esplica un’azione eccitante diretta e selettiva, che si manifesta anche dopo degenerazione del nervo e che differisce essenzialmente, nel suo determinismo, da quella dovuta all’eserina, la quale agisce invece con un effetto inibente sulla colinesterasi determinando quindi, in definitiva, un potenziamento dell’azione acetilcolinica.
Non sembrerebbe tuttavia che la pilocarpina sia completamente esente dall’azione anticolinesterasica la quale, secondo Vincent e Legreu (41) sarebbe però molto debole e si manifesterebbe più nettamente sulla colinesterasi serica che su quella del sistema nervoso. Anche l’azione gangliare, per quanto molto ridotta, sarebbe ancora evidenziabile nella pilocarpina. Marazzi (42) ha dimostrato che essa aumenta la risposta gangliare alle stimolazioni fisiologiche ed elettriche gangliari, con effetti che sono antagonizzati dall’atropina. Secondo questo A. anzi, non esisterebbero differenze di ordine qualitativo, ma soltanto quantitativo, fra le droghe che determinano stimolazioni nicotiniche gangliari e quelle comunemente ritenute come più specificamente muscariniche. Alle stesse conclusioni giunsero Ambache (43) e Feldberg e coll. (44) i quali ultimi osservarono che la pilocarpina è capace di stimolare la midollare surrenalica alla secrezione di adrenalina e che, analogamente alla neostigmina, può aumentare il tono dei muscoli scheletrici (nella capra) in particolari condizioni patologiche.
Per quanto riguarda l’intimo meccanismo d’azione, McCashland (45), in base ai risultati di sue ricerche, suppone che la pilocarpina determini la liberazione di acetilcolina a livello dei ricettori specifici, per stimolazione delle terminazioni colinergiche.
Resterebbe tuttavia da spiegare il fatto osservato da Masayoshi Suda e coll. (46) i quali sperimentando sul cuore isolato di rana secondo Yogi Straub, notarono che la pilocarpina antagonizza l’effetto depressivo dell’acetilcolina sul battito cardiaco, antagonismo che non venne invece osservato con altre droghe ad azione colinergica post-gangliare, quali la carbaminoilcolina, la muscarina e l’arecolina, l’azione delle quali ultime è considerata simile a quella della pilocarpina.
Più recentemente Dzoljic e Atanackovic (47) constatarono che la pilocarpina (50-100 g) antagonizza l’effetto contrariamente della carbocolina e dell’arecolina (10 g) sull’intestino isolato di ratto, allorché essa venga somministrata almeno un minuto dopo le suddette sostanze. Questo effetto però non è reciproco, in quanto l’azione contratturante della pilocarpina sull’intestino isolato, nelle stesse condizioni, non è antagonizzato dalla carbocolina nè dalla arecolina.
La diidroergotamina e l’esametonio non hanno alcuna influenza sul suddetto effetto spasmolitico della pilocarpina. Questa, inoltre, non decontrae l’intestino isolato precedentemente contratto dall’acetilcolina, dall’istamina e dal cloruro di bario.
Per la sua azione sui ricettori innervati dalle fibre colinergiche postgangliari, la pilocarpina estende la sua influenza a molti organi che si trovano sotto il dominio di questo settore del sistema nervoso autonomo. Le sue applicazioni terapeutiche tuttavia, per gli effetti secondari cui dà luogo, sono molto limitate.
Essa aumenta il tono e stimola le contrazioni dei muscoli lisci, aumenta la secrezione delle ghiandole esocrine innervate dai nervi colinergici postgangliari e particolarmente quella delle ghiandole sudorifere e salivari; determina miosi, vasodilatazione periferica e, di solito, abbassamento della pressione arteriosa.
Il tono ed i movimenti peristaltici dell’intestino vengono notevolmente aumentati da dosi terapeutiche di pilocarpina, la quale determina perciò un potente effetto evacuante e a tale scopo essa è impiegata in medicina veterinaria. A dosi elevate determina spasmo e tenesmo.
Il tono e la motilità dei muscoli lisci della colecisti, dei dotti biliari, degli ureteri e della vescica urinaria, vengono parimenti aumentati.
I bronchi e i bronchioli subiscono una costrizione alla quale può conseguire l’insorgere di fenomeni dispnoici asmaticosimili.
La diaforesi è fortemente aumentata e, sotto l’azione della pilocarpina possono essere eliminate, attraverso la secrezione sudorifera, notevoli quantità di azoto non proteico, sotto forma di urea; le dosi diaforetiche dell’alcaloide possono però determinare effetti secondari non desiderati.
Le secrezioni lacrimale, salivare e dei succhi digerenti (gastrica, intestinale, epatobiliare e pancreatica esocrina), come pure quella della mucosa bronchiale, vengono in varia misura stimolate dall’azione della pilocarpina.
In terapia lo Jaborandi è impiegato soprattutto come scialagogo, come diaforetico (nell’uremia), e per facilitare l’espettorazione.
La pilocarpina, sotto forma dei suoi sali, è impiegata in oculistica come miotico, e, inoltre, come antagonista negli avvelenamenti da Belladonna e da atropina ed in medicina veterinaria, in alcuni casi, come purgante.
Gum e Kooke (48) hanno impiegato la pilocarpina per abolire gli effetti secondari determinati dai ganglioplegici (esametonio, tartrato di pentolinio) usati nella terapia dell’ipertensione. La dose di 5 mg di pilocarpina fu sufficiente a dominare gli effetti collaterali derivanti dal blocco gangliare, che scomparvero dopo mezz’ora dalla somministrazione dell’alcaloide e per la durata di 6-10 ore, secondo la dose somministrata.
In alcuni casi di febbre da fieno e di rinite spasmodica aperiodica, in cui l’efedrina e i preparati di calcio risultarono inattivi, il de Gunten (49) impiegò, con buoni risultati, un estratto di jaborandi somministrato topicamente a gocce o per via sottocutanea, tanto negli adulti quanto nei bambini, dai quali venne pure ben tollerato. Anche in diversi casi di flogosi rinosinusali, con infiammazione dell’etmoide, in alcuni dei quali il trattamento antibiotico era rimasto senza effetto, il Mombelli (50) impiegò un preparato risultante dall’associazione di estratto di jaborandi, di clorofilla e di acido nicotinico, notando una decisiva azione risolutrice di questo medicamento nelle suddette sindromi.
La pilocarpina viene in parte distrutta nell’organismo e in parte eliminata con le urine in forma combinata.
L’intossicazione da pilocarpina può essere provocata da dosi aggirantesi intorno ai 100 mg e si manifesta con nausea, vomito, diarrea, scialorrea, sudorazione, spasmo bronchiale e difficoltà di respirazione, astenia, tremore, vertigine, stato confusionale, depressione e, in fine, collasso.
La terapia dell’avvelenamento consiste nella somministrazione di atropina come antagonista diretto e nel praticare una terapia sintomatica per sostenere la respirazione e per combattere l’edema polmonare.
Estratti e preparati vari
a) Estratto fluido (titolo chimico 0,4 % di alcaloidi) (g 1 = L gtt).
Dosi: g 0,5- 1 pro dose, g 2-6 pro die.
b) Tintura titolata allo 0,04 % di alcaloidi.
Preparazioni usuali e formule galeniche
Tintura
Estratto fluido jaborandi g 10
Alcool di 50° g 90
(fino a g 15 pro die).
Sciroppo
Estratto fluido jaborandi g 5
Alcool e glicerina ana g 10
Sciroppo semplice F. U. g 75
(a cucchiai).
Pozione diaforetica
Estratto fluido jaborandi g 2
Rhum…………………. g 30
Sciroppo di arancio amaro g 50
Acqua distillata g 70
(a cucchiai).
BIBLIOGRAFIA
(1) GERRARD A. W., Pharm. J., 5, 865 ..1875 – (2) GERRARD A. W.. ibid., 5, 965, 1875 – (3) qER- RARD A. W., ibid., 6, 227, 1876 – (4) GERRARD A. W., ibid. 7, 255, 1877 – (5) HARDY E., BuH. soc. ehim. Frane., 24, 497, 1875 – (6) PETIT A. e POLONOVSKI, ibid., 17, 554, 1897 • (1) JO^^^ H. A. D., J. Chem. Soc., 77, 473, 1900 • (8) MERCK E., Merck’s Jahrb., 1896, 11 – (9) MERCK E., ibid., 1897, 5 – (10) PYMAN F. L., J. Chem. Soc., 101, 2260, 1912 – (H) LÉGER E. c ROQUES F., Compt. rend., 155, 1088, 1912 – (12) LÉGER E. e ROQUES F., ibid., 156, 1687, 1913 • (13) PETIT A. e POLONOVSKI M., Bull. soc. chim. Frane., 17, 553, 1897 – (14) PARODI D., citalo èa HOLMES E. M., Pharm. J. 5, 781, 1875 – (15) HARNACK E. e MEYER H., Lieb. Ann., 204, 67, 1880 – (16) JOWETf H. A. D., J. Chem. Soc., 83, 438, 1903 • (17) PINNER A., Ber., 33, 2357, 1900; 35, 192, 190J – PINNER A. e SCHWARZ, ibid., 35, 2441, 1902 – PINNER A., ibid., 38, 1510, 1905 – {18) PREOBRASHENSKI N. A. e W. A. e coll., Bull. acad. sci. U.R.S.S., 983, 1936 – (19) HARNACK E., Chem. Zbl., 628, 1885 – (20) HARNACK e., Arch. exp. Path. u. Pharmakol., 20, 439; Chem. Zbl., 805, 1886 – (21) HARNACK E., Lieb. Ann., 238, 230, 1887 – (22) BURTLES R., PYMAN F. L. e ROYLANCE J., J. Chem. Soc., 127, 581, 1925 – (23) SPAETH e. e KUNZ E., Ber., 58, 513, 1925 – (23a) BATIERSBY A. R. e OPENSHAW H. T. in MANSKE R. H. F. e HOLMES H. L., The Alkaloids, vol. III, p, 206 • (24) PAUL B. H. e COWNLEY A. J., Pharm. J., 3, 1, 1896 – (25) HOLMES E. M., ibid., 1, 520, 1895 – (26) CHEMNITIUS F., J. prakt. Chem., H8, 20, 1928 – (27) TARAN E. N., Farmatsiya, n. 5, 26, 1940; Chem. Abs., 34, 8180, 1940 – (28) IMBESI a., Arch. farmaco/. sper., 65, 113, 1938 – (29) CARR F. H. e REYNOLDS W. C., Pharm. J., 26, 543, 1908 – (30) EVANS, SONS, LESCHER e WEBB, Ltd., Analytical Notes, 21, 1906 – (31) EVANS, SONS, LESCHER e WEBB, Ltd., Analytical Notes, 35, 1909 – (32) EVANS, SONS, LESCHER e WEBB, Ltd., Analytical Notes, 42, 1912 – (33) BLACK O. F., KELLY J. W. e STOCKBERGER W. W., Am. J. Pharm., 95, 4, 1923 – (34) COWNLEY A. J., citato da HOLMES E. M., Pharm. J., 28, 54. 1904; Chem. Zbl., 75, I, 464, 1904 – (35) JOWETT H. A. D. e PYMAN F. L., Proc. Chem. Soc., 28, 268, 1912 – (36) HOLMES E. M., Pharm. J., 17, 713, 1903 – (37) HOLMES E. M., ibid., 1, 501, 1895 – (38) IMBESI a., Arch. it. sci. /arm.. 7, 66, 1957 – (39) GILDEMEISTER e HOFFMANN, Die Aethe- rische Oele, III ed., voi.. II, 945 – GUENTHER E., The Essential Oils, III vol., 1949, p. 374 – (40) SCHIMMEL e CO., Ber. Schimmel, 1924, 50; 1929, 51 – (41) VINCENT D. e LEGREU R., Ann. pharm. Jang., n, 321, 1953 – (42) MARAZZI A. S., J. Pharmacol. exp. Ther., 65, 18, 35, 1939 – (43) AMBACHE N., J. Physiol., no, 164, 1949 . (44) FELDBERG W.. MINZ B. e TSUDZIMURA H., ibid., 82, 286, 1934 – (45) MCCASHLAND B. W., J.A.Ph.A. ed. sci., 42, 327, 1953 – (46) MASAYOSHI SUDA, TOMIO TOYAMA e KOZABUTO SEKI, Nippon Yakurigaku Zasshi, 53, 881, 1957; Chem. Abs., 52, 20637i, 1958 – (47) DZOUIC M. e ATANACKOVIC D., Arch. intem. pharmacod. et de ther., 140, 29, 1962 – (48) GUM J. A. e KOOKE A. M., Brit. Med. J., 1, 1473, 1954 – (49) DE GUNTEN P., Schweiz. med. Woch., n. 33, 958, 1941 – (50) MOMBELLI U., li Valsalva, 29 ott. 1953.

