Melanzana
Tratto da “Piante Medicinali – Chimica, Farmacologia e Terapa” di R. Benigni, C. Capra e P.F.Cattorini
(Solanum melongena L. – Fam. Solanacee/Solanee/Solaninee)
(Sin. – Solanum esculentum Dunal. – Melonga tereta Mill.)
Melanzana- Ultimo aggiornamento pagina: 27/02/2018
Indice dei contenuti
- Generalità
- Componenti principali
- Proprietà farmacologiche
- Estratti e preparati vari
- Preparazioni usuali e Formule
- Bibliografia
Generalità

Etimologia – Solanum, dal latino solari = alleviare, lenire, calmare, allusione alle virtù sedative di alcune piante di questo genere.
melongena, dal greco mhlon = mela, pomo e gennaw = produco, che dà
frutti simili a mele.
esculentus – mangereccio.
tereta, dal latino teres, teretis = bislungo, ovale.
La specie melongena si trova indicata col sinonimo Solanum incanum L. (incanum, con la c.) : è un qui pro quo. Il Solanum incanum, della Flora Peruviana (la c.d. Maça amarga = mela amara), è sinonimo del Solanum albidum Dunal. Incanus (lat.) = biancastro. Ha i frutti tossici. Nelle antiche farmacopee la sp. melongena è indicata Mala insana Dod., Mala insana syriaca Park., Malum insanum Gesn. e da ciò è derivata l'indicazione Solanum insanum L. (insanum, con la s), cioè mela matta. L’uso della melongena come cibo è antico. Si ritiene che debba però essere usata se non perfettamente matura, perchè, acerba, può nuocere. I vari preoccupanti inconvenienti indicati da Avicenna (ricordati dal Mattioli, IV lib. di Diosc. cap. LXXVIII), con tutta probabilità, conseguivano all’uso, secondo Dunal, dei frutti della Solanum ovigerum Dunal. la c.d. pianta delle uova, per il suo frutto che ha la forma, il volume, il colore di un uovo di gallina. Questa specie ha i semi involti in una polpa molto acre, molle, tossica (che manca nella melongena), che bisogna togliere per usare i frutti a scopo alimentare. Malcrida ricorda (Materia Medica, 1896) che Alessandri trovò la solanina nel frutto edule della melongena, anzi, in certe condizioni di suolo e di clima, vi aumenta, pare, in guisa da rendere i frutti pericolosi, perchè anche con la cottura la solanina non scompare. Ciò giustificherebbe lo insanum ed il mala insana.
Nome volgare – Pomo d’amore (antic.) (si mangiano i frutti per provocare lussuria, Avicenna), petonciano, petronciano (tose.), malignana (nap.), muligiana (sic.), meinzano (sard.) ecc.
Eyerfrucht (ted.), the egg-plant (ingl.), melongène, aubergine (fr.), berinjena (spagn.), beringela (port.), tojàs csucsor (ungh.), ca-an (cocinc.), k’ié, koen luen koa, ts’ao pie kia (cinese), baklazhàn (russ.).
Habitat – Originaria dall’India e dalla Cocincina. Coltivata da tempi antichissimi in Asia, Africa. Nel mezzodì d’Europa (Francia, Italia, Spagna, Portogallo). Bacino mediterraneo (Siria, Tripolitania, Cirenaica), in molte delle regioni calde e temperate, America, Antille (Martinica, Guadalupa), Guyana, nelle diverse forme e varietà (violetta lunga, cilindrica, ovale, violetta grossa rotonda, violetta nana, screziata della Guadalupa) (bianca picchiettata di rosso), gialla, rotonda della Cina, mostruosa di New York, ecc.).
Pianta erbacea, annuale.
Parti usate – I frutti.
Componenti principali
Composti caffeici cinarinosimili 0,00231 %, espressi in acido caffeico, nel frutto fresco (1); acido clorogenico (1a): il glucoalcaloide steroidico solasonina C45H73O16N-3H2O (2); le antocianine nasunina e nasunina A, isolate dal pericarpo (3), carotene g 22 e vitamina A 34 U.I. in 100 g di frutto fresco (4); riboflavina (4a) ed acido ascorbico (5), il contenuto dei quali diminuisce nel corso della maturazione del frutto; acido glutammico (6) 0,605-0,642% (7), acido aspartico e asparagina (6), tiramina, 5-ossitriptamina (6a), triptamina (6b); una globulina, trovata nel sarcocarpo del frutto, la quale agisce come inibitrice dell’ossidasi dell’acido ascorbico (8); ossidasi dell’acido ascorbico ed un fattore inibitore dello stesso, contenuti nel succo del frutto (8); un fattore inibitore della colinesterasi (9); o-polifenolossidasi (10); pectine
(11) 3,2-5,1% nel frutto secco (12), 11% come pectato di calcio nella sostanza secca (12a). Dall’analisi del frutto fresco sono stati ottenuti i seguenti valori quantitativi: acqua 92-93%, sostanze azotate 0,76-1,5%, grasso 0,06-0,13%, ceneri 0,4-0,7% (13), acido ossalico 29,1 mg % (13a), ferro totale mg 1%, ferro ionizzato mg 0,89% (14), sodio mg 2,8% nella varietà a forma allungata, mg 3,6% nella varietà a forma rotonda (frutti delle isole Hawaii) (15). E’ citata anche la presenza di zinco e di manganese (15a).
Glucoalcaloidi
Un glucoalcaloide, C45H73O16N-3H2O, isolato da Waal e coll. (2) dai frutti del Solanum melongena L., che presenta spettro infrarosso identico a quello della solasonina e per idrolisi produce i medesimi zuccheri, ottenibili per scissione della solasonina, cioè glucosio, galattosio e ramnosio, ed un aglucone, C27H43O2N, identificato con la solasodina, aglucone della solasonina.
La solasonina, C44H73O16N, già nota per essere stata estratta per la prima volta da Oddo (16) dal Solanum sodomaeum L. e denominata solanina S, è stata in seguito identificata con il glucoalcaloide solancarpina del S. xanthocarpum Schrad e Wendl. e con la purapurina del S. aviculare Forst. (17). La composizione chimica della solasonina è stata studiata specialmente da Rochelmeyer (19) e da Briggs e coll. (17) (18) (20). Questi ultimi AA. (20) per la solasodina hanno proposto la formula di struttura steroidica I.
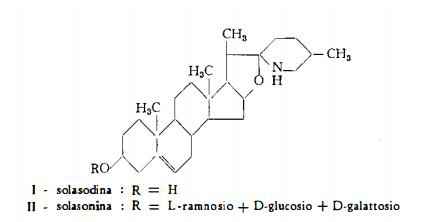
Il contenuto alcaloidico dei frutti, espresso in solasodina è risultato pari allo 0,25% (20a).
Glucosidi antocianici
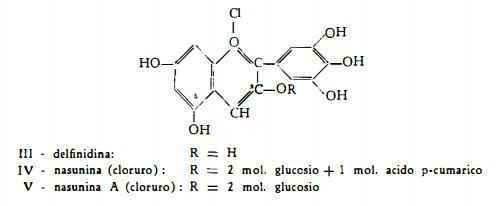
Nasunina (cloruro: C36H37O19CI), glucoside antocianico estratto per la prima volta da Kuroda e Wada (3) dal pericarpo del frutto del Solanum melongena L. var. esculentum Ness., è stato dagli stessi AA. denominato nasunina (21) e riconosciuto probabilmente identico ad un glucoside della delfinidina, che per idrolisi produce una molecola di acido p-cumarico e due molecole di glucosio (22).
Gli stessi AA. (3) hanno pure separato dal pericarpo del frutto un altro glucoside della delfinidina (cloruro: C27H31O17CI), che era già stato estratto dai fiori del Linum grandiflorum var. rubrum (23) e dai fiori violetti delle Clematis (24). Questa sostanza è stata denominata nasunina A (21).
Proprietà farmacologiche ed impiego terapeutico
Il merito di aver attratta l'attenzione sulle attività farmacologiche e terapeutiche della Melanzana, spetta all'argentino Roffo (25) il quale in una sua nota apparsa nel 1943 riferì i risultati da lui ottenuti studiando questa solanacea sia sperimentalmente che clinicamente.
Sperimentalmente egli osservò che estratti ottenuti dal mesocarpo del frutto di Melanzana, determinano nei conigli una diminuzione di circa il 50% del tasso colesterolemico e nei cani portatori di fistola biliare, un aumento del flusso sino a raggiungere il doppio dei valori iniziali. Tali estratti manifestano la stessa attività nell’uomo in cui danno luogo inoltre, ad un notevole aumento della diuresi.
Le ricerche di Roffo furono riprese e confermate nel 1949 da De Filippi (26) e da Mininni e Scardigli nel 1950 (15a), relativamente alla azione diuretica e ipocolesterolemizzante e da Siliprandi (27) relativamente all’azione colagoga.
Graham, Beare e Grices (28) al contrario, sperimentando su conigli alimentati con diete ricche di colesterolo e successivamente trattati con estratti di Melanzana, non hanno osservato alcun effetto ipocolesterolemizzante e nessuna differenza fra gli animali trattati con i suddetti estratti.
Recentemente Orgell e coll. (29) hanno trovato che, analogamente agli estratti acquosi di altre solanacee, anche quelli di frutti di S. melongena, sono dotati di un’attività inibente, in vitro, la colinesterasi contenta nel plasma umano.
L’attività terapeutica della Melanzana è molto simile e si potrebbe dire identica a quella del Carciofo: la stessa azione colagoga e coleretica, la stessa azione ipocolesterolemizzante e la stessa azione diuretica. L'unica differenza esistente va ricercata nel fatto che, mentre la parte terapeuticamente attiva del Carciofo è rappresentata dalle foglie caulinari non commestibili, la parte attiva della Melanzana è data dal frutto largamente usato nell’alimentazione.
E’ appunto da questa analogia di azione e dal fatto che Politis (1a) aveva già accertato la presenza dell’acido clorogenico, nel frutto di Solanum melongena, che siamo stati indotti ad istituire alcune ricerche al fine di vedere se all’analogia farmacologica e terapeutica, corrispondesse anche una più stretta analogia chimica fra i principi attivi delle due droghe. I risultati di ricerche spettrofotometriche e cromatografiche eseguite su estratti ottenuti dalla Melanzana, hanno confermato infatti la presenza in essa di composti cinarinosimili analoghi a quelli contenuti nel Carciofo, sebbene in quantità inferiore (1).
Per quanto riguarda quindi il meccanismo con cui questi principi attivi svolgono la loro azione, vale quanto fu già detto a proposito del Carciofo
Più recentemente Bergonzi (30) ha sperimentato clinicamente un preparato a base di estratto di Melanzana e di Carciofo, in un gruppo di 15 bambini d’ambo i sessi e di età compresa fra 1 e 13 anni, affetti da epatite virale.
Dai risultati ottenuti l’A. conclude sostenendo l’opportunità di associare alla terapia antibiotica e, eventualmente, cortisonica, preparati a base di composti cinarinici i quali, per la loro attività coleretica, colagoga, ipocolesterolemizzante ed epatoprotettiva, sono capaci di favorire una rapida normalizzazione sia dei segni obiettivi, sia della funzionalità epatica.
Estratti e preparati vari
a) Estratto fluido (g 1 = XXVIII gtt).
Dosi: a cucchiaini diluito in acqua.
b) Estratto molle acquoso (1 p. = 20 p. circa di droga).
Dosi: g 0,1-1 e più pro dose.
c) Estratto molle iniettabile.
Dosi: pari a g 1-5 o più di droga.
d) Estratto secco acquoso (1 p. = 30 p. circa di droga).
Dosi: g 0,1-1 e più pro dose.
Preparazioni usuali e formule galeniche
Tintura
Estratto fluido melanzana……………………………………………. g 20
Alcool di 20°……………………………………………………………….. g 80
(a cucchiai).
Sciroppo
Estratto fluido melanzana……………………………………………. g 50
Sciroppo semplice F.U……………………………………………….. g 50
(a cucchiai).
BIBLIOGRAFIA
(1) BENIGNI R., CASTOLDI C. F. e BACCHINI M., Fitoterapia, 29, 815, 1958 – (la) POLITIS J., Compt. rend., 226, 692, 19 48 • (2) WAAL J. S.. DE NEETHLING L. P. e PEROLD G. W., J. S. African Chem. Inst,, 13, 45, 1960; Chem. Abs.. 54, 22871 d, 1960 – (3) KURODA C. e WADA M., Chem. Zbl., IL 1472, 1934 – {4) BORREL S., Anal. Bromat., n. 1, 1956;Mon, de la Farm., 62, 275, 1956 – (4a) JUNZO HAYASHI, Shiga Kenritsu Nogyó Tankidaigaku, Gakujutsu Hokoku, Ser. I, n. 8, 24, 1956; Chem. Abs., 51, 13083e, 1957 – (5) EMIKO NAKAMURA, Vitamins (Japan), 8, 424, 1955; Chem. Abs.. 49, I5117a, 1955 – (6) KENJI SAIO, TAKAO HIRANO e JIRO KIMURA, Nippon Dofo-hiryogaku Zasshi, 27, 503, 1957; Chem. Abs., 52, 6692i, 1958 • (6a) UDENFRIEND, LOVENBERG e SJOERDSMA, Arch. Biochem. Biophys., 85, 487, 1959 -(6 b) TYLER e SMITH, Arbeitstagung «Biochemie und Physiologie der Alkaloide», Halle, 1960 – (7) MAGGIOLO FIGARI E., Rev. Fac. Farm. y Bioq.. 14, 17, 1952 – (8) CHOTEN INAGAKI, HIROYASU FUKUBA e AYAKO MATSUSHITA, Nautral Sci. Rept. Ochanumizu Vniv., (Tokyo), 5, 313 e 323, 1955; Chcm. Abs., 50, 7171, 1956 – (9) ORGELL W. H., VAIDYA K. A. e DAHM P. A., Science, 128, 1136, 1958 – (10) KENKARE V. W. e SOHONJE K., Current. Sci., 20, 268, 1951; Ber. wiss. Biol, 76, 276, 1952 – (li) SCHARPENSEELE H. W., Landwirtsch. Forsch., 10, 191, 1957; Chem. Abs., 52 , 6662h, 1958 – (12) CORRAO A., Ann. Sper. Agr., IO, 269, 1956; Chem. Abs,, 52, 3192e, 1958 – (12a) BENNETI, Food Research, 9, 462, 1944 – (13) WEHMER C., Die Pflam.:enstofle, 1931, p. 1090 • (13 a) MAJUNDAR B. e coli., Indian J. Med. Research, 35, 671, 1938 – (14) SHASH C. C. e PATEL S. Z., Bansilal Amritlal Agr. Col/. Mag., 9, 4, 1955; Chem. Abs., 51, 17013a, 1957 – (15) WENKAM N, S. e MILLER C. D., Hawaii Farm, Sci., 6, 2, 1957; Chem. Abs., 52, 14889i, 1958 • (I5a) MININNI G. e SCARDIGLI G., La Settimana Medica, 38, 276, 1950 – (16) ODDO G., Ber., 62, 267, 1929 – (17) BRIGGS L. H., J. Am. Chem. Soc.. 59, 2467, 1937; Nature, 144, 247, 1939; BRIGGS L. H. e ANDERSON A. R., J. Chem. Soc., J036, 1937: BRIGGS L. H. e BELL R. C., ibid., 1, 1942; BRIGGS L. H., NEWBOLD R. P. e STACE N. E., ibid., 3, 1942; BRIGGS L. H., BELL R. C. e CARROLL J. J., ibid., 12; 1942 – (18) BRIGGS L. H. e CARROLL J. H,, ibid., 17, 1942 – (19) ROCHELMEYER H., STUETZEL H. e CHEN H., Arch. Pharm., 282, 92, 1944 – (20) BRIGGS L. H., HARVEY W. E., LOCKER R. H., MCGILLIVRAY W. A. e SEELYE R. N., J. Chem. Soc., 3013, 1950 – (20a) GRACZA L. e SZASZ K., Arch. Pharm., 295, 859, 1962 – (21) KURODA C. e WADA M., Chem. Zbl., Il, 1939, 1936 – (22) KURODA C. e WADA M., Chem. Zbl,, II, 3244, 1935 – (23) ROBINSON G. M. e ROBINSON R., Biochem. J., 25, 1687, 1700, 1931 – (24) ROBINSON G. M. e ROBINSON R., Biochem. J., 28, 1712, 1934 – (25) ROFFO A. H., Boli. Inst. Med. Experim-, n. 62, 1943 – (26) DE FILIPPI P., Min. Med., 40, 46, 366, 1949 – (27) SILIPRANDI N., cit. da DE FILIPPI I.c. – (28) GRAHAM W. D., BEARE J. L. e GRICES H. C., Circu/ation Research, 7, 403, 1959 – (.29) ORGELL W. H., VAIDYA K. A. e DAHM P. A., Science, 128, 1136, 1958 – (30) BER- GONZI F., Min. Ped., 13, 7, 209, 1961.

