Se hai un abbonamento attivo ACCEDI QUI
Lobelia
Tratto da “Piante Medicinali – Chimica, Farmacologia e Terapa” di R. Benigni, C. Capra e P.F.Cattorini
(Lobelia inflata L. – Fam. Lobeliacee)
Lobelia- Ultimo aggiornamento pagina: 27/02/2018
Indice dei contenuti
- Generalità
- Componenti principali
- Proprietà farmacologiche
- Estratti e preparati vari
- Preparazioni usuali e Formule
- Bibliografia
Generalità

Etimologia – Lobelia – genere dedicato a Matthias von Lobel (1538-1616) o de l’Obel, medico e botanico olandese.
La Lobelia fu trovata fra le droghe usate dagli Indiani dell’America e venne portata in Inghilterra dal Recce ed introdotta come medicamento da Cutler, Druy, Elloston, Andrew (1829-30).
inflata – perchè, dopo la fecondazione, l'ovario cresce e si rigonfia formando una cassula vescicolosa, sormontata dal calice e dalla corolla secca. Il frutto contiene dei caratteristici semi piccoli, rossi, reticolati, foveolati, numerosi.
Nome volgare – Tabacco indiano, perchè fresca (più debole nel secco) ha odore aspro, irritante e sapore pungentissimo, viroso, che ricorda quello del tabacco. La polvere della pianta secca è starnutatoria e provoca la tosse. Common Lobelia, Indian Tobacco (ingl.), Lobélie enflée (fr. canad.).
Habitat – Vegeta allo stato selvaggio, nei terreni acquitrinosi dell’America settentrionale (U.S.A. – Texas, Michigan, Carolina, Missisipi, Georgia/sud, Arkansas) Canada. Coltivata in America (New York, New Lebanon – Massachusetts) e in Europa, anche come pianta ornamentale.
Pianta erbacea annuale (0,30-0,60 cm. alt.).
Parti usate – Le parti aeree (steli, foglie, sommità fiorite) raccolte alla fioritura e private dei cauli basilari (Lobeliae herba F.U.). La droga si trova in commercio, oltre che sciolta, anche in pacchetti rettangolari, ravvolti in stagnola, che contengono frammenti di cauli ispidi, angolosi, appiattiti per compressione, striati longitudinalmente, foglie verdastre o giallastre o frammenti di esse, fiori, frutti con semi.
Si trova sostituita con parti aeree di altre congeneri (L. urens L., nicotianaefolia Heynes (India, detta dawul-deowul o boke-nu), syphilitica L., cardinalis L., radicans Thumb. e sofisticata con parti aeree della Scutellaria lateriflora L. (Labiate, Viriginia), la quale è priva del caratteristico odore e sapore della Lobelia.
Componenti principali
Alcaloidi con nucleo piperidinico, la cui presenza è stata segnalata per la prima volta dal Procter (1) nel 1836. Con il nome di lobelina furono in seguito designati diversi preparati alcaloidici, che erano in realtà miscele di diverse sostanze. L’isolamento e la conoscenza della struttura chimica della lobelina e di altri tredici alcaloidi della Lobelia inflata si deve al Wieland (2-11), che, in collaborazione con i propri allievi, nel periodo dal 1921 al 1939, pubblicò una serie di importanti lavori su questo argomento. I quattordici alcaloidi isolati dal Wieland sono i seguenti:
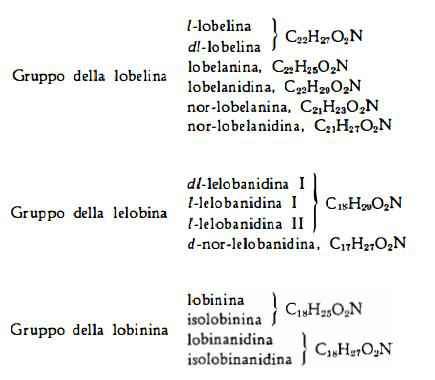
La presenza di almeno trenta alcaloidi secondari della Lobelia inflata L., estraibili con cloroformio dalle soluzioni acquose acide per acido cloridrico, è stata stabilita nel 1957 dallo Schòpf e coll. (12). Sette di questi alcaloidi sono stati isolati in forma pura e per sei di essi è stata chiarita la composizione chimica. Si tratta delle seguenti sostanze:
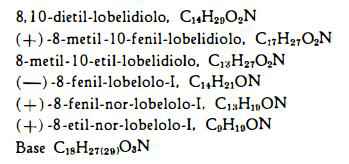
Gli alcaloidi qui nominati sono quelli sinora isolati dalla Lobelia inflata L.; molto più grande è però il numero degli isomeri teorici, che possono in realtà sussistere (2-11) (12).
Classificazione e struttura chimica degli alcaloidi della Lobelia inflata
Gli alcaloidi della Lobelia inflata constano di un nucleo piperidinico, portatore di una o di due catene laterali.
1) Alcaloidi con due catene laterali
I 14 alcaloidi, isolati ed identificati dal Wieland e coll. (2-11), sono stati classificati in tre gruppi, gruppo della lobelina, gruppo della lelobina e gruppo della lobinina, ciascuno dei quali riunisce rispettivamente 8,10-difenilderivati, 8-etil-10-fenil-derivati e 8-etil-10-fenil-deidroderivati. Schòpf e coll. (12) hanno estratto ed identificato tre altri alcaloidi con nucleo piperidinico e con due catene laterali, simili agli alcaloidi isolati dal Wieland. Per questi tre composti e per gli altri già noti, gli stessi AA. hanno proposto una nuova nomenclatura (ved. la tabella I), considerando che la loro struttura è riferibile alle tre formule basilari (I, II e III) denominate rispettivamente lobelidione, lobelionolo e lobelidiolo:
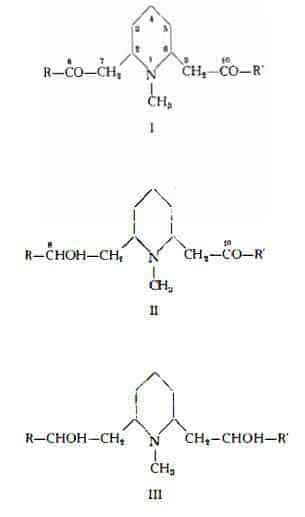
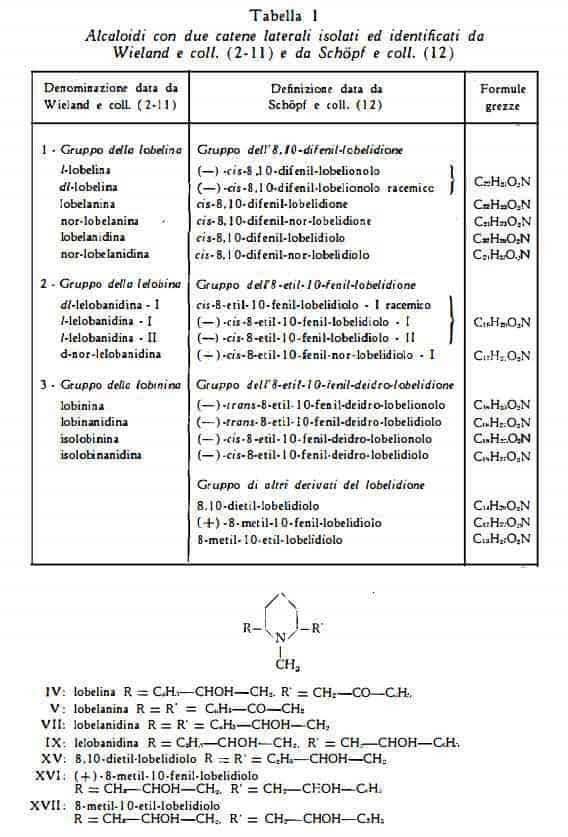
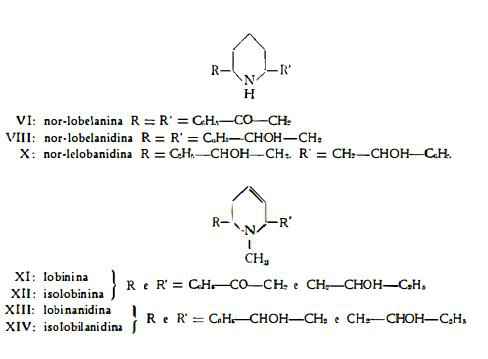
2) Alcaloidi con una catena laterale
Gli alcaloidi della Lobelia con una sola catena laterale sono le sostanze con lo schema basilare XVIII (R=H), indicate dallo Schòpf (12) con il nome di lobelolo.
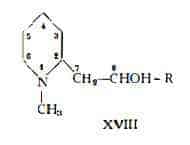
Si tratta di alcaloidi secondari della Lobelia, per uno dei quali, già isolato da Wieland e coll. (11), Schòpf e coll. (12) hanno definito la formula centesimale C13H19ON in sostituzione della C14H21ON proposta dal Wieland (11). Schòpf e coll. (12) hanno inoltre stabilito, quale formula di struttura della stessa sostanza, la XIX, equivalente a (+)-8-fenil-nor-lobelolo-I.
Due altri alcaloidi secondari con una sola catena laterale sono stati estratti dalla Lobelia inflata dallo Schòpf e coll. (12) ed identificati come (—)-8-fenil-lobelolo-I e (+)-8-etil-nor-lobelolo-I con le formule (XX) e (XXI) rispettivamente. Entrambi questi alcaloidi erano già stati estratti e qualificati da Wieland e coll, come probabili fenil-lobelolo il primo (8) e metil-lobelolo il secondo (11). La formula di struttura dell’8-fenil-lobelolo è stata riconosciuta identica a quella di un alcaloide già ottenuto per sintesi (13) ed alla sedamina, isolata dal Sedum acre (14). La sedamina è l’8-fenil-lobeIolo-II.
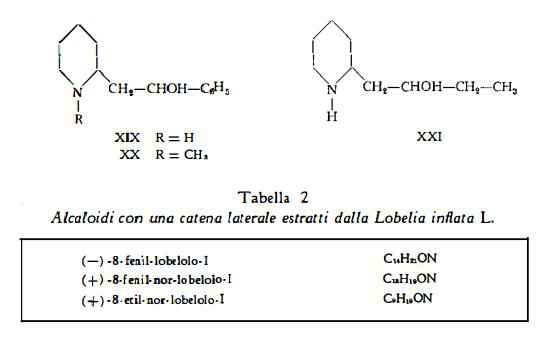
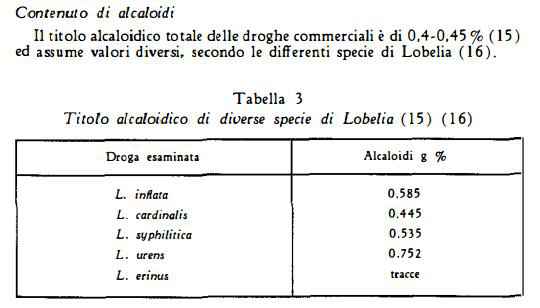
Una buona resa di alcaloidi e di lobelina è stata ottenuta dalla Lobelia urens (17) (18) (19), specie europea facilmente coltivabile. D'altra parte anche la coltivazione della Lobelia inflata L., attuata con adatta concimazione in Europa (zona di Parigi), ha prodotto droga attiva come quella importata dall’America (19). Ricerche fatte in territorio svizzero sulla cultura di Lobelia inflata tetraploide hanno permesso di aumentare sino al doppio il rendimento di alcaloidi del raccolto (20). La Lobelia infiata L. è stata pure coltivata in Italia, nella zona di Pavia ed ha dato raccolti di ottimo rendimento (20a).
Il contenuto di alcaloidi della Lobelia inflata varia nelle diverse fasi di crescita (0,134-0,635%) (21); aumenta rapidamente nella pianta giovane sino a raggiungere un primo massimo poco prima della fioritura, un secondo massimo alla fine della fioritura ed una rapida diminuzione quando la pianta appassisce. Gli alcaloidi sono distribuiti differentemente nella pianta (22), come appare dai valori raccolti nella tabella 4.
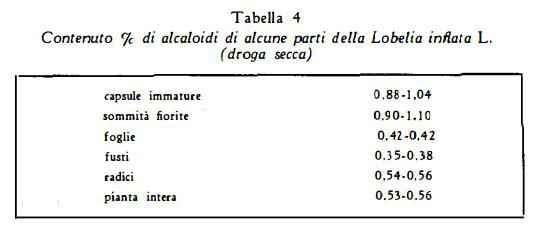
Gli steli e le foglie hanno il più basso contenuto di alcaloidi; le sommità fiorite e le capsule il contenuto più elevato. Le radici hanno un titolo equivalente a quello del resto della pianta ed è pertanto consigliabile anche la raccolta delle radici.
Altri componenti: acido b-b’-fenilossipropionico (11), acido chelidonico nei fiori (ca. 0,2%0), nei semi (tracce) e nelle radici (tracce) (23), acqua 5,42-7,18%, in media 9,58% nella pianta essiccata all'aria (24). Ceneri 6,9-7,4% nella pianta (25).
La presenza di cristalli di ossalato di calcio, ammessa da alcuni AA. (26)
(27), è stata negata da altri (28-32), Recentemente Wallis (33) ha dimostrato che la sostanza, abbondantemente presente in forma di cristalli nel mesofillo delle foglie della Lobelia inflata L., non è costituita da ossalato di calcio, ma da grasso. Da notarsi che la presenza di minute gocce di olio sparse nel mesofillo della Lobelia era già stata segnalata nella British Pharmacopoeia (34).
Proprietà farmacologiche ed impiego terapeutico
La Lobelia era usata nei paesi di origine come emetico ed anche in sostituzione del tabacco.
In medicina venne introdotta nei primi anni del secolo scorso da Samuele Tompson secondo alcuni (35), o da Cutler secondo altri (36).
L'azione farmacologica e terapeutica della Lobelia è in gran parte dovuta al suo alcaloide principale, la lobelina, la cui azione presenta molte analogie con quella della nicotina [Edmunds (37)], ma di questa meno tossica.
Oltre quest'azione nicotinica, per la quale i gangli sinaptici vengono prima eccitati poi depressi, la lobelina possiede a piccole e medie dosi, una notevole attività sulla funzione respiratoria la quale viene eccitata non per stimolazione diretta del centro respiratorio ma, secondo Heymans e coll. (38), indirettamente dai chemiocettori dei glomi carotidei e aortici, ciò che anche recentissimamente venne confermato da Penna e Aviado (39). Sono soltanto le dosi elevate e pertanto non terapeutiche, che possono agire direttamente sul centro respiratorio deprimendolo prima ed eccitandolo poi.
L'azione della lobelina sulla funzione respiratoria è energica ma transitoria ed è specialmente evidente allorché il centro respiratorio è patologicamente depresso o si trovi sotto l’azione di veleni paralizzanti (ipnotici, narcotici, anestetici, ossido di carbonio ecc. [Dreser (40), Gnus (41)]. Secondo altri l'azione stimolante della lobelina sulla respirazione, sarebbe invece più debole allorché il centro respiratorio sia stato depresso con cloralio o con morfina [Curtis e Wrigh (42)]. L’azione della lobelina sarebbe anche meno attiva contro l’azione deprimente dei narcotici alifatici [Wieland e Mayer (43)].
La ventilazione polmonare viene facilitata anche dalla broncodilatazione che consegue all’azione della lobelina [Forster ed altri (44)], azione che secondo alcuni sarebbe dovuta alla paralisi degli accettori colinergici (azione atropinosimile quindi) e, secondo altri, a una stimolazione di quelli adrenergici, dovuta a una scarica adrenalinica, fatto questo che spiegherebbe anche l’ipertensione che accompagna l’azione respiratoria.
Bjorkman (45) avrebbe invece osservato che la lobelina non é dotata di azione broncodilatatrice pur essendo capace di antagonizzare l’azione di alcuni broncocostrittori, quali la pilocarpina e l’arecolina.
Lendle e Richter (46) hanno confermato l’azione spasmolitica della tintura di Lobelia iniettata endovena in gatti resi sperimentalmente asmatici. Gli AA. notarono però che né la lobelina, né altri 8 alcaloidi della Lobelia, si dimostrarono attivi, mentre l’isolobinina dimostrò di essere dotata della stessa azione dell’adrenalina.
La tintura di Lobelia somministrata per os non ha azione spasmolitica ma agirebbe come emetico indiretto per eccitazione delle terminazioni emetico-sensitive della mucosa gastrica.
Winterstein e Wiemer (47) hanno iniettato nella cisterna magna di 57 gatti e di 6 conigli, dopo denervazione chirurgica dei chemiocettori, una soluzione di Ringer contenente 0,45 mg di lobelina oppure 0,05-0,075 mg di cianuro di sodio e hanno notato che tanto la lobelina (nel 23% dei casi), quanto il cianuro di sodio (nel 48% dei casi), determinano un aumento reversibile del volume respiratorio.
Tale risultato sarebbe dovuto, secondo gli AA., a un effetto specifico delle due sostanze e non avrebbe alcuna relazione né con la tensione del CO2 né col pH della soluzione.
L’edema polmonare provocato nei ratti esponendoli a vapori di cloropicrina, é prevenuto dalla lobelina somministrata con iniezioni endoperitoneali alla dose di 30, 20, 15 e 10 mg/kg, praticate a 5’ di intervallo e iniziando immediatamente dopo l’esposizione.
L’ipofisectomia o la surrenale-medullectomia, non interferiscono, ma la protezione manca nei ratti surrenalectomizzati, a meno che a essi non vengano somministrati 5-100 mg di cortisone sottocute, 6 h prima della esposizione.
La protezione dei ratti surrenalectomizzati può essere ottenuta con lobelina, anche se precedentemente trattati con l-naftilurea, con cloruro di ammonio o con adrenalina.
La protezione con lobelina contro l’edema polmonare manca anche nei ratti, allorché la corteccia surrenalica venga stimolata con aldeide formica o in quelli cui venga somministrata corticotropina, desossicorticosterone o cortisone in dosi elevate.
Dopo vagotomia cervicale bilaterale, i ratti non rispondono più alla lobelina.
Quantunque la corteccia surrenalica intatta sia essenziale per la protezione contro l’edema polmonare mediante somministrazione di lobelina, il cortisone avrebbe un ruolo coadiuvante ma non rappresenterebbe un essenziale regolatore dell'azione [Almagyi e coll. (48)].
Il meccanismo di azione della lobelina é stato indagato anche da Marro (49) su cavie in diverse condizioni sperimentali: giovani e adulte, normali e a vario grado di ipotermia, a pressione barometrica normale e in alta montagna. In accordo con altri autori Marro conclude che la lobelina esplica la sua azione sulla funzione respiratoria, in via riflessa, mediante vie afferenti vagali.
Il centro bulbare del vomito viene eccitato direttamente dalla lobelina allorché essa venga somministrata a dosi piuttosto elevate, ma la lobelanina e la lobelanidina, sono sotto questo aspetto più attive.
Sulle stazioni gangliari vegetative la lobelina determina, come abbiamo precedentemente accennato, un’azione nicotinosimile, eccitandole prima e paralizzandole poi. Altrettanto avviene sulla muscolatura scheletrica, sulla quale la lobelina, a dosi elevate, manifesta un’azione curarica.
Konzett (50) ha studiato l’effetto della lobelina sul ganglio cervicale superiore del gatto, perfuso isolatamente secondo il metodo di Kibjakow e ha constatato che a piccole dosi (da 0,1 a 0,5 g) la lobelina sensibilizza il ganglio all’azione dell’acetilcolina. A dosi medie (da 1 a 10 g) la lobelina eccita direttamente le cellule gangliari.
Dosi elevate (superiori a 10 g) determinano una stimolazione iniziale seguita da un effetto paralizzante ma reversibile. Gli effetti eccitanti e paralizzanti della lobelina sulle cellule ganglionari sinaptiche, sarebbero meno marcati di quelli dovuti alla nicotina.
Donzelot e Milovanovich (51) hanno dimostrato che l’applicazione del cloridrato di lobelina sulla superficie esterna del cuore di rana in situ, determina regolarmente, un rallentamento considerevole del ritmo, con effetti cronotropi e dromotropi.
Lo studio della portata cardiaca nell’unità di tempo, effettuato con la tecnica della diagrafia ad alta frequenza, mostra che questo rallentamento é accompagnato da un aumento importante della portata/secondo, della durata di 2 h. Una nuova applicazione di lobelina praticata 2 h dopo la prima, determina un’ulteriore bradicardia ma, questa volta, con flessione della portata/secondo, dovuta al rallentamento eccessivo del ritmo che può discendere al di sotto di 1/3 del suo valore normale.
Un impiego della lobelina a scopo diagnostico, é quello preconizzato da Tepslow e Schor (52) i quali hanno notato che l’iniezione endovenosa rapida, di lobelina, determina dopo qualche secondo, una breve apnea e un accesso di tosse irresistibile.
Il metodo venne successivamente descritto da diversi autori fra i quali Masbernard e coll. (53) e Stanojevic (54) secondo cui, somministrando endovena da 0,04 a 0,07 mg/kg di lobelina, si ottiene dopo 10”,6 in media nei soggetti sani, dopo 14” in media nei cardiaci senza segni di insufficienza e dopo 30”,3 in media negli asistolici, una tosse riflessa che indica l’effetto ottenuto con la lobelina (tempo di circolazione o velocità circolatoria).
Con questo metodo che si vale della lobelina per provocare un riflesso involontario, si otterrebbero risultati più sicuri che con quelli che si basano sulla somministrazione di sostanze sapide (decolin, saccarinato di sodio), nei quali interferisce la capacità di percezione del soggetto e la sua volontà di marcare il momento dell’effetto.
Secondo le più recenti concezioni si ammette che il riflesso tussigeno è strettamente connesso con l’azione della lobelina a livello del glomo carotideo. Con questo metodo si misura quindi, il tempo che impiega la lobelina per compiere il tragitto dal punto in cui viene iniettata (vena basilica in generale), al glomo carotideo.
Nel valutare il tempo di circolazione, che rappresenta una costante fisiologica, occorre tener conto del fatto che esso si eleva regolarmente e parallelamente con l’età ciò che esprime il rallentamento delle funzioni cardiovascolari [Herbenval e coll. (55)].
I casi che controindicano l’applicazione di questo metodo sono piuttosto rari e comprendono l’emottisi recente, gli interventi addominali recenti, l’infarto miocardico, l’edema polmonare acuto e recente e la tachicardia ventricolare.
Alcuni rilievi critici sull’impiego di questo metodo per la misura del tempo di circolazione, sono stati fatti da Gastelmand e Bruneau (56). Questi AA. comparando i risultati da essi ottenuti (57-58), con quelli di Herbenval e coll. (55), fanno osservare che se è vero che il tempo di circolazione tende ad aumentare nei soggetti in età avanzata, ciò non avviene in tutti i casi.
In secondo luogo gli AA. osservano che in base alle loro esperienze, che riguardano 1500 osservazioni, il tempo medio di circolazione nei soggetti normali indicato da Masbernard e coll, (l.c.) è troppo elevato e tale da dover essere considerato patologico, in quanto molto vicino a quello rilevabile nei cardiaci scompensati. Queste differenze possono provenire secondo gli AA., dalla concentrazione della soluzione di lobelina, dalla freschezza di queste soluzioni, dal luogo e dal punto di iniezione, particolari questi già valutati e discussi dagli AA. i quali infine, osservano che se tutti gli autori sono concordi nel ritenere che la sede del riflesso tussigeno sia situata nel seno-carotideo, certi fatti da essi osservati li inducono a ritenere che questo riflesso provenga dalla piccola circolazione, pur senza negare l’esistenza di un «relais» seno-carotideo.
Un altro impiego della lobelina è quello che è stato tentato, ma con risultati non brillantissimi, nella desassuefazione all’uso del tabacco.
Secondo Kushinsky (59) si otterebbe in questi casi, un risultato con la somministrazione di dosi singole di 8 mg per os, dose che se necessario, può essere ripetuta parecchie volte durante i primi giorni e gradualmente ridotta nel corso di una settimana.
Questo trattamento però determina, non raramente, effetti secondari consistenti in vertigini, malessere, inappetenza ecc.
Rapp e Olen (60) consigliano la somministrazione di 2 mg di lobelina associata a deboli antiacidi. Gli AA. hanno notato che l’80% dei soggetti su cui hanno sperimentato, si astenevano dal fumo dopo 5-6 giorni di trattamento, in confronto al 10 % ai quali era stato somministrato un placebo oppure solfato di lobelina senza antiacido.
Molto saggiamente gli AA. aggiungono però, che il solfato di lobelina in associazione con l’antiacido, ha il merito di aiutare ad astenersi dal fumo «specialmente se il soggetto ha il desiderio di smettere di fumare»…. Il quale fatto lo si può anche più facilmente comprendere se si considera che Bartlett e Whitehead (61) i quali nel corso di uno studio sulla desassuefazione al fumo condotto su 33 studenti di medicina, non hanno osservato alcun effetto nè con la somministrazione di mepabromato alla dose di 400 mg al giorno, nè somministrando un preparato di lobelina in associazione con un antiacido (lo stesso impiegato dagli AA. precedentemente citati), tre volte al giorno.
Da altre prove condotte dagli stessi AA. su 15 studenti cui veniva somministrato o mepabromato o un placebo, è risultato che sia l’uno che l’altro determinavano gli stessi effetti. In 6 su 7 soggetti inoltre, gli AA. constatavano che il placebo era ugualmente efficace nel sopprimere o nel diminuire il desiderio di fumare.
Terapia – La Lobelia è usata in terapia sotto forma di estratto fluido, di tintura o di sigarette, soprattutto nel trattamento dell’asma, nel qual caso viene frequentemente associata a droghe atropiniche (Stramonio specialmente). Impiegata a dosi opportunamente elevate, la Lobelia può risolvere completamente un accesso asmatico.
Essa è usata anche come espettorante nelle bronchiti catarrali e specialmente in quelle spastiche e anche nella pertosse. Non deve però essere mai impiegata come emetico.
La lobelina si usa alla dose di 10-20 mg per via sottocutanea o intramuscolare e alla dose di 3 mg per via endovenosa, negli stati di depressione respiratoria prodotta da agenti depressivi (morfina, ipnotici) o da altre cause patologiche (polmonite, stenosi laringea), o nell’asfissia dei neonati. In quest’ultimo caso, si possono ottenere buoni risultati secondo Lònne (62), praticando una pressione ripetuta sulla vena ombelicale, mentre il bambino viene tenuto in posizione declive e iniettando contemporaneamente un preparato a base di lobelina, Simpatolo e Cardiazolo, a dosi più o meno elevate a seconda della gravità del caso.
La stimolazione respiratoria prodotta dalla lobelina è in ogni caso, piuttosto transitoria e non supera di solito la durata di mezz’ora o un’ora ed è frequentemente seguita da nausea e da vomito, a volte da collasso più o meno grave e da respirazione di Cheyne-Stokes [Norris e Weiss (63). Marshal (64)].
Un’azione bronchiodilatatrice più rapida, più efficace e più duratura, la si può ottenere secondo Dautrebande (65), con una soluzione di un sale di lobelina (cloridrato o solfato), in associazione con un anestetico locale (novocaina, cocaina), somministrata per aerosol.
A questa soluzione possono essere associate, ove lo si ritenga utile, altre sostanze (atropina, stricnina, guaiacolo, solfoguaiacolato di potassio, glicole etilenico, penicillina) ed è impiegabile nel trattamento
Franck (66) richiama l’attenzione sull’azione, precedentemente ignorata, della lobelina nel trattamento dell’orticaria. Egli sperimentò su di un caso grave che non aveva reagito al trattamento abituale ed osservò che dopo due iniezioni sottocutanee di g 0,01 il primo giorno e un’iniezione il giorno seguente, tutte le manifestazioni dell’orticaria e di tossicosi generale scomparvero completamente. La lobelina si dimostrò attiva anche in numerosi altri casi di orticaria di varia origine. L’A. riferisce che a volte furono sufficienti 3-8 iniezioni di g 0,003 di lobelina, mentre a volte si dovettero somministrare dosi di g 0,01.
Assorbimento – Rapp e coll. (67), valendosi di un micrometodo per la determinazione della lobelina nel sangue deproteinizzato, trovarono che essa, sotto forma di solfato e somministrata per os in eccipiente amidaceo, è assorbita lentamente. Le prove furono eseguite in 50 soggetti d’ambo i sessi, di età compresa fra i 21 e i 48 anni e tutti fumatori abituali. Il solfato di lobelina veniva invece prontamente assorbito se somministrato in veicolo di carbonato di magnesio.
Tossicologia – Le foglie e le capsule di Lobelia a dosi elevate, determinano vomito, nausea e tremito generale. In forti dosi il vomito si intensifica e la nausea è continua; compare inoltre sudorazione copiosa e senso di rilasciamento generale.
Le dosi tossiche determinano l’aggravamento della sintomatologia suddetta cui si aggiunge senso di bruciore alle fauci o all’esofago, perdita progressiva dei movimenti volontari, pulsazioni deboli e frequenti, caduta della temperatura e infine, collasso con stupore e coma. In alcuni casi la morte è preceduta da fatti convulsivi [Osol-Farrar (35)].
Le alterazioni cardiocircolatorie si manifesterebbero, secondo Curtis e Wright (68), con un rallentamento del polso, con considerevole caduta della pressione iniziale e con successivo ritorno ai valori normali. Forti dosi determinano acceleramento del polso, marcato abbassamento della pressione e iperpnea dovuta alla stimolazione dei chemiocettori glomocarotidei, effetto transitorio questo, che non supera la durata di 10’. Nel caso in cui il centro respiratorio sia stato depresso con cloralio o morfina, tale effetto stimolante sulla respirazione, sarebbe relativamente debole. Da Forster e coll. (44) venne riscontrata anche una dilatazione bronchiale.
Estratti e preparati vari
a) Estratto fluido per tintura (g 1 = XLVIII gtt).
Dosi: da IV a XX gtt pro dose.
b) Estratto fluido per sciroppo (g 1 = XLV gtt).
Dosi: da IV a XX gtt pro dose.
c) Estratto molle acquoso (1 p. = 6 p. circa di droga).
Dosi: g 0,03-0,06 pro dose.
d) Tintura F.U. al 10% di droga.
Dosi: g 1 -3 pro dose.
Preparazioni usuali e formule galeniche
Tintura F.U.
Estratto fluido lobelia per tintura……………………………….. g 10
Alcool di 70° …………………………………………………… g 90
(g 1-3 pro dose).
Sciroppo
1) Tintura lobelia F.U……………………………………………………. g 5
Sciroppo semplice F.U……………………………………………… g 95
(a cucchiaini).
2) Estratto fluido lobelia per sciroppo……………………… g 0,5
Sciroppo semplice F.U………………………………………………….. g 99,5
(a cucchiaini).
Calmante nell'asma
Tintura lobelia F.U……………………………………………………. g 10
Tintura giusquiamo F.U…………………………………………….. g 10
Sciroppo diacodio…………………………………………………………. g 40
Sciroppo semplice q. b. per…………………………………….. g 150
(1 cucchiaino ogni 3-4 ore).
Gocce antiasmatiche
Tintura lobelia F.U.
Tintura oppio
Tintura giusquiamo F.U……………………………………….. ana g 10
(XX-XXX gtt pro dose).
Pozione nell’asma infantile
Estratto fluido lobelia g 1
Estratto fluido grindelia g 1
Sciroppo arancio…………………………………………………….. g 40
Acqua anice……………………………………………………………. g 60
(a cucchiai).
Sciroppo nella pertosse
Tintura lobelia F.U………………………………………………….. g 20
Sciroppo belladonna…………………………………………………. g 25
Sciroppo balsamo tolù g 75
Alcool di 95°
Glicerina……………………………………………………………… ana g 20
(a cucchiaini).
BIBLIOGRAFIA
(1) PROCTER, Am. J. Pharm., 9, 98, 1836 • (2) WlELAND H., Arch. exp. Path. u. Pharmakoi., 79, 95, 1915; Ber., 54, 1784, 1921 – (3) WIELAND H., SCHOEPF C. e HERMSEN W., Lieb. Ann., 444, 40, 1925 – (4) WIELAND H. e DRAGENDORFF O., Lieb. Ann., 473, 83, 1929 • (5) WIELAND H. e DRISHAUS I., Lieb. Ann., 473, 102, 1929 – (6) WIELAND H., KOSCHARA W. e DANE E., Lieb. Ann., 473, 118, 1929 –
(7) WIELAND H., SCHEUING G. c WINTERHALDER L., Lieb. Ann., 473, 126, 1929 – (8) WIELAND H., ISHIMASA M. c KOSCHARA W., Lleb. Ann., 491, 14, 1931 – (9) WIELAND H., SCHOEPF C. c LEHMANN G., Lieb. Ann., 518, 12, 1935 – (10) WIELAND H. c THOMAE O., Lieb. Ann.,.540, 99, 1939 –
(II) WIELAND H., KOSCHARA W., DANE E., RENZ J., SCHWARZE W. c LINDE W., Lieb. Ann., 540, 103, 1939 – (12) SCHOEPF C., KAUFMANN T., BERTH P., BUNDSCHUH W., DUMMER Q., FETT H., HABERMEHL G., WIETERS E. e WUST W., Lieb. Ann., 608, 88, 1957 – (13) DUMMER G., Diplomarbeit, Darmstadt, 1950; Dissertation T. H., Darmstadt, 1954 – (14) MARION L., LAVIGNE R. c LEMAY L., Can. J. Chem., 29, 347, 1951; Chem. Abs., 46, 8128, 1952 – (15) MASCRÉ M. e CARON M., Bull. sci. pharm., 37, 657, 1930 • (16) MASCRÉ M. c CARON M., Bull. sci. pharm., 40, 519, 1933 –
(17) CORRELA DA SILVA, Lobelia urens. Ensaios sòbre a sua ac^ao fisiologica, Università Porto, 1944 –
(18) CORREIRA DA SILVA, Nota sÒbre a riqueza alcaloidka da Lobelia urens, 1943 – (19) MASCRE M. c GENOT H., BuH. sci. pharm., 39, 165, 1932 • (20) STEINEGGER E., Pharm. Acta Helv.. 23, 1, 1948; Svensk Farm. Tidskr., 65, 841, 1961 – (20a) POLLACCI G., Fitoterapia, 32, n. 2, 9, 1961 – (21) KALASHNIKOV V. P., Farmatsiya, n. I, 20, 1939; Chem. Abs., 34, 4227, 1940 – (22) ESDORN I., Hell. u. Gewurz-Pfianzen, 19, J, 1940; Chem. Abs., 36, 6309, 1942 – (23) RAMSTAD E., Pharm. Acta He/v., 28, 45, 1953 – (24) KRONE W.,Pharmazie, 15, 502, 1960- (25) WINKLER L. W., Pharm. Zentralh., 73, 614, 1952 • (26) KOCH, Pharmakognostischer Atlas, Lcipzig, 1914, p. 153; citato da WALLIS, !oc. cit. (33) • (27) FLUCK, SCHLUMPF c SIEGFRIED, Pharmakognostischer Atlas, Basel, 1935, p. 260; citato da WALLIS,
loc. cit. (33) – (28) ZOERNIG., Tabellen fur das Pharmakognostische Praktikum, Berlin, 1925, p. 77 •
(29) GILG, BRANDT e SCHUERHOFF, Lehrbuch der Pharmakognosie, 4 ed., Berlin, 1927, p. 434 –
(30) KARSTEN e BENCKE, Lehrbuch der Pharmakognosie, 4 cd., Jena, 1928, p. 222 – (3J) GATHER- COAL e WIRTH, Pharmacognosy, 3 ed., London, 1956, p. 433 – (32) TREASE, Textbook of Pharmaco- gnosy, 3 ed., London, 1952, p. 761 – (33) WALLIS T. E., J. Pharm. Pharmacol., 9, 663, 1957 – (34) British Pharmacopoeia, 1932, p. 275 – (35) OSOL A. e FARRAR G., The Dispensatory of tbc U.S.A., 25" ed., 1955, p. 768 – (36) SOLLMANN T., A Manual Pharmacology, Sauders Comp. Ed., Phyladclphia- London 1950, p. 352 – (37) EDMUNDS, Am. J. Physiol., 11, 79, 1904 • (38) HEYMANS C., BOUCKAERT J. J. e DAUTREBANDE L., C.R. Soc. Biol., 106, 469, 1931 – (39) PENNA M. e AVIADO D. M., Arch. intern. pharmacod et de thh., 140, 269, 1962 (40) DRESER H., Therap. Monatsh., 4, 1890 – (41) GNUS P., Arch. intern. pharmacod. et de thér., 32, 1926 • (42) CURTIS e WRIGHT, Lancet, 211, 1255, 1926 – (43) WIELAND e MAYER, cit. da SOLLMANN I.c. (44) FORSTER e coll., J. Pharmacoi. exp. Ther., 87. 73, 1946 – (45) BJORKMAN, C. R. Soc. Biol., 94, 947, 1926 • (46) LENDLE e RICHTER, Klin. Woch.. 28, 665, 1950 . (47) WINSTERSTEIN H. e WIEMER W., Arch. exp. Path. u. Pharmakol., 235, 235, 1959 – (48) HALMAGYI D. F. J., KOWACS A. e NEUMANN P., Disease of Chest, 33, 285, 1958; Chem. Abs.. 53. 3475a, J959 – (49) MARRO F., Boli. soc. it. biol. sper., 27, 1362, 1951 e 27, 1420, 1951 – (50) KONZEIT H., Arch. intern. pharmacod. et de thér., 85, 446, 1951 (51) DONZELOT E. e MILOVA- NOVICH J. B., Soc. Biol., 10, 7, 1954; ree. in Presse Méd., 62, 52, 1100, 1954 • (52) TEPSLOW e SCHOR, cit. in Presse Méd., 61, 58. 1170, 1953 • (53) MASBERNARD A., DELESTRAC M. e CAMELIN A., Ann. de méd., 54, 228, 1953 – (54) STANOJEVIC L., Presse Méd., 57, 77, 1135, 1949 – (55) HERBEN- VAL R., CUNY G., LARCAN A. e TENETTE M., Presse Méd.. 65, 67, 1498, 1957 – (56) GASTELMAND R. e BRUNEAU J., Presse Méd, 65. 81, 1827, 1957 • (57) GASTELMAND R. e BRUNEAU J., Semaine hÒp., 27, 29, 1951 – (58) BRUNEAU J., Thése de Paris, 25 giugno 1952 – (59) KUSCHINSKY G., Disch.
med. Woch.. n. 1, 41, 1953 – (60) RAPP G. W. e OLEN A. A., Am. J. Med. Sci., 230, 9, 1955 – (61) BARTLEIT W. A. e WHITEHEAD J., J. Lab. C/in. Med., 50, 278, 1957 – (62) LONNE F., Zbl. Gynak., n. 45, 1690, 1943 – (63) NORRIS W. H., c WEISS, J. Pharmacoi. exp. Ther., 31, 43, 1927 – (64) MARSHAL W. R., Arch. int. med., 42, 180. 1928 – (65) DAUTREBANDE L., U. .S. patcnt 2.594.296, 29 aprile 1952. Chem. Abs., 46, 6797, 1952 – (66) FRANCK G., Schweiz. med. Woch., n, 37, 1120. 1943 – (67) RAPP G. W., DUSZA B. T. e BLANCHET L., Amer. J. Med. Sci., 237, 287, 1959 – (68) KURTIS e WRIGHT, Lancet, 211, 1255, 1926.

