Oleandro
Tratto da “Piante Medicinali – Chimica, Farmacologia e Terapa” di R. Benigni, C. Capra e P.F.Cattorini
(Nerium Oleander L. – Fam. Apocinacee/Hechitoidee/Hechitidee) (Sin. – Nerium laurifolium Lamk.)
Oleandro- Ultimo aggiornamento pagina: 27/02/2018
Indice dei contenuti
- Generalità
- Componenti principali
- Proprietà farmacologiche
- Estratti e preparati vari
- Preparazioni usuali e Formule
- Bibliografia
Generalità

Etimologia – Nerium, dal greco nhrion = da nhros = umido, per la stazione abituale presso le acque.
Oleander – verrebbe per la somiglianza (?) delle sue foglie con quelle dell’Olivo (Olea) (Mérat). Questa somiglianza è però lontana.
(L’antica denominazione era Rhododendron: Rhododendron flore rubro et albo I. B. Ray, Nerion floribus rubescentibus G. Bauh., Nerion seu Rhododendron flore rubro J. Bauh.).
Rhododendron, dal greco rodon = rosa e dendron = albero, cioè albero che ha i fiori rosei).
laurifolium – che ha le foglie somiglianti (?) a quelle del Lauro.
Nomi volgari – Leandro, rosagine, osalauro, mazza di S. Giuseppe, alloro d’india, ecc. (tosc.), belladonna (da non confondere con l’Atropa), bell’omo, sciù d’or (lig ), velen dij rat (piem.), alandru, ecc. (sic.), leonaxi, sabadiglia (da non confondere con Schoenocaulon) (sard.), Olander(ted.), laurier rose, ecc. (fr.), adelfa (spagn.), defla (arab.), hitia (Cabiria, Algeria), alili (berb.), kay dao le (indoc.), kamir (ind.), trùc dào (Vietnam), leànder (ungh.), ecc.
Habitat – Spontaneo nell’Europa meridionale, regione e isole mediterranee, sino alla Crimea, Africa del nord, Europa centrale. India, Indocina, Reunion, Martinica. In Italia nei luoghi umidi e sassosi, lungo i corsi di acqua, nel greto dei torrenti (Lago di Garda, Liguria, M. Argentaro, Salernitano, Puglie, Basilicata, Calabria, grandi isole, Is. del Giglio, Capraia), lungo le spiagge marittime.
Estesamente coltivata nei giardini, lungo i viali, talora inselvatichita.
Arboscello o piccolo albero (2-5 m.).
Parti usate – Le foglie.
Componenti principali
Numerosi glucosidi digitaloidi nelle foglie (1-7), nei semi (8), nel pericarpo (7) e nei fiori (7). Nelle foglie sono stati identificati i seguenti glucosidi e genine con struttura steroidica: oleandrina (1-6), desacetil-oleandrina (5), gitossigenina (7), strospeside (7), 16-anidro-strospeside (7), digitalinum verum (7), adinerina (5) (9-13a), neriantina (11) (12), digitossigenina (7), odorosidi A, B e H (7), odorobioside G (7) (14), odorotrioside G (7) (14) (15), odorobioside K (7) (14) (17), odoroside K (odorotrioside K) (7) (16) (17). Inoltre un glucoside amorfo, neriina, scindibile con liberazione di glucosio (18).
Mediante analisi cromatografica su carta sono stati separati glucosidi complessi, probabilmente monogluco-oleandroside (19) e digluco-oleandroside della oleandrigenina (19) (20), digluco-oleandroside della adinerigenina, triglucoside della neriantina ed un quarto che potrebbe essere un triglucoside della gitossigenina (= nerioside?) (20).
Oleandrina (folinerina), C32H48O9, separata dalle foglie del Nerium Oleander in forma non pura da Lukowski sin dal 1861 (1), fu riconosciuta come glucoside da Schmiedeberg (2) ed ottenuta pura da Windaus e Westphal (3). Fu estratta dalle foglie con il nome di folinerina da Flury e Neumann (4), ma identificata poi all'oleandrina dallo stesso Neumann (5) e da Tschesche (6). Per idrolisi l’oleandrina (I) si scinde in oleandrigenina (monoacetil-gitossigenina), C25H36O6, ed in una molecola di L-oleandrosio, C7H14O4 (5) (6).
Desacetil-oleandrina. C30H46O8, è stata ottenuta dalle foglie del Nerium Oleander L. nel 1957 da Neumann (5), che ne ha determinato i prodotti di idrolisi: gitossigenina C23H34O5 + 1 mol. L-oleandrosio, C7H14O4.
Strospeside (desgluco-digitalinum verum), C30H46O9, così denominato da Reichstein e coll. (16) (21), che l'hanno estratto dapprima dai semi dello Strophanthus speciosus Ward et Harv. e dello S. bovinii Baill., è stato trovato nelle foglie del Nerium Oleander da Turkovic (7). E’ la 3-D-digitalosido-gitossigenina (II).
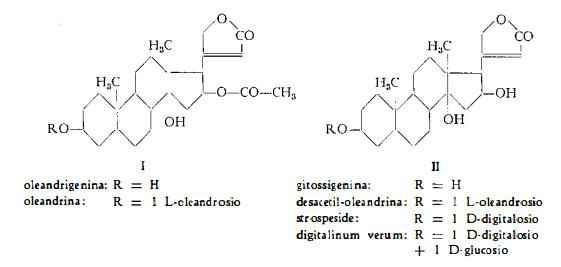
16-Anidro-strospeside (15) (16) [ 16-anidro-desglucodigitalinum verum (22)], C30H44O8, ottenuto per la prima volta da Hunger e Reichstein (22) con processo enzimatico dai semi dell’Adenium multiflorum Kl., è stato identificato per via cromatografica nelle foglie del Nerium Oleander da Turkovic (7).
Digitalinum verum, C36H56O14, già estratto dai semi e dalle foglie della Digitalis purpurea L. e della Digitalis lanata Ehrh, è stato trovato anche nelle foglie del Nerium Oleander L. da Turkovic (7) nel 1959. E' un glucoside difficilmente idrolizzabile che, per energica scissione idrolitica, produce, insieme con gli zuccheri componenti (1 mol. D-digitalosio + 1 mol. di D-glucosio), non l’aglucone originale, che è la gitossigenina, C23H34O5, bensì dianidro-gitossigenina, C23H30O3 (23).
Adinerina, C30H44O7, estratta da Neumann (5) dalle foglie del Nerium Oleander L., è risultata essere un glucoside non cardioattivo, che per idrolisi si scinde in una molecola di D-diginosio, C7H14O4 (9) e nell’aglucone adinerigenina, C23H32O4 (5). La struttura della adinerigenina è stata oggetto degli studi di Tschesche e coll. (9-12), di Cardwell e Smith (13) e di Reichstein e coll. (13a). Questi ultimi (13a), dall’esame dei prodotti di degradazione e di sintesi parziale della adinerigenina, hanno dedotto per questa la formula strutturale (IV) e per l’adinerina quella (V) di b-D-diginoside della adinerigenina.
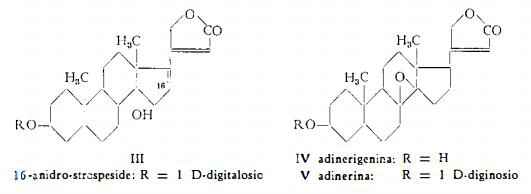
Neriantina, C29H42O9, isolata da Tschesche, Bohle e Neumann (11) dalle foglie dell'Oleandro, è stata identificata con la 3-D-glucosido-neriantogenina, C23H32O4, (VI). Si tratta di un glucoside non cardioattivo.
Odoroside A, C30H46O7, D-diginoside della digitossigenina (VII), già noto come componente della corteccia del Nerium odorum Sol. per merito delle ricerche di Rangaswami e Reichstein (15), è stato riconosciuto tra i monosidi delle foglie del Nerium Oleander, identificati da Turkovic (7) mediante esame cromatografico.
Odoroside H, C30H46O8, D-digitaloside della digitossigenina (VII), già ricavato dalla pianta dello Strophanthus gracilis K. Schurn. et Pax., come anche dalle foglie della Digitalis purpurea, è stato riconosciuto presente nelle foglie del Nerium Oleander per opera di Turkovic (7).
Odorobioside G, C36H56O13, ottenuto in un primo tempo, in forma di monoacetato, per idrolisi parziale dell’odorotrioside G (14), è stato poi trovato come prodotto naturale nelle foglie del Nerium Oleander L. (7). Il monoacetato è composto dell'aglucone digitossigenina, C23H34O4, di una molecola di acetil-digitalosio e di una molecola di glucosio: è cioè un b-D-glucosido-monoacetil-b-D-digitaloside della digitossigenina (VII) (14).
Odorotrioside G (odoroside G), estratto in forma di monoacetato, C44H68O19, per la prima volta dalla corteccia del Nerium odorum (15), e stato poi isolato anche dalle foglie del Nerium Oleander L. (7). Il monoacetato dell’odorotrioside G è costituito dall’aglucone digitossigenina, unito con una molecola di D-digitalosio, con due molecole di D-glucosio e con un gruppo acetilico fissato al digitalosio (14); è cioè la 3-b-D-glucosido-b-D-glucosido-monoacetil-b-D-digitalosido-digitossigenina (VII).
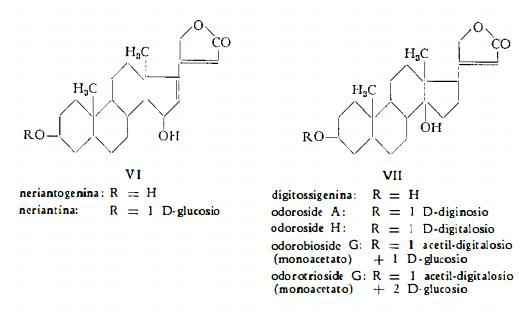
Odoroside B, C30H46O7, estratto in un primo tempo dalla corteccia del Nerium odorum Sol. ed identificato alla 3-D-diginosido-odorigenina B ( = uzarigenina, 5-allo-digitossigenina) (VIII) ( 15) (24), è stato poi trovato da Turkovic (7) tra i componenti del Nerium Oleander L.
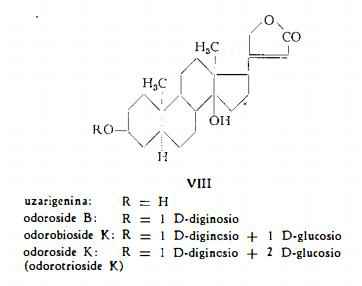
Odorobioside K [3-b-D-glucosido-b-D-diginosido-uzarigenina (VIlI)], C36H56O12 (17), è stato ottenuto per idrolisi parziale dell’odoroside K e trovato anche in forma libera nella corteccia del Nerium odorum (17) e nelle foglie del Nerium Oleander L. (7).
Odoroside K (odorotrioside K), C42H66O17, isolato dalla corteccia del Nerium odorum ed identificato con la 3-b-D-glucosido-b-D-glucosido-b-D-diginosido-uzarigenina (VIlI) (16) (17), è stato messo in evidenza anche nelle foglie del Nerium Oleander L. (7).
Il principale componente glucosidico è l'oleandrina, che è stata trovata nelle foglie essiccate in quantità pari sino allo 0,11 % (25) ed anche allo 0,5% in foglie di provenienza italiana, in cui l’oleandrina è risultata costituire circa il 90 % dei glucosidi cardiotonici (19). Le foglie contengono anche quantità notevoli di digitalinum verum (7).
Dalla determinazione dei glucosidi cardiotonici delle foglie secche, eseguita mediante il metodo di Knaffl-Lenz sulla cavia, usando oleandrina cristallizzata come campione di confronto (26), si è rilevato un titolo medio dello 0,5%, espresso in oleandrina (27).
Nelle foglie del Nerium Oleander L. sono state inoltre identificate le seguenti sostanze:
— i flavonoidi rutina (28-30) e 3-ramnosido-glucosido-canferolo (29) (30). Il 90% della frazione flavonica è costituita da rutina (19);
— gli acidi ossalico, malico, citrico, succinico (31), ursolico (7) (32) e oleanolico (7);
— zuccheri 0,706% (33);
— dambonitolo (etere 1,3-dimetilico del mesoinositolo), C8H16O6 (34);
— carotene (tracce) (33);
— vitamina C 40 mg % (33);
— vitamina K (tracce) (33);
— tannino catechico (35);
— lipidi 4,05%. (33) ;
— olio etereo 0,025 % (36).
Umidità 6,1%; ceneri 10,54%. Assenza di glucosidi antracenici, di saponine, di vitamine A, D, E, P e PP (33).
Proprietà farmacologiche ed impiego terapeutico
L’Oleandro come pianta tossica era nota sin dall antichità. Plinio, Galeno, Dioscoride conoscevano la tossicità delle foglie e dei fiori di Oleandro per gli animali che se ne cibavano e quella dell’acqua in cui i fiori sono stati in macerazione. Ignota era invece l’azione che questa pianta ha sul cuore, azione che venne individuata soltanto dopo la metà del secolo scorso con le ricerche di Lukowski (37) che forse per primo ne studiò l’azione farmacologica.
A queste prime ricerche seguirono quelle di Pelikan (38), di Schmiedeberge (39), di Pouloux (40-41), di Oefele (42): quelle cliniche di Magnanini (43) e quelle relativamente più recenti di Galli (44) eseguite per lo più sulla droga e moltissime altre farmacologiche e cliniche, fra le quali ricorderemo quelle di Windaus e Westphal (45), di Heubner e Nyary (46), di Bauer e Fromherz (47), di Flury e Neumann (48), di Schwab (49), di Hosslin (50), di Schuler e Ott (51), di Heuler (52), di Castelle-Roth (53) e di molti altri, alcuni dei quali verranno ricordati in seguito.
Dal complesso di queste ricerche farmacologiche e cliniche, la maggior parte delle quali vennero eseguite impiegando il glicoside oleandrina o folinerina, risultò chiaramente che all'Oleandro e al suo principio attivo principale, l’oleandrina, poteva essere attribuita un’azione cardiotonica, bradicardizzante e diuretica di tipo digitalico.
Per quanto lo studio dell’oleandrina non sia stato condotto così a fondo come quello di altri glicosidi digitalici, si può presumere che il suo meccanismo di azione sia fondamentalmente simile a quello già descritto per la Digitale (ved. Digitale), dalla quale differirebbe soprattutto per un’azione più pronta, per una più rapida eliminazione e quindi per una minor durata di azione, caratteristiche queste che avvicinerebbero i glicosidi oleandrici a quelli strofantinici e quindi ai digitaloidi di secondo tipo.
Un estratto di foglie di Oleandro, molto depurato e titolato biologicamente, venne studiato sperimentalmente da Osterwald (54), che ne dimostrò la grande tollerabilità e l'ampio margine terapeutico.
Secondo Schindel e Braun (55), la foliandrina (identificabile con la oleandrina), differisce nettamente dagli altri glicosidi isolati dalle varie specie di Oleandro. A prescindere dalle sue caratteristiche chimiche, essa si distinguerebbe per le sue proprietà farmacologiche che, anche secondo questi AA., permettono di considerare la foliandrina come un glicoside cardioattivo di tipo strofantinoide la cui attività può essere ritenuta intermedia fra quella dei glicosidi della Digitale e quelli dello Strofanto.
Iniettata endovena nel gatto, essa determina infatti, modificazioni elettrocardiografiche in tutto simili a quelle dovute ai glicosidi strofantinici, sui quali la foliandrina avrebbe tuttavia il vantaggio di esplicare una piena attività anche per somministrazione orale.
Prove comparative di attività di estratti fluidi preparati dalla corteccia e dalle foglie stabilizzate ed ottenuti per estrazione acquosa o alcoolica vennero eseguite da Astruc, Giroux e Hoarau (56). Questi AA. sperimentando sul cane, cui veniva registrata l’attività cardiaca, la pressione arteriosa e il volume renale, osservarono che la dose mortale nel cane cloralosato e in respirazione artificiale, differisce di poco impiegando i diversi estratti e che l’azione cardiocircolatoria dell'Oleandro è più affine a quella dello Strofanto che a quella della Digitale.
Giroux, Hoarau e Desbordes (57) studiando l'attività di diversi estratti di Oleandro sull’intestino isolato di coniglio, hanno potuto notare un effetto parasimpaticomimetico.
Lo studio farmacologico dell’Oleandro venne ripreso in Italia da Aiazzi-Mancini (58) durante la seconda guerra mondiale allorché, per la difficoltà di approvvigionamento della maggior parte delle droghe esotiche, sorse la necessità di studiare la loro sostituzione, per quanto possibile, con quelle indigene. Fu appunto con lo scopo di sostituire lo Strofanto di cui in quel periodo si lamentava l'assenza sui nostri mercati, che il suddetto A. diresse la sua attenzione sull'Oleandro che, fra le droghe digitaliche indigene, gli apparve quella che meglio potesse prestarsi a realizzare questa sostituzione.
I risultati delle sue ricerche confermarono l’azione digitalisimile dell’Oleandro e la possibilità di sostituirlo allo Strofanto del quale peraltro, si sarebbe dimostrato meno tossico.
Questi risultati vennero in seguito confermati da Cortesi (59) il quale, impiegando diverse preparazioni di Oleandro in una serie di controlli farmacologici, potè dimostrare che l'attività farmacodinamica di questa droga, si avvicina più a quella dello Strofanto che a quella della Digitale e che può costituire un cardiotonico di sostituzione o di mantenimento, come altre droghe digitaliche, quali l’Adonide e la Scilla.
L’attività dell’Oleandro e di alcuni suoi preparati galenici (infuso, tintura), venne studiata da Boriani (60) comparativamente con quella della Digitale e impiegando il metodo di Hanzlik sul piccione. I risultati ottenuti dimostrano che le foglie di Oleandro sarebbero dotate di un’attività di poco inferiore a quella del campione internazionale di Digitale e che la zona maneggevole, allorché vengano impiegate sotto forma di infuso, sarebbe tanto ampia da rendere questo preparato particolarmente adatto agli usi terapeutici.
La tintura sarebbe invece dotata di un più basso coefficiente terapeutico e raggiungerebbe una stabilità di titolo soltanto dopo un lungo periodo durante il quale la sua attività diminuirebbe però notevolmente. Si potrebbe dedurre da ciò che per la preparazione della tintura di Oleandro, come per tutte le preparazioni di questa droga che, a differenza dell'infuso, debbono essere conservate a lungo, deve essere impiegata la droga stabilizzata.
Sul cuore di embrione di pollo l'oleandrina agirebbe, secondo Wolfred (61), in maniera simile alla gitossina alla quale è legata da strette analogie chimiche.
La stessa azione digitalisimile venne dimostrata con esperienze eseguite sul muscolo papillare del cuore di gatto e su quello isolato dal miocardio di giustiziati, montati sul miografo di Loubatiéres (62-64) e ad analoghe conclusioni giunsero Sevilla e coll. (65) i quali sperimentarono su cuori isolati di gatto e di cane che sarebbero risultati più sensibili del cuore di rana all'azione dell'oleandrina.
Piccole dosi di oleandrina determinano un aumento dal 20 al 40 % del volume cardiaco, mentre dosi più elevate provocano una progressiva e rapida diminuizione accompagnata da aritmie. Con concentrazioni da 1:10000000 a 1:1000, si nota vasodilatazione mentre concentrazioni superiori determinano vasocostrizione.
Sull'utero isolato le piccole dosi inibiscono le contrazioni automatiche, mentre le dosi più elevate determinano un aumento del tono.
Secondo gli AA. l'oleandrina sarebbe indicata in ogni tipo di insufficienza cardiaca. L’assorbimento e la comparsa dell'azione sarebbero tanto rapidi da poter notare, già entro le prime 24 ore, l’effetto bradicardizzante e l'aumento della diuresi.
I risultati di più recenti ricerche eseguite da Aiazzi-Mancini (66) sull’azione di una sostanza glicosidica pura e cristallizzata estratta dall'Oleandro, hanno permesso di dimostrare che essa è certamente dotata di una attività digitalo-mimetica. In particolare essa esercita sul cuore di mammifero, sia in vitro che in vivo, sul cuore di rana e sul piccione, gli effetti caratteristici dei glicosidi digitalici di II ordine.
Secondo valutazioni preliminari comparative, la suddetta sostanza ha dimostrato di possedere un'attività inferiore del 20-30 % sul cuore isolato e del 40-50% in vivo sulla cavia e sul piccione, a quella della k-strofantina.
I risultati di queste prove permettono di attribuire al glicoside puro e cristallizzato ottenuto dall'A., gli effetti di tipo digitalico già notati dall’A. stesso sperimentando con l’estratto fluido (58), ad eccezione tuttavia dell'azione stimolante la diuresi da sovraccarico idrico e idrico-salino, ciò che potrebbe essere dovuto, secondo l’A., alla presenza nell’estratto fluido, di principi diversi dal glicoside ottenuto e dotati di una debole attività diuretica diretta.
Terapia – Per quanto riguarda l'impiego terapeutico, gli AA. sembrano concordi nel ritenere che l’Oleandro e il suo glicoside oleandrina sono dotati di un'azione intermedia fra quelle della Digitale e quella dello Strofanto e in tal senso si esprimono, fra gli altri, il già citato Castelle-Roth (53), Puglisi (67) che ha sperimentato l’oleandrina nella terapia pediatrica e Binder (68) il quale trovò anche che i glicosidi dell’Oleandro agiscono sull'E.C.G. nello stesso modo di quelli digitalici.
Se si eccettua un caso di bigeminismo transitorio, non furono mai osservati dall’A., disturbi del ritmo (extrasistoli in particolare), seguire l’azione dell’Oleandro. Su 71 casi trattati dall'A., soltanto 4 non reagirono al trattamento, 2 dei quali si mostrarono però refrattari anche alla terapia digitalica.
Prove cliniche con un preparato totale di Oleandro studiato farmacologicamente da Osterwald (54), furono eseguite da Hildebrandt (69), da Bansi (70), da Becker-Freiseng (71), da Lauer (72) e dimostrarono che il preparato può essere vantaggiosamente impiegato nel trattamento dei disturbi del ritmo, nell’insufficienza cardiaca da vizi valvolari e da affezioni miocardiche.
Un preparato pressocchè analogo, contenente cioè i glicosidi cardioattivi totali della foglia di Oleandro, venne sperimentato clinicamente da Pendl e Rossner (73), i quali lo trovarono dotato di una buona azione diuretica e di un minimo potere di accumulo, tanto da permettere di poter passare alla terapia strofantinica in qualsiasi periodo del trattamento lo si credesse opportuno.
L'oleandrina fu studiata clinicamente anche da Monquin e coll. (74), secondo i quali l'azione più notevole di questo glicoside sarebbe quella bradicardizzante, indice di un’azione vagotonica più pronta e più intensa di quella ottenibile con la digitalina. La sua azione diuretica, per quanto efficace, sarebbe al contrario, meno costante e meno duratura di quella dovuta alla Digitale. I risultati terapeutici più favorevoli si otterrebbero, secondo gli AA., nelle miocarditi con aritmia totale e, in particolare, nella insufficienza cardiaca dei mitralici.
Ravera (75) ha voluto controllare l'azione dell’oleandrina che fu sperimentata su 10 pazienti scompensati e su 5 individui sani che servirono di confronto.
Essa venne somministrata per os alla dose di mg 1,2 ogni 8 h, per 5 giorni. L’A. osservò che essa è ben tollarata e che i risultati clinici sono soddisfacenti. L'esame elettrocardiografico ha posto in evidenza alterazioni simili a quelle prodotte dalla Digitale, ma assai meno marcate, soprattutto per quanto riguarda il tratto ST-T. Alle dosi terapeutiche normali di carico, la somministrazione di oleandrina determina nei cardiopatici alterazioni elettrocardiografiche del tutto simili a quelle prodotte dalla Digitale ma inferiori come frequenza, intensità e durata, mentre negli individui sani, contrariamente a quanto avviene con la Digitale, le alterazioni sono più rare e meno intense.
In base ai risultati da lui ottenuti, l’A. crede di poter affermare che all’oleandrina compete un posto notevole fra i cardiotonici più importanti.
Con una sua nota successiva Mouquin (76) ha fornito ulteriori precisazioni sull’azione terapeutica dell'oleandrina, glicoside acetilato neutro che, come la cimarina, presenta la particolarità di possedere caratteristiche simili, nello stesso tempo, a quelle proprie ai glicosidi digitalici e a quelli strofantinici.
Secondo questo A., le caratteristiche farmacologiche e terapeutiche sarebbero però più vicine a quelle della Digitale che a quelle dello Strofanto. Come la Digitale essa agirebbe soprattutto nelle insufficienze ventricolari destre: è diuretico e parasimpaticomimetico, ma queste azioni diuretica e bradicardizzante, sarebbero molto più marcate di quelle proprie alla Digitale.
Al contrario, caratteri questi che lo avvicinano allo Strofanto, l’oleandrina agisce molto più prontamente della Digitale, la sua azione è breve e non si accumula. Come la Digitale essa può determinare la comparsa di extrasistoli, ma la sua tossicità sembra essere tuttavia inferiore tanto a quella della Digitale quanto a quella dello Strofanto.
I risultati terapeutici migliori si otterrebbero, secondo l’A., nei mitralici in aritmia completa e anche nel flutter auricolare.
In quest’ultimo caso debbono essere somministrate dosi elevate, comparabili alle dosi elevate di digitalina normalmente usate.
Nelle insufficienze ventricolari sinistre a cuore regolare, i risultati sarebbero al contrario, meno appariscenti.
La dose ordinaria consigliata dall’A., è di 1-2 mg al giorno. Potrebbe essere utile ricorrere alla via endovenosa e intramuscolare, per quanto altri AA., in considerazione della rapidità con cui essa viene assorbita anche per somministrazione orale, ritengono superfluo ricorrere ad altre vie di somministrazione.
Nei casi ribelli e nel flutter, la dose può essere portata a 2,2-3 mg (12-15 compr. da 1/5 di mg) al giorno. Il vantaggio dei preparati di Oleandro consiste nel poter essere impiegati altrettanto bene, sia prima che dopo trattamento con digitale o con ouabaina e nel non determinare praticamente, disturbi del ritmo.
L’A. trova un ostacolo all’impiego dei preparati di Oleandro, nella intolleranza gastrica che si manifesterebbe con una certa frequenza, tanto da limitare l'uso di questo medicamento che, secondo l’A., rappresenterebbe qualche cosa di più di un tonicardico minore.
Lozada e coll. (67) che hanno impiegato per le loro prove cliniche, oleandrina pura in soluzione idroalcoolica al 0,04%, somministrandola alla dose di mg 1,6 al giorno, sia per os che endovena, confermano che questo glicoside è dotato di un’azione digitalica che, secondo loro, può essere situata fra quella della Digitali lanata e quella dello Strofanto.
Il suo effetto bradicardizzante, può essere neutralizzato dall’atropina, è più rapido di quello della Digitale, più durevole di quello dello Strofanto e si manifesterebbe con particolare intensità soprattutto nei casi di fibrillazione.
Anche questi AA. hanno notato alterazioni elettrocardiografiche di tipo digitalico, ma l’eccitazione delle attività ectopiche è sembrata loro trascurabile, particolare questo che conferirebbe all’oleandrina un notevole interesse terapeutico.
A conclusioni analoghe a quelle riferite dagli AA. precedenti, giunse anche Martelli (78) che ha sperimentato l’oleandrina in un gruppo di 12 cardiopazienti, notando in particolare, che gli effetti dell’oleandrina sui segni generici di scompenso cardiaco (dispnea, cianosi, stasi polmonare, epatica, renale, edemi alle parti declivi) sono in tutto e per tutto simili a quelli ottenibili con la Digitale, con lo Strofanto e con la Scilla. Il progressivo ripristino dell’efficienza contrattile del miocardio, è accompagnato da un aumento dei valori pressori massimali e da una diminuzione di quelli medi e minimali.
La notevole efficacia cardiotonica, la rapidità di attacco miocardico di grado medio, la grande velocità di distacco e di eliminazione e la completa mancanza di accumulo, fanno dell’oleandrina, anche secondo questo A., un cardiotonico intermedio fra la Digitale e lo Strofanto, mentre la completa assenza di preoccupanti fenomeni di dromotropismo negativo e di batmotropismo positivo, renderebbero questo farmaco particolarmente indicato allorquando il trattamento cardiotonico deve essere condotto con scarsa o nessuna sorveglianza medica.
Alla stessa conclusione giungono Bar e Zeitler (79) che avendo sperimentato un preparato a base di oleandrina su di un gruppo di 33 cardiopazienti, sottolineano i vantaggi del suo impiego nella terapia ambulatoriale.
Rosario (80) ha sperimentato clinicamente lo stesso preparato totale depurato e titolato biologicamente (1 g del quale corrisponde all’attività di 0,4 U.I.), già studiato sperimentalmente da Osterwald (54) e clinicamente da Tursi (81) per la terapia di mantenimento dopo un trattamento di attacco con il lanatoside C e, inoltre, da De Biasio e Mazzi (82) e da Castellani e Consolini (83) in soggetti in età avanzata con manifestazioni non gravi di insufficienza cardiocircolatoria in fase cronica. Rosario ha sperimentato il suddetto prodotto, su cardiopazienti di varia età, con fenomeni pronunciati di insufficienza cardiocircolatoria a tipo congestizio (dispnea, cianosi, edemi, fegato da stasi, oliguria, tachicardia). Nella maggior parte dei casi si trattava di pazienti affetti da vizi mitralici o mitro-aortici. Le ricerche vennero condotte complessivamente su 12 pazienti ai quali il prodotto veniva somministrato a dosi oscillanti fra i 5 e i 6 g (150-180 gocce) al giorno. I risultati ottenuti permettono all’A. di concludere che il prodotto somministrato per via orale a dosi sufficienti, viene assorbito rapidamente ed è ben tollerato dalle mucose gastroenteriche, dal miocardio e dall’apparato neurovegetativo.
Le dosi terapeutiche nei cardiopatici scompensati, debbono essere secondo l'A. piuttosto elevate e superiori comunque a quelle sino ad ora consigliate. Il più delle volte sarebbero necessarie dosi di 180 gocce al giorno, pari a 2,4 U.I., suddivise in tre dosi. Dosi inferiori sarebbero raramente sufficienti per determinare un buon effetto terapeutico. Con le dosi suddette, l’effetto bradicardizzante è, di norma, notevolmente marcato e rapido e sembrerebbe essere espressione di una spiccata azione vagotonica
Parallelamente all’azione bradicardica, si rende evidente anche un miglioramento delle condizioni circolatorie che si manifesta sia clinicamente che per le modificazioni che subisce la pressione venosa e la velocità d circolo.
Le modalità con cui compare l’effetto diuretico, inducono l'A, a ritenere che esso possa essere considerato come una conseguenza delle migliorate condi
Raggiunta la riduzione della frequenza cardiaca, occorrono dosi di mantenimento che poco si discostano da quelle impiegate per la terapia di attacco. Riducendo la dose o sospendendo la somministrazione, l’A. ha notato una chiara tendenza ad un rapido rielevarsi della frequenza cardiaca.
La prontezza d'azione del farmaco e la sua rapida reversibilità, inducono anche questo A. a ritenere che l’azione dell’Oleandro si avvicini molto a quella dello Strofanto. Tuttavia, per quanto l’Oleandro, a dosi sufficienti, si dimostri un cardiotinico dotato di rapida azione, di discreta o buona attività nella terapia degli scompensi circolatori di tipo congestizio e di notevole maneggevolezza, la sua breve durata di effetto e la necessità di impiegare un dosaggio di mantenimento piuttosto elevato, lo renderebbero, secondo l’A., poco adatto per trattamenti prolungati.
Schweitzer (84) ha sperimentato un preparato risultante dall’associazione dei glicosidi dell’Oleandro con un nitrocomposto che, oltre a conferire al preparato un marcato effetto vasodilatatore delle coronarie, prolungherebbe anche l'azione caratteristica dei glicosidi oleandrinici. L’A. afferma infatti, che i risultati da lui ottenuti dimostrano che il preparato può essere usato anche per il trattamento prolungato nei casi di insufficienza cardiaca di lieve o di media gravità.
Potere di accumulo, tossicità ed assuefazione
Nel riferire i risultati delle ricerche farmacologiche e cliniche, abbiamo avuto più volte l’occasione di rilevare le caratteristiche di accumulo e di tossicità dell'Oleandro e dei suoi glicosidi cardioattivi. Completeremo ora questo capitolo riferendo i risultati ottenuti da autori che di questo argomento fecero oggetto di particolari indagini.
Flury e Neumann (48), oltre l’azione farmacologica della folinerina e la sua resistenza all'azione degli acidi, e quindi del succo gastrico, hanno indagato anche il suo potere di accumulo nel gatto, nel quale la folinerina veniva iniettata endovena ad una dose corrispondente al 36,5% di quella mortale. Essi notarono che notevoli sintomi di avvelenamento permanevano anche il giorno seguente, mentre una successiva iniezione di folinerina dimostrava il sussistere ancora dell’azione della prima dose e cioè un residuo del 35,5% della dose mortale. Dopo 3 giorni è ancora presente un residuo del 31% e del 19% dopo 5 giorni. Esisterebbe quindi un accumulo ma non come per la digitossina per la quale Bansi e Fromherz (85), dopo la somministrazione di una dose pari al 35% dell’unità gatto, hanno constatato che dopo 3 giorni moriva il 20% degli animali trattati e fino all’80% entro il 12°giorno. Flury e Neumann non hanno invece osservato nessun caso di morte tardiva dopo somministrazione di oleandrina.
Heubner e Nyary (46) che hanno sperimentato comparativamente l’azione cumulativa della digitossina, della g-strofantina e dell’oleandrina, hanno trovato che la d.m.m. della digitossina somministrata ai ratti per perfusione endovenosa, è di 12 mg/kg, sia se questa dose veniva iniettata in 10-20’ sia in 30-50’ o in 100-200’: per la g-strofantina hanno trovato invece, per gli stessi tempi, dosi mortali di 17 mg/kg, di 28 mg/kg e di 43 mg/kg e per l’oleandrina di 10, 11,6 e 16,6 mg/kg.
Si può quindi concludere da ciò che l’oleandrina si accumula, ma in misura inferiore alla digitossina.
L'accumulo e l’assuefazione per intossicazione lenta da Oleandro, furono studiati successivamente con una serie di ricerche da Giroux e coll, i quali impiegarono estratti stabilizzati di foglie di Oleandro ottenuti con alcool di 30° e di 70°.
Per quanto riguarda l’intossicazione rapida, ottenuta cioè col metodo dell’iniezione unica, Giroux, Mathieu e Desbordes (85), hanno sperimentato i suddetti estratti sul coniglio, sulla cavia, sul ratto e sulla rana, constatando che l’animale che meglio si presta per la determinazione della tossicità con questo metodo, sia per i risultati più costanti che si ottengono, sia perchè le differenti fasi dell’intossicazione sono più nette, è la cavia.
Nell’intossicazione acuta da Oleandro si possono distinguere quattro fasi: una fase preliminare, una fase di torpore, una fase convulsiva e una fase di atonia premortale.
Gli estratti di Oleandro preparati con alcool di 30° si sono dimostrati meno tossici di quelli preparati con alcool di 70°, su tutti gli animali su cui sono stati sperimentati.
I valori trovati dagli AA. per la d.m.m. nei diversi animali sono i seguenti:
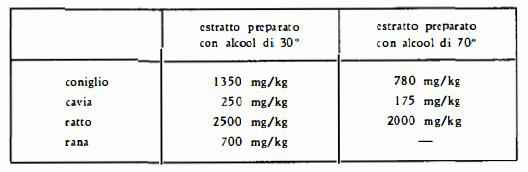
Controlli istologici eseguiti da Giroux, Guibert e Desbordes (87) nei vari organi di animali intossicati, sia col metodo rapido che con quello lento, hanno dimostrato che soltanto nel reni e nei surreni è possibile osservare una tendenza alla congestione ma nessun’altra modificazione o lesione del parenchima.
Il potere di accumulo e l’assuefazione sono stati studiati da Giroux, Monnier e Desbordes (88) impiegando l’estratto ottenuto con alcool di 30° a dosi molto elevate.
Le prove sono state eseguite su cavie e su conigli ai quali l’estratto veniva iniettato alle dosi di 2000 mg/kg e di 500 mg/kg al giorno, frazionate in 2 iniezioni.
Gli AA. hanno potuto constatare che iniettando la dose di 2000 mg/kg al giorno, gli animali possono tollerare una dose complessiva superiore di 3 volte la dose mortale unitaria, mentre somministrando il preparato alla dose di 500 mg/kg al giorno, gli animali potevano tollerare una dose complessiva superiore di 10 volte a quella mortale unitaria.
Contrariamente a quanto osservarono sul coniglio, gli AA. hanno notato che nella cavia i sintomi di intossicazione sono già molto evidenti anche dopo la somministrazione di dosi relativamente piccole.
Iniettando la dose di 100 mg/kg al giorno, in due volte, dello stesso preparato di oleandrina, la cavia dimostra di sopportare una dose complessiva pari a 8 volte la dose mortale unitaria.
Resterebbe quindi ulteriormente provato che tanto nella cavia quanto nel coniglio, l'Oleandro, specie se somministrato a dosi elevate, può dar luogo ad un’azione cumulativa ma di grado non elevato.
Nel corso di queste prove gli AA. hanno inoltre notato che, tanto nella cavia quanto nel coniglio, si verifica una certa assuefazione, ma limitatamente ad alcune manifestazioni nervose dell’intossicazione da Oleandro. Queste manifestazioni infatti, che compaiono dopo le prime iniezioni, cessano dopo le iniezioni successive, per ricomparire però durante la fase premortale allorché l’accumulo e quindi la concentrazione in circolo, raggiunge un certo livello.
Ricerche condotte con lo scopo di studiare l’attività dei vari organi della pianta di Oleandro, stabilizzati o non, sono state eseguite da Giroux, Hoanau e Desbordes (89), i quali hanno esaminato 8 estratti fluidi ottenuti con alcool di 30° e di 70° dalla corteccia dei rami e dalle foglie, dopo stabilizzazione o dopo semplice essiccazione all’aria.
L’attività dei diversi estratti è stata studiata comparativamente, col metodo della perfusione del cuore isolato di coniglio e col metodo della perfusione endovenosa e registrazione della pressione carotidea nel cane.
I risultati ottenuti hanno dimostrato che gli estratti preparati con la droga stabilizzata sono più attivi di quelli preparati con la droga semplicemente essiccata all’aria e, inoltre, che gli estratti della corteccia dei rami e quelli delle foglie, dopo stabilizzazione, sono ugualmente attivi.
Berezhinskaya (90) ha studiato comparativamente l’attività terapeutica e la tossicità di diversi glicosidi digitalici. Per quanto riguarda la loro attività, l’A. avrebbe stabilito la seguente successione, in ordine discendente: erisimina, strofantina, cimarina, folinerina. L’attività fisiologica generale e la tossicità (valutate sulla rana e sul gatto) non sarebbe parallela poiché la folinerina è risultata la più tossica e la cimarina la meno tossica.
In tutti è stato constatato un effetto digitalico sull'elettrocardiogramma e un effetto diuretico: la cimarina si sarebbe dimostrata la più attiva sotto quest’ultimo aspetto.
Le dosi terapeuntiche hanno un marcato effetto sulla pressione venosa, mentre le dosi tossiche determinano miocarditi con distrofia adiposa e proteica delle fibre muscolari cardiache.
Da determinazioni della d.m.m. su diversi animali, eseguite comparativamente con alcuni glicosidi cardioattivi dalla Capra e pubblicate in collaborazione con Ghielmetti e Castoldi (32), risulta che la d.m.m. dell’oleandrina è intermedia fra quella della g-strofantina e quella della digitossina e, inoltre, che la forte differenza di attività riscontrata per l’oleandrina nel coniglio, in confronto con gli altri glicosidi cardiotonici, non si verifica invece nella cavia e nel gatto.
Il coniglio appare molto resistente all’azione dell’oleandrina e risulta pertanto meno adatto degli altri animali per il dosaggio biologico di questo glicoside.
La cavia ha invece dimostrato di essere più sensibile verso l’oleandrina, sensibilità che può essere considerata simile a quella che presenta verso la digitossina e la g-strofantina.
L'A. ritiene quindi che la cavia, per le sue caratteristiche di sensibilità, di maneggevolezza e per la facile reperibilità, sia l'animale che meglio si presta per la titolazione dell’oleandrina e dei preparati di Oleandro e ciò in accordo anche con quanto era stato già dimostrato precedentemente da Giroux, Mathieu e Desbordes (86).
Per riassumere si può dunque dire che le caratteristiche più salienti dell’Oleandro e dell’oleandrina consistono principalmente in un’azione più pronta di quella della Digitale, in un assorbimento molto rapido sia per os che per via rettale, tanto da rendere superflua la somministrazione per via parenterale; in un elevato potere bradicardizzante: nel possedere una zona maneggevole molto ampia e un minimo potere di accumulo.
Sullo Strofanto, l’Oleandro avrebbe inoltre il vantaggio di permettere il manifestarsi del massimo dell’azione anche per somministrazione orale.
Per tali sue caratteristiche la maggior parte degli AA. sono concordi nel situare l’Oleandro fra la Digitale e lo Strofanto, anche se alcuni AA. ritengono che la sua azione si avvicini più a quella della Digitale o a quella della Digitalis lanata.
Terapeuticamente sembra che i risultati migliori si ottengano nel trattamento dei disturbi del ritmo, dell’insufficienza cardiaca dovuta a vizi valvolari o ad affezioni miocardiche. Secondo Mouquin e coll. (74), l’azione più notevole dell’oleandrina sarebbe quella bradicardizzante e secondo il Lozada (77) essa si manifesterebbe con particolare intensità nei casi di fibrillazione. Buoni risultati si ottengono nelle miocarditi con aritmia totale e, in particolare, nell'insufficienza cardiaca dei mitralici, nell’insufficienza ventricolare destra e nel flutter auricolare.
Un inconveniente cui può dar luogo l'impiego dell'Oleandro e dei suoi derivati, è dovuto all'intolleranza gastroenterica che non raramente si manifesta, specialmente se la somministrazione avviene a stomaco vuoto o in soggetti particolarmente sensibili. Questo inconveniente può essere, almeno in parte, evitato specialmente per quanto riguarda l’irritazione gastrica, ricorrendo all’uso di preparati in compresse con rivestimento gastroresistente, oppure a soluzioni con l'aggiunta di un colloide protettore (gelatina idrolizzata per es. od altro) che ne attenui l'azione irritativa di contatto.
Estratti e preparati vari
Estratto fluido (Titolo biologico 1 % oleandrina cristalli) (g 1 = LII gtt)
Dosi: II gtt pro dose, due-tre volte pro die.
Preparazioni usuali e formule galeniche
Tintura
Estratto fluido oleandro……………………………………………. g 10
Alcool di 70° ……………………………………………………….. g 90
(XX gtt due-tre volte pro die).
Gocce antidispnoiche
Estratto fluido oleandro ………………………………………………… g 10
Estratto fluido scilla………………………………………………………. g 2
Estratto fluido convallaria……………………………………………… g 2
Estratto fluido grindelia ………………………………………………… g 6
Alcool di 60°
Glicerina………………………………………………………………….. ana g 40
(X-XX gtt due-tre volte pro die).
BIBLIOGRAFIA
(1) LUKOWSKl P. J., J. Pharnwcic, 46, 397, 1861 – (2) SCHMIEDEBERG O., Arch. cxp. Patii. u. Pharmakol., 16, 199, 1882; Ber., 16, 253, 1883 – (3) WINDAUS A. e WESTPHAL K., Chem. Zbl., I, 1814, 1926 – (4) FLURY F. e NEUMANN W., Chem. Zbl., li, 3542, 1935 – (5) NEUMANN W., Ber., 70, 1547, 1937 – (6) TSCHESCHE R., Ber., 70, 1554, 1937 – (7) TURKOVIC I., J. Pharm. Belg., 14, 263, 376 e 447, 1959; Pharm. Acta Heh'., 37, 301, 1962 • (8) JEGER H., SCHINDLER O. e REICHSTEIN T., Heir. Chim. Acta, 42, 977, 1959 – (9) TSCHESCHE R. e GRIMMER G., Ber., 87, 418, 1954 – (10) TSCHESCHE R. e BOHLE K., Ber.. 71, 654, 1938 – (li) TSCHESCHE R., BOHLE K. e NEUMANN W., Ber., 71, 1927, 1938 – (12) TSCHESCHE R. e SNATZKE G., Ber., 88, SII, 1955 – (13) CARDWELL H.
M. E. e SMITH S., J. Chem. Soc., 2012, 1954 – (13a) JANIAK P. 5.. WEISS E. . v. EUW J. e REICHSTEIN T., Helv, Chim. Aita, 46. 374. 1963 • (14) RHEINER A., HUNGER A. e REICHSTEIN T., Heh'. Chim. Acta, 35, 687, 1952 – (15) RANGASWAMI S. e REICHSTEIN T., Heli'. Chim. Acta, 24, 159, 939, 1949 – (16) RITTEL W., HUNGER A. e REICHSTEIN T., Helv. Chim. Acta, 36, 434, 1953 – (17) RITTEL W. e REICHSTEIN T. Heh'. Chim. Acta, 37, 1361, 1954 – (18) TANRET G .. Comot. retid., 194, 914, 1932; Buìl. soc. chim. biol., 14, 708, 1932 – (19) GOERLICH B., Pianta Med., 9, 442, 1961 – (20) LLOPIS A., Galenica Acta, 8, 101, 1955; 9, 81, 1956 – (21) SCHlNDLER O. e REICHSTEIN T., Helv. Chim. Acta, 35, 442 e 673, 1952 – (22) HUNGER A. e REICHSTEIN T., Helv. Chim. Acta, 33, 1993, 1950 – (23) WINDAUS A. e SCHWARTE G., Ber., 58, 1515 e 1519, 1925 – (24) RANGASWAMI
5. e REICHSTEIN T., Pharm. Acic( Helv., 24, 159, 1949 – (25) NEUMANN W., Chem. Zhl., II, 3342, 1933 – (26) GHIELMErn G., CASTOLDI C. F. e CAPRA C., Il Farmaco, ed. prat., 13, 303, 1958 – (27) CAPRA C., dati inediti di analisi eseguite nei Laboratori Inverni & Della Beffa – Milano, 1961 – (28) WAGNER H. e LUCK R., Naturwijj., 42, 607, 1955; Chem. Abs., 51, 1813li, 1957 – (29) HOERHAM- MER L,, WAGNER H. e LUCK R., Arch. Pharm., 289, 613, 1956; Chem. Ahs., 51, 8376 f, 1957 – (30) HOERHAMMER L. e WAGNER H., Arch. Pharm., 290, 224, 1957; Chem. Abs., 51, 14203 i, 1957 – (31) PEYROT P., GIROUX J. e DELMAS J., Relaz. alla Soc. Pharmacie de Montpellier (31-1-1944) – (32) LE MEN G. e POURRAT H., Ann. pharm. irang., 10, 349, 1952 – (33) ATAKISHIEVA Z. N., Doklady Akad. Nauk. Azebaidzhan S.S.R., 9, 353, 1953; Chem. Abs., 50, 5240 a, 1956 – (34) PLOUVIER V., Compt. rend., 251, 131, 1960 – (35) SCHINDLER H., Inhaltstofle und Priifungsmethoden homaopatisch verwcndeter Heilpflanzen; 1955, p. 145 – (36) WEHMER C., Die Pflanzenstoffe, II ed., p. 992 – (37) LUKOWSKI, Repert. de Chimie, 3, 77, 1861 • (38) PELTKAN, Comp. rend., 62, 237, 1866 – (39) SCHMIEDEBERG O., Arch. exp. Path. u. Pharmakol., 16, 149, 1883 – (40) POULOUX, Bull. gen. Thérap., 114, 393, 1888 – (41) POULOUX, Thése de Paris 1889 – (42) OEFELE, Pharm. Zentralh., 34, 342. 1893 – (43) MAGNANINI, Boll. Accad. Med., Roma, 119, 679, 1893 – (44) GALLI G., Arch. Cardiol. y Rematol., 349, 1924 – (45) WINDAUS e WESTPHAL, Nachr. Gescll. Wissensch. Gottingen, 78, 1925 – (46) HEUB- NER e NYARY, Arch. exp. Path. u. Pharmakol., 177, 60, 1934 – (47) BAUER e FROMHERZ, Klin. Woch., 973, 1933 – (48) FLURY e NEUMANN, ibid., 14, 562, 1935 – (49) SCHWAB, ìbìd., 14, 569, 1935 – (50) HOSSLIN, ibid., 15, n. 4, 1936 • (51) SCHULER e OTI, Munch. med. Woch., 14, 49, 1937 – (52) HEULER, Med. Wclt., 12, 1590, 1938 – (53) CASTELLE-ROTH, Therap. Gegenw., 80, 355, 1939 – (54) OSTERWALD K. H., Klin. Woch., 20, 146, 1941 – (55) SCHIDEL L. E. e BRAUN K., Brit. Heart J..
6, 149, 1944 – (56) ASTRUC A., GIROUX J. e HOARAU M., Soc. Pharm. Montpellier – seduta 31 gennaio 1944 – (57) GIROUX J., HOARAU M. e DESBORDES J., ibid., 27 novembre 1944 – (58) AIAZZI MANCINI M., Ricerche farmacologiche sull'Oleandro (N. oleander), Elli & Pagani, Milano 1946 – (59) CORTESI R., Boll. chim. Jarm., 90, 48, 1951; Schweiz. Ap. Zig., 89, 721, 1951 – (60) BORIANI A., Il Farmaco, 8, 428, 1948 – (6l) WOLFRED M. M., J.A.Ph.A., 38, 581, 1949 – (62) LOUBATIÉRES, Arch. intern. pharmacod. et de thér., 85, 49, 1951 – (63) LOUBATIERES, Actualité Pharmaceutiques, Hazard M., Masson, Paris 1951, p. 69 – (64) LOUBATIÉRES, BOUYARD, MACABIES e MOURALIS, J. Physiol., 41, 207, 1949 – (65) SEVILLA M. e SOLER Y MONSALVE J. M., Ga:;. med. espan., 27, 570, 1953; Excerpta Med., 11, 7, 449, 1954 • (66) AIAZZI-MANCINI M., Arch. interzi. pharmacod. et de thér., 139, 42, 1962 – (67) PUGLISI A., Semana Med., n. 13, 791, 1940 – (68) BINDER L., Z. Kreislaufiorsch., 31, 23, 1939 – (69) HILDEBRANDT, Klio. Woch., n. 6, 146, 1941 – (70) BANSI, Med. Klin., n. 42, 1390, 1937 – (71) BECKER-FREISENG, Klin. Woch., n. 23, 815, 1938 – (72) LAUER, Z. Kreislaufiorsch., n. 3, 81, 1940 – (73) PENDL F. e RÒSSNER A., Dtsch. med. Woch., n. 6, 183, 1951 – (74) MOUQUIN, MACREZ, PARIS e RENARD, Arch. mal. coeur et vaiss., dicembre 1950 – (75) RAVERA L., Min. Med., 42, 73, 680, 1951 – (76) MOUQUIN M., Thérapie, 8, 140, 1953 – (77) LOZADA B. B., TEMPONE N. D. e PLESCH S. A., Revista Argentina de Cardiol., 24. 99. 1954 – (78) MARTELLI A., Min. Med., 45, 690. 1954 – (79) BAR C. G. e ZEITLER G., Dtsch. med. Woch., 80, 1038, 1935 – (80) ROSARIO G. M., ScritU in onore del 25° anno di Cattedra dei Prof.ri Condorelli L., Greppi E. e Villa P., La Settimana Medica, edit. Firenze 1954, p. 64 – (81) TURSI F., cit. da ROSARIO (80) – (82) DE BIASIO B. e MAZZI G., cit. da ROSARIO (80) – (83} CASTELLANI T. e CONSOLINI M., cit. da ROSARIO (80) – (84} SCHWEITZER H., Med. Klin., 25, 387, 1960 – (85) BANSI e FROMHERZ, Klin. Woch., 973, 1933 – (86) GIROUX J., MATHIEU S. e DESBORDES, Comunicaz. alla Soc. Pharm. Montpellier, 30 aprile 1945 – (87) GIROUX J., GUIBERT H. L. e DESBORDES, ibid. – (88) GIROUX J., MONNIER P. e DESBORDES, ibid. – (89) GIROUX J., HOANAU M. e M.LLE DESBORDES, ibid. – (90) BEREZHIN- SKAYA V. V., Farmakol. i Toksikol., 19, 38, 1956: Chem. Abs., 51, 6882 h. 1957 – (91) REDONNET T. A., Farmacognosia, 13, 375, 1953.


