Recentemente si è posta all’attenzione una nuova terapia per il trattamento dello scompenso cardiaco con ridotta frazione d’eiezione a base di Entresto (sacubitril-valsartan).
Si tratta di un’associazione orale precostituita dell’inibitore della neprilesina Sacubitril e dall’antagonista dei recettori dell’angiotensina Valsartan (nome commerciale Entresto).
La nuova associazione sta ricevendo notevole risonanza mediatica sui così detti siti specializzati sull’informazioni sui farmaci inoltre sembra riscuotere notevole apprezzamento da parte dei clinici e della comunità scientifica tanto da essere inserita tra le opzioni di trattamento di prima linea dalle più recenti linee guide americane, quindi un approfondimento risulta più che doveroso.
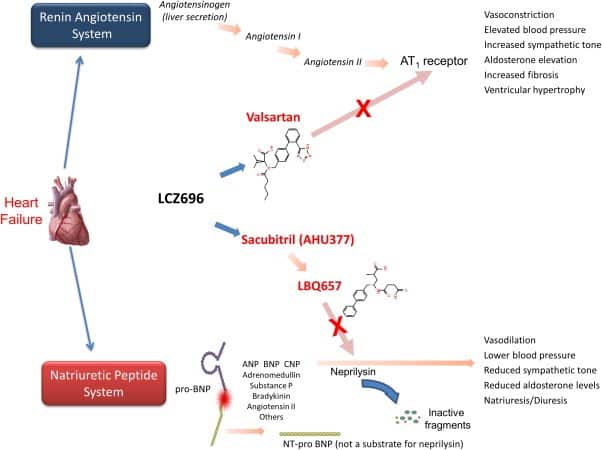
La neprilesina è un’endopeptidasi neutra che degrada alcuni peptidi vasoattivi, inclusi i peptidi natriuretici, la bradichinina e l’adrenomedullina. L’inibizione della neprilesina ad opera del metabolita attivo di Sacubitril (LBQ657) aumenta i livelli di questi peptidi, riducendo di fatto la vasocostrizione, la ritenzione di sodio e il rimodellamento maladattivo.
Il Valsartan blocca i recettori dell’angiotensina II di tipo 1 (AT1), inibendo l’angiotensina II e il rilascio dell’aldosterone.
I dati di efficacia sull’associazione Sacubitril (S) + Valsartan (V) derivano unicamente dallo studio PARADIGM-HF (1), mentre sono trascurabili altri due studi (PARAMOUNT e TITRATION) vista la breve durata -12 settimane- e gli outcome in analisi cioè sicurezza (a 12 settimane per un trattamento cronico?) o variazioni del NT-proBNP (outcome surrogato).
Lo studio PARADIGM-HF è un trial di fase III randomizzato controllato in doppio cieco condotto su 8442 pazienti con scompenso cardiaco di classe II-IV e ridotta frazione di eiezione (≤40% prima dell’emendamento ad un anno dall’inizio del trial che ha visto ridurre questo valore, portandolo ad un valore di ≤35%).
I pazienti sono stati randomizzati a ricevere S+V 200 mg due volte al giorno o Enalapril (E) 10 mg bid, entrambi in aggiunta alla terapia di fondo.
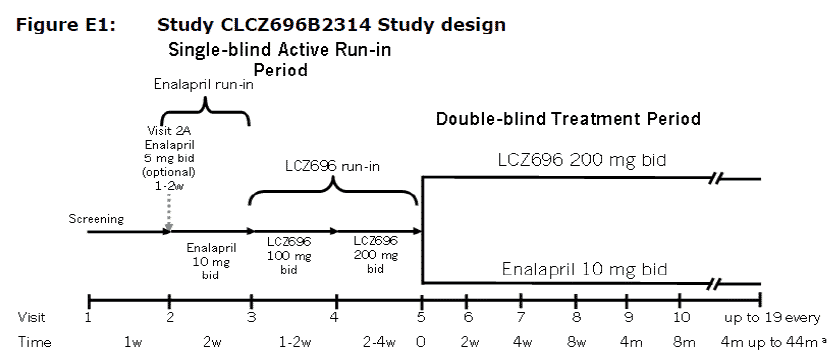
Lo studio nel suo complesso ha previsto 4 fasi (come da figura):
- screening per i criteri di inclusione ed esclusione. I pazienti eleggibili erano in trattamento con una dose stabile di un ACE inibitore o un Sartano (ARB) equivalente a enalapril 10 mg al giorno per 4 settimane o più prima della visita di screening.
- Enalapril run-in (2 settimane): i pazienti eleggibili sono passati dal trattamento con ACE inibitore o ARB ad un trattamento in singolo cieco con enalapril (10 mg due volte al giorno).
- Sacubitril valsartan run-in (da 4 a 6 settimane): i pazienti risultavano eleggibili se non avessero sperimentato effetti collaterali inaccettabili nella precedente fase. I pazienti eleggibili sono stati passati a trattamento in singolo cieco con sacubitril + valsartan ad una dose di 100 mg due volte al giorno, aumentata in seguito a 200 mg due volte al giorno durante la fase di run-in. Le 2 fasi run-in erano sequenziali, con solo un breve periodo di washout (circa 36 ore)
- Trial principale: i pazienti senza effetti collaterali inaccettabili dopo l’assunzione di dosi target del 2 farmaci in studio sono stati randomizzati (1: 1) per il trattamento in doppio cieco con valsartan sacubitril (200 mg due volte al giorno) o enalapril (10 mg due volte al giorno).
L’end point primario era un composito di mortalità cardiovascolare e ospedalizzazione per insufficienza cardiaca.
Dopo 27 mesi di follow-up lo studio è stato interrotto prematuramente in quanto la terza analisi ad interim predefinita ha mostrato una mortalità cardiovascolare inferiore nei pazienti nel braccio di trattamento con Entresto (sacubitril-valsartan).
Di seguito si riassumono gli outcome ed i risultati ottenuti dal confronto Entresto (sacubitril-valsartan) vs Enalapril:
-
Mortalità cardiovascolare o Ospedalizzazione per scompenso cardiaco
21.8% vs. 26.5% (HR 0.80; 95% CI 0.73-0.87; P<0.001; NNT 21) -
Mortalità cardiovascolare
13.3% vs. 16.5% (HR 0.80; 95% CI 0.71-0.89; P<0.001; NNT 31) -
Ospedalizzazione per scompenso cardiaco
12.8% vs. 15.6% (HR 0.79; 95% CI 0.71-0.89 P<0.001; NNT 36) -
Mortalità per tutte le cause
17.0% vs. 19.8% (HR 0.84; 95% CI 0.76-0.93; P<0.001; NNT 36)
L’analisi per sottogruppi ha evidenziato un miglioramento nell’outcome primario per i pazienti affetti da scompenso cardiaco classe NYHA I e II con l’associazione ma tale tendenza non si è riscontrata nei pazienti con scompenso classe NYHA III-IV, cioè nei pazienti più gravi.
Nessun miglioramento dell’outcome primario è stato ottenuto nei sottogruppi: pazienti con età maggiore od uguale a 75 anni; con frazione d’eiezione maggiore del 35%; pazienti dell’Europa dell’Ovest.
Di seguito si riassumono i principali risultati sulla sicurezza e quelli ottenuti dal confronto Entresto (sacubitril-valsartan) vs Enalapril:
- Ipotensione sintomatica: 14.0% vs. 9.2% (P<0.001; NNH 21)
- Pazienti sintomatici con pressione arteriosa sistolica <90 mmHg: 2.7% vs. 1.4% (P<0.001; NNH 77)
-
Aumento della Creatinina
- ≥2.5 mg/dL: 3.3% vs. 4.5% (P=0.007)
- ≥3.0 mg/dL: 1.5% vs. 2.0% (P=0.10)
-
Aumento del Potassio
- ≥5.5 mmol/L: 16.1% vs. 17.4% (P=0.15)
- ≥6.0 mmol/L: 4.3% vs. 5.6% (P=0.07)
- Tosse: 11.3% vs. 14.3% (P<0.001)
-
Angioedema
- Nessuna terapia oppure antistaminici: 0.2% vs. 0.1% (P=0.19)
- Uso di catecolamine o corticosteroidi: 0.1% vs. 0.1% (P=0.52)
- Ospedalizzazione senza compromissione delle vie aeree: 0.1% vs. <0.1% (P=0.31)
- Compromissione delle vie aeree: Nessun caso
Quindi in definitiva il trial ha dimostrato che Entresto (sacubitril-valsartan) rispetto al solo Enalapril ha ridotto mortalità cardiovascolare, mortalità totale e ospedalizzazione per insufficienza cardiaca.
Tuttavia si evidenziano numerose criticità nella conduzione del trial:
- si tratta di uno studio sponsorizzato dalla ditta produttrice Novartis che ha collaborato sia nella conduzione dello studio che nell’analisi dei dati ed è ampiamente documentato in letteratura che gli studi condotti dalle Aziende sono molto più propensi a fornire risultati favorevoli al trattamento in studio
- come comparator è stato scelto l’Enalapril arrivando a titolarlo ad un dosaggio massimo di 20 mg al giorno, dosaggio ben al di sotto di quanto consigliato dalle attuali Linee guida europee (European Heart Journal [2012] 33, 1787-1847) che prevedono un dosaggio di 40 mg die (20 mg due volte al giorno). Si ricorda che è stato utilizzato il dosaggio massimo consentito (all’interno dell’associazione S+V) di Valsartan cioè 160 mg BID
- la fase di run-in ha potuto selezionare ulteriormente i pazienti in studio (5% pazienti dalla fase di selezione a quella di randomizzazione hanno migliorato la classe NYHA sino a giungere alla classe NYHA I)
- sono stati randomizzati 961 pazienti con frazione di eiezione maggiore del 35%, cioè prima dell’emendamento e ciò ha potuto inficiare il dato finale
- oltre il 70% dei pazienti era affetto da scompenso cardiaco di classe NYHA II, età media di 63,8 anni, quindi si tratta in maggioranza di pazienti giovani (32% dei partecipanti aveva 55 anni od era più giovane)
- nella randomizzazione risultano leggermente squilibrati i due gruppi di trattamento per quel che concerne la gravità della classe NYHA. Classe NYHA II braccio trattamento Entresto (sacubitril-valsartan) 71,6%-braccio trattamento E 69,3%; classe NYHA III braccio trattamento Entresto (sacubitril-valsartan) 23,1%- braccio trattamento E 24,9%. Quindi sembrerebbe che ci siano nel gruppo di trattamento con E un piccolo eccesso di pazienti più gravi ed un piccolo difetto di pazienti meno mal messi
- solo poco più del 50% dei pazienti assegnati ad ambo i trattamenti al baseline erano in trattamento con un antagonista dell’aldosterone mentre è notorio che la terapia di riferimento per i pazienti affetti da scompenso cardiaco e con ridotta frazione d’eiezione è basata sull’utilizzo di ACE-inibitore (se non tollerato Sartano), un beta bloccante e un antagonista dell’aldosterone
- solo poco meno del 15% dei pazienti in ambo i gruppi di trattamento aveva un impianto di defibrillatore
Occorre sottolineare che si tratta di una terapia di add-on alla terapia standard (non usato ovviamente in associazione il Sacubitril con un ACE-inibitore per evitare eventi di angioedema) e quindi va a cadere la tanto strombazzata superiorità verso Enalapril.
Infatti si utilizza ed è stato studiato il Sacubitril, inibitore della Neprilesina, insieme al Valsartan, farmaco che modula il sistema renina-angiontensina verso il solo Enalapril anch’esso farmaco che agisce modulando il sistema renina-angiotensina.
In sostanza i dubbi sono molteplici a fronte di risultati potenzialmente ottimi che vanno confermati in ulteriori studi, che forniscano dati molto più robusti degli attuali, prima che Entresto (sacubitril-valsartan) diventi una prima linea nel trattamento dello scompenso cardiaco sintomatico con ridotta frazione d’eiezione…ricordiamo infine il vecchio adagio “Una hirundo non facit ver”…
BIBLIOGRAFIA
(1) McMurray JJ, Packer M, Desai AS et al Angiotensin-neprilysin inhibition versus enalapril in heart failure N Engl J Med. 2014 Sep 11;371(11):993-1004
(2) The Medical Letter Anno XLIV n.20 15 ottobre 2015
(3) Yancy CW, Jessup M, Bozkurt B et al. 2016 ACC/AHA/HFSA Focused Update on New Pharmacological Therapy for Heart Failure: An Update of the 2013 ACCF/AHA Guideline for the Management of Heart Failure: A Report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines and the Heart Failure Society of America Circulation. 2016;134