Saliciliati e Aspirina
Salicilati: indice
Generalità
Chimica
Proprietà farmacologiche
Farmacocinetica e metabolismo
Usi terapeutici
Tossicità ed effetti collaterali
Trattamento del sovradosaggio
Generalità
Nonostante l’introduzione di molti nuovi farmaci, l’aspirina è ancora il farmaco analgesico, antipiretico e antinfiammatorio maggiormente utilizzato ed è il composto di riferimento per il confronto e la valutazione di altri farmaci con le stesse proprietà.
Un’enorme quantità di questo farmaco viene usata negli Stati Uniti: alcune stime indicano tra le 10.000 e le 20.000 tonnellate l’anno.
L’aspirina è il più comune analgesico per uso domestico; tuttavia, poiché il farmaco è così ampiamente disponibile, la possibilità di abuso e grave tossicità è probabilmente sottostimata ed esso rimane una causa di avvelenamento fatale nei bambini.
La farmacologia clinica dei salicilati è stata discussa da Amann e Peskar nel 2002.
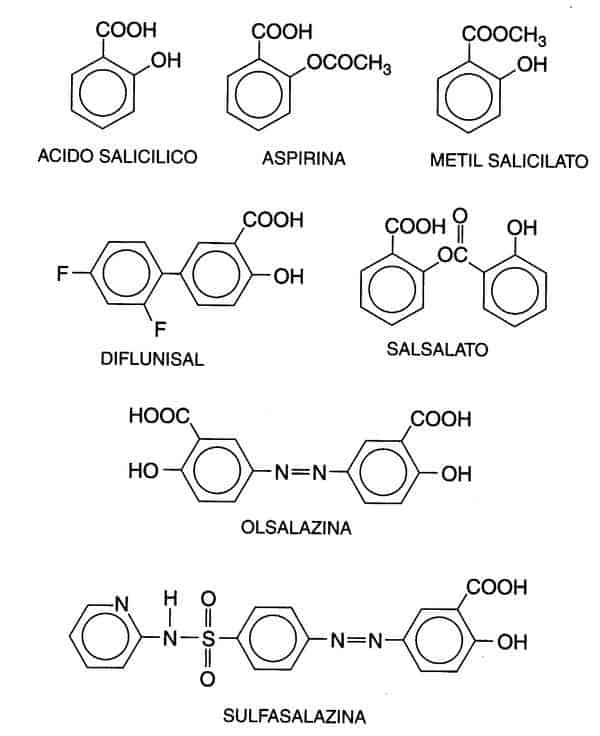
Chimica dei salicilati
L’acido salicilico (acido ortoidrossibenzoico) è così irritante che può essere usato solo esternamente; per questo motivo sono stati sintetizzati vari derivati di questo acido per uso sistemico.
Questi comprendono due ampie classi, gli esteri dell’acido salicilico, ottenuti da sostituzioni all’interno del gruppo carbossilico, e gli esteri salicilati degli acidi organici, nei quali il gruppo carbossilico viene mantenuto mentre la sostituzione avviene a carico del gruppo ossidrilico.
Per esempio, l’aspirina è un estere dell’acido acetico.
Inoltre, vi sono sali dell’acido salicilico.
Relazioni struttura-attività
I salicilati generalmente agiscono in virtù del loro contenuto in acido salicilico, anche se alcuni effetti unici dell’aspirina sono legati alla sua capacità di acetilare le proteine, come descritto più avanti.
La sostituzione sui gruppi carbossilico e ossidrilico modifica la potenza o la tossicità dei salicilati.
La posizione in orto del gruppo ossidrilico è una caratteristica importante per l’azione dei salicilati.
Gli effetti derivati dalla semplice sostituzione sull’anello benzenico sono stati ampiamente studiati e sono in corso di sintesi nuovi salicilati.
Un derivato difluorofenilico, il diflunisal, è disponibile per l’uso clinico.
Proprietà farmacologiche dei salicilati
Analgesia
I tipi di dolore solitamente risolti dai salicilati sono quelli di bassa intensità che si sviluppano dalle strutture tegumentali piuttosto che dai visceri, specialmente l’emicrania, la mialgia e l’artralgia.
I salicilati sono utilizzati per il sollievo dal dolore più di qualsiasi altra classe di farmaci.
I salicilati alleviano il dolore in virtù dell’azione periferica; possono essere coinvolti anche effetti diretti sul SNC.
Effetto antipiretico.
Solitamente i salicilati abbassano rapidamente ed efficacemente la temperatura corporea elevata.
Comunque, dosi moderate che producono questo effetto aumentano anche il consumo di ossigeno e la velocita metabolica.
Questi composti hanno un effetto piretico a dosi tossiche, e la sudorazione aggrava la disidratazione che viene indotta dall’intossicazione da salicilati.
Effetti sulla respirazione.
I salicilati aumentano il consumo di ossigeno e la produzione di CO2 (specialmente nel muscolo scheletrico) a dosi piene; questo effetto è il risultato di un disaccoppiamento della fosforilazione ossidativa.
L’incrementata produzione di CO2 stimola la respirazione (principalmente attraverso un incremento della profondità del respiro, con aumento lieve della frequenza respiratoria).
L’incremento della ventilazione alveolare bilancia l’aumentata produzione di CO2 e la pressione parziale di CO2 (PCO2) non cambia o può ridursi lievemente.
Equilibrio acido-base ed elettrolitico ed effetti renali.
Dosi terapeutiche di salicilato inducono modificazioni dell’equilibrio acido-base e del profilo elettrolitico.
La compensazione dell’evento iniziale, l’alcalosi respiratoria (vedi sopra), è raggiunta mediante un’aumentata escrezione renale di bicarbonato, che è accompagnata da un incremento dell’escrezione di Na+ e K+.
Il bicarbonato del sangue viene quindi ridotto e il pH ematico ritorna ai valori normali.
Questo è lo stadio dell’acidosi renale compensata. Questo stadio si osserva piu spesso negli adulti che sono sottoposti a una terapia intensiva con salicilati e raramente procede ulteriormente, a meno che si giunga all’intossicazione.
I salicilati possono causare ritenzione di sale e acqua, cosi come riduzione acuta della funzione renale nei pazienti con scompenso cardiaco congestizio, malattia renale o ipovolemia.
Sebbene l’uso prolungato dei salicilati da soli raramente si associ a nefrotossicità, l’ingestione prolungata ed eccessiva di miscele di analgesici contenenti salicilati in associazione con altri composti può produrre necrosi papillare e nefrite interstiziale.
Effetti cardiovascolari.
Basse dosi di aspirina (<100 mg/die) sono ampiamente utilizzate per i loro effetti cardioprotettivi.
Ad alte dosi terapeutiche (>3 g/die), come quelle somministrate per la febbre reumatica acuta, la ritenzione di sale e acqua può portare a un incremento (fino al 20%) della volemia e a una diminuizione dell’ematocrito (effetto di diluizione).
Vi è una tendenza dei vasi periferici a dilatarsi per un effetto diretto sulla muscolatura liscia. La gittata e il lavoro cardiaci sono aumentati.
Gli individui con miocardite o compromissione della funzione cardiaca possono non avere una sufficiente riserva cardiaca per rispondere all’aumentata richiesta e possono svilupparsi scompenso cardiaco congestizio ed edema polmonare.
Alte dosi di salicilati possono indurre edema polmonare non cardiogeno, particolarmente nei pazienti più anziani che assumono regolarmente salicilati per periodi prolungati.
Effetti gastrointestinali.
L’ingestione di salicilati può provocare fastidio epigastrico, nausea e vomito.
I salicilati possono anche causare ulcere gastriche, esacerbazione dei sintomi dell’ulcera peptica (pirosi, dispepsia), emorragia gastrointestinale e gastriti erosive.
Questi effetti si verificano principalmente con i salicilati acetilati (per es., aspirina).
Poiché i salicilati non acetilati mancano della capacità di acetilare la ciclossigenasi e, di conseguenza , di inibire irreversibilmente la sua attività, sono inibitori più deboli dell’aspirina.
Il sanguinamento gastrico indotto dall’aspirina è talvolta indolore e, se non riconosciuto, può portare ad anemia da carenza di ferro.
La somministrazione giornaliera di dosi antinfiammatorie di aspirina (4 o 5 g) conduce mediamente a una perdita di sangue nelle feci tra i 3 e gli 8 ml al giorno, rispetto agli 0.6 ml al giorno dei soggetti non trattati.
L’esame gastroscopico dei soggetti trattati con aspirina spesso evidenzia distinte lesioni ulcerative ed emorragiche della mucosa gastrica; in molti casi si sono osservate lesioni emorragiche multiple con aree fortemente demarcate di necrosi focale.
L’incidenza di sanguinamento può essere maggiore con i salicilati che si dissolvono lentamente e si depositano come particelle nelle pieghe della mucosa gastrica.
Effetti epatici.
I salicilati possono causare danno epatico, di solito nei pazienti trattati con alte dosi che portano a concentrazioni plasmatiche superiori a 150 mcg/ml.
Il danno non è un effetto acuto, piuttosto, l’insorgenza caratteristicamente avviene dopo molti mesi di trattamento.
La maggior parte dei casi si verifica nei pazienti con alterazioni del tessuto connettivo.
Di solito non vi sono sintomi, ma semplicemente un incremento dei livelli sierici di transaminasi epatiche; tuttavia, alcuni pazienti accusano dolenzia al quadrante addominale superiore destro.
L’ittero franco non è comune.
Di solito il danno è reversibile dopo la sospensione dei salicilati.
Comunque, l’uso dei salicilati è controindicato nei pazienti con malattia epatica cronica.
Evidenze considerevoli, come discusso piu avanti, indicano che l’uso dei salicilati è un importante fattore nel danno epatico grave e nell’encefalopatia osservati nella sindrome di Reye.
Effetti urocosurici.
Gli effetti dei salicilati sull’escrezione dell’acido urico dipendono marcatamente dalla dose: basse dosi (1 o è g al giorno) possono diminuire l’escrezione di urato ed elevarne la concentrazione plasmatica; dosi intermedie (2 o 3 g al giorno) di solito non alterano l’escrezione di urato; alte dosi (piu di 5 g al giorno) inducono uricosuria e riducono di livelli plasmatici di urato.
Comunque, talvolta queste dosi elevate sono mal tollerate dal paziente.
Anche piccole dosi di salicilato possono bloccare gli effetti del probenecid e altri agenti uricosurici che diminuiscono il riassorbimento tubulare di acido urico.
Effetti sul sangue.
L’ingestione di aspirina da parte di individui sani prolunga il tempo di sanguinamento.
Per esempio, una singola dose di 325 mg di aspirina raddoppia approssimativamente il tempo medio di sanguinamento dei soggetti normali per un periodo di 4-7 giorni.
Questo effetto e dovuto all’acetilazione irreversibile della ciclossigenasi piastrinica, con conseguente ridotta formazione di TXA2 fino alla produzione di nuove piastrine dai precursori megacariociti.
I pazienti con danno epatico grave, ipoprotrombinemia, deficit di vitamina K o emofilia dovrebbero evitare l’aspirina perché l’inibizione dell’emostasi piastrinica può provocare emorragia.
Se possibile, la terapia con aspirina dovrebbe essere interrotta almeno una settimana prima di un intervento chirurgico.
Molta attenzione va posta anche nell’uso dell’aspirina durante il trattamento a lungo termine con agenti anticoagulanti orali, perché
L’effetto del prolungamento del tempo di sanguinamento si somma alla perdita di sangue dalla mucosa gastrica.
D’altra parte, l’aspirina è ampiamente utilizzata per la profilassi delle malattie tromboemboliche, specialmente della circolazione coronarica e cerebrale, ed è associata frequentemente con anticoagulanti orali nei pazienti con protesi valvolari biologiche o meccaniche.
I salicilati di solito non alterano il numero di leucociti o di piastrine, l’ematocrito o il contenuto di emoglobina.
Comunque, dosi di 3 o 4 g al giorno diminuiscono marcatamente la concentrazione di ferro nel sangue e riducono la sopravvivenza degli eritrociti.
L’aspirina può causare un lieve grado di emolisi negli individui con deficit di glucosio-6-fosfato deidrogenasi. Come gia detto, alte dosi (>3 g/die) possono aumentare il volume del sangue e diminuire l’ematocrito per diluizione.
Effetti sui processi reumatici, infiammatori e immunologici e sul metabolismo del tessuto connettivo.
Sebbene i salicilati sopprimano i segni clinici e spesso migliorino il quadro istologico della febbre reumatica, i danni tissutali, come le lesioni cardiache e il coinvolgimento di altri visceri, non sono influenzati da questa terapia.
In aggiunta all’effetto sulla biosintesi delle prostaglandine, il meccanismo d’azione dei salicilati nella patologia reumatica potrebbe anche comprendere effetti su altri processi cellulari e immunologici nei tessuti mesenchimale e connettivo.
In considerazione della ben nota relazione tra febbre reumatica e processi immunologici, l’attenzione è stata focalizzata sulla capacità dei salicilati di inibire molte reazioni antigene-anticorpo.
Queste capacità includono l’inibizione della produzione di anticorpi, dell’aggregazione antigene-anticorpo e del rilascio di istamina indotto dagli antigeni.
I salicilati inducono anche una stabilizzazione non specifica della permeabilita dei vasi durante l’insulto immunologico.
Le concentrazioni di salicilato necessarie per produrre questi effetti sono elevate e la loro relazione con l’efficacia antireumatica non è chiara.
I salicilati possono anche modificare il metabolismo del tessuto connettivo e questi effetti potrebbero essere coinvolti nella loro azione antinfiammatoria.
Per esempio, i salicilati potrebbero influenzare il consumo, la biosintesi e il metabolismo dei mucopolisaccaridi del tessuto connettivo nella sostanza fondamentale che funge da barriera al diffondersi delle infezioni e dell’infiammazione.
Effetti metabolici
Fosforilazione ossidativa.
Il disaccoppiamento della fosforilazione ossidativa da parte dei salicilati è simile a quello indotto dal 2,4-dinitrofenolo.
L’effetto può avere luogo alle dosi di salicilato usate nel trattamento dell’artrite reumatoide e può portare all’inibizione di numerose reazioni ATP-dipendenti.
Altre conseguenze includono l’incremento indotto dai salicilati della captazione di O2 e della produzione di CO2, la deplezione del glicogeno epatico e l’effetto piretico delle dosi tossiche di salicilati.
A dosi tossiche i salicilati possono diminuire il metabolismo aerobico e aumentare la produzione di acidi organici forti.
Metabolismo dei carboidrati.
Dosi elevate di salicilati possono causare iperglicemia e glicosuria e ridurre notevolmente il glicogeno epatico e muscolare.
Effetti endocrini.
La somministrazione a lungo termine dei salicilati diminuisce la captazione e la clearance di iodio dalla tiroide, ma aumenta il consumo di O2 e la velocità di scomparsa dalla circolazione di tiroxina e trilodotironina.
Questi effetti sono probabilmente causati dallo spiazzamento competitivo, operato dal salicilato, sulla tiroxina e sulla trilodotironina legate alla transtiretina e alla globulina legante la tiroxina nel plasma.
Farmacocinetica dei salicilati
Assorbimento
I salicilati assunti per via orale vengono assorbiti rapidamente, prima dallo stomaco ma, per la maggior parte, dalla porzione superiore dell’intestino tenue.
Concentrazioni apprezzabili sono presenti nel plasma dopo meno di 30 minuti; dopo una singola dose, il picco di concentrazione è raggiunto in circa 1 ora, dopo di che i livelli ematici si riducono gradualmente.
La velocità di assorbimento è determinata da molti fattori, in particolare la velocità di disgregazione e di dissoluzione delle compresse somministrate, il pH a livello della superficie mucosa e il tempo di svuotamento gastrico.
L’assorbimento del salicilato avviene primariamente per diffusione passiva dell’acido salicilico non dissociato o dell’acido acetilsalicilico attraverso le membrane gastrointestinali ed e perciò influenzato dal pH gastrico.
Anche se il salicilato risulta più ionizzato quando il pH è aumentato, un incremento del pH aumenta anche la solubilità del salicilato e quindi la dissoluzione della compressa.
L’effetto complessivo è un aumento dell’assorbimento. Come risultato, vi è solo una trascurabile differenza tra la velocità di assorbimento del salicilato sodico e dell’aspirina rispetto alle numerose preparazioni tamponate dei salicilati.
La presenza di cibo ritarda l’assorbimento dei salicilati. L’assorbimento rettale dei salicilato è di solito più basso di quello orale, oltre a essere incompleto e incostante.
L’acido salicilico è assorbito rapidamente dalla cute intatta, specialmente quando applicato sotto forma di linimenti oleosi o ungenti, e un avvelenamento sistemico si e talvolta verificato in seguito all’applicazione su ampie aeree cutanee.
Anche il metil salicilato è assorbito velocemente quando applicato sulla cute; tuttavia, il suo assorbimento gastrointestinale può essere ritardato di molte ore, il che rende il lavaggio gastrico efficace anche nei casi di avvelenamento a esordio tardivo dopo ingestione orale.
Distribuzione
Dopo l’assorbimento, i salicilati si distribuiscono in molti tessuti dell’organismo e fluidi transcellulari, principalmente mediante processi passivi dipendenti dal pH.
I salicilati sono trasportati attivamente, mediante un sistema saturabile a bassa capacità, al di fuori del liquor attraverso il plesso coroideo.
I farmaci attraversano velocemente la barriera placentare.
II volume di distribuzione delle dosi usuali di aspirina e sodio salicilato nei soggetti normali è mediamente intorno ai 170 ml/kg di peso corporeo; alle alte dosi terapeutiche, questo volume aumenta fino a circa 500 ml/kg a causa della saturazione dei siti di legame sulle proteine plasmatiche.
L’aspirina ingerita è assorbita mediamente come tale, ma una parte entra nel circolo sistemico come acido salicilico dopo l’idrolisi da parte di esterasi della mucosa gastrointestinale e del fegato.
L’aspirina può essere rilevata nel plasma solo per un breve periodo, come risultato dell’idrolisi nel plasma, nel fegato e negli eritroci; per esempio, 30 minuti dopo una dose di 0,65 g, solo il 27% del salicilato totale nel plasma è nella forma acetilata.
Anche il metil salicilato viene idrolizzato rapidamente ad acido salicilico, principalmente nel fegato.
Approssimativamente l’80-90% del salicilato plasmatico è legato alle proteine, in modo particolare all’albumina, alle concentrazioni usate in clinica; la parte legata si riduce con l’aumentare delle concentrazioni plasmatiche.
L’ipoalbuminemia, che si può instaurare per esempio nell’artrite reumatoide, è associata a un più alto livello di salicilato libero nel plasma.
Il salicilato compete con molti composti per i siti di legame sulle proteine plasmatiche; questi includono la tiroxina, la trilodotironina, la penicillina, la fenitorna, il sulfinpirazone, la bilirubina, l’acido urico e altri FANS come il naprossene.
L’aspirina è legata in misura più limitata; comunque, essa acetila l’albumina umana plasmatica in vivo mediante reazione con l’amino-gruppo ε della lisina e può modificare il legame all’albumina di altri farmaci.
L’aspirina acetila anche gli ormoni, il DNA, l’emoglobina e altre proteine.
Biotrasformazione ed escrezione
La biotrasformazione dei salicilati avviene in molti tessuti, ma in modo particolare nel reticolo endoplasmatico e nei mitocondri epatici.
I tre prodotti metabolici principali sono l’acido salicilurico (coniugato alla glicina), il glucuronide etere o fenolico e l’estere o acilglucuronide.
In aggiunta, una piccola frazione viene ossidata ad acido gentisico (acido 2,5-dildrossibenzoico) e negli acidi 2,3-dildrossibenzoico e 2,3,5-trildrossibenzoico; viene anche prodotto l’acido gentisurico, il coniugato della glicina all’acido gentisurico.
I salicilati sono escreti nelle urine come acido salicilico libero (10%), acido salicilurico (75%), glucuronidi salicilici fenolici (10%) e acilici (5%) e acido gentisico (meno dell’ 1%).
Comunque, l’escrezione dei salicilati liberi è estremamente variabile e dipende dalla dose e dal pH delle urine.
Nelle urine alcaline piu del 30% del farmaco ingerito può essere eliminato come salicilato libero, mentre nelle urine acide i livelli scendono fino al 2%.
L’emivita plasmatica dell’aspirina è di circa 20 minuti e quella dei salicilati è di è o 3 ore alle dosi antipiastriniche, raggiungendo le 12 ore alle classiche dosi antinfiammatorie.
L’emivita del salicilato può raggiungere le l5-30 ore alle dosi terapeutiche elevate o in caso di intossicazione.
Questa eliminazione dose-dipendente è il risultato di una limitata capacità del fegato di formare acido salicilurico e glucuronide fenolico, il che comporta che una più elevata percentuale del farmaco immodificato venga escreto nelle urine alle dosi piu alte.
Rapporto tra concentrazione del salicilato nel plasma, effetti terapeutici e collaterali e tossicità.
L’aspirina è uno dei FANS per i quali il salicilato plasmatico può rappresentare un indice per monitorare la terapia e la tossicità.
Dosi intermittenti analgesiche-antipiretiche di aspirina producono tipicamente livelli di aspirina nel plasma inferiori a 20 mcg/ml e livelli plasmatici di salicilato inferiori a 60 mcg/ml.
La somministrazione giornaliera di dosi antilnfiammatorie di 4 o 5 g di aspirina produce livelli di salicilati plasmatici nell’ordine di 120-350 mcg/ml.
Per ottenere effetti ottimali nei pazienti con malattia reumatica sono richieste concentrazioni plasmatiche di salicilato pari a 150-300 mcg/ml.
Effetti collaterali significativi possono essere rilevati in presenza di livelli superiori a 300 mcg/ml.
Generalmente l’iperventilazione si instaura a concentrazioni superiori a 350 mcg/ml e altri segni di intossicazione, come l’acidosi, a concentrazioni superiori ai 460 mcg/ml.
Nella fascia piu bassa di concentrazioni, la clearance del farmaco è all’incirca costante (nonostante il fatto che la saturazione della capacità metabolica venga avvicinata) perché la frazione di farmaco libero, e quindi disponibile per il metabolismo o l’escrezione, aumenta mano a mano che i siti di legame sulle proteine plasmatiche vengono saturati.
La concentrazione totale di salicilato nel plasma è quindi una funzione relativamente lineare della dose alle concentrazioni più basse.
Alle concentrazioni piu alte, tuttavia, poiche le vie metaboliche di eliminazione sono saturate, piccoli incrementi della dose possono aumentare in maniera sproporzionata la concentrazione di salicilato nel plasma.
La mancata prevenzione di questo fenomeno può portare a tossicità.
Poiché l’intervallo di concentrazioni plasmatiche di salicilato necessario per l’efficacia ottimale si può sovrapporre a quello in cui si osserva il tinnito o acufene, è importante individualizzare le dosi antinfiammatorie di aspirina.
Il tinnito può essere un indice reale di eccesso di concentrazione plasmatica nei pazienti con udito normale, ma non è un indicatore preciso nei pazienti con ipoacusia preesistente; quindi, il controllo di questo sintomo non sostituisce il monitoraggio periodico dei livelli di salicilato nel plasma.
La concentrazione di salicilato nel plasma è aumentata nelle condizioni che portano a riduzione della velocità di filtrazione glomerulare o della secrezione tubulare prossimale dei salicilati, come le nefropatie, o in presenza di inibitori che competono per il sistema di trasporto (per es., probenecid).
Cambiamenti del pH urinario hanno anch’essi effetti significativi sull’escrezione del salicilato.
Per esempio, l’eliminazione del salicilato è circa quattro volte migliore a pH 8 che a pH 6, ed è ben al di sopra della velocita di filtrazione glomerulare a pH 8.
Alte velocità di flusso urinario diminuiscono il riassorbimento tubulare, mentre i’opposto si osserva nell’oliguria.
I coniugati dell’acido salicilico con glicina e acido glucuronico non retrodiffondono subito attraverso le cellule tubulari renali.
La loro escrezione, perciò, avviene attraverso filtrazione glomeruiare e secrezione tubulare prossimale, ma non è dipendente dal pH.
Usi terapeutici dei salicilati
Utilizzo sistemico
Le due preparazioni più utilizzate di salicilato per via sistemica sono l’aspirina (acido acetilsailcilico) e il sodio salicilato.
La dose di salicilato dipende daila malattia ehe si intende trattare.
Altri salicilati disponibili per l’uso sistemieo sono il salsalato (acido salicilsalicilico), il quale viene idrolizzato ad acido salicilico durante e dopo i’assorbimento, il sodio tiosalicilato (per iniezione), la colina salicilato (liquido per via oraie) e il magnesio salicilato (compresse).
È anche disponibile una combinazione di colina e magnesio sailcilato (colina magnesio, trisalicilato).
Antipiresi
La terapia antipiretica è riservata ai pazienti nei quali la febbre può essere di per se deleteria e a quelli che sperimentano un notevole sollievo quando la febbre si abbassa.
Poco è conosciuto circa la relazione tra febbre e cinetica temporale dei processi infiammatorio e immune; può essere, a volte, un processo fisiologico protettivo.
Il decorso della malattia può essere reso di difficile interpretazione dal sollievo dei sintomi e dalla riduzione della febbre mediante l’uso di farmaci antipiretici.
La dose antipiretica di salicilato per gli adulti varia da 325 mg a 650 mg per via orale ogni 4 ore.
I salicilati sono controindicati per la febbre associata a infezione virale nei bambini; per le eziologie non virali, 50-75 mg/kg al giorno vengono somministrati in quattro o sei dosi, fino a un massimo giornaliero di 3,6 g.
La via di somministrazione orale è quella piu usata; la somministrazione parenterale (di sodio tiosalicilato) è raramente necessaria.
La somministrazione rettaie di supposte di aspirina può essere necessaria nei bambini o quando la via orale non sia accessibile.
Analgesia
I salicilati sono farmaci vaildi per il sollievo non specifico del dolore di entità lieve-moderata (per es., emicrania, artrite, dismenorrea, nevralgia e mialgia).
A questo scopo essi sono prescritti alle stesse dosi e con le medesime modalità utilizzate nella terapia antipiretica.
Artrite reumatoide
Sebbene l’aspirina sia considerata come il composto standard con il quale gli altri farmaci dovrebbero essere paragonati per il trattamento dell’artrite reumatoide, molti clinici favoriscono l’uso di altri FANS ritenuti meno gastrolesivi, anche se questa opinione non è stata ancora avvalorata da studi clinici convincenti.
Come per i FANS, la terapia con salicilati produce un’analgesia adeguata a permettere movimenti più efficaci e una terapia fisica nell’osteoartrite e nell’artrite reumatoide.
In aggiunta, la terapia con aspirina è associata ad aumento dell’appetito, sensazione di benessere e riduzione dell’infiammazione nei tessuti articolari e nelle strutture circostanti.
I pazienti con malattia progressiva o resistente richiedono una terapia con farmaci di seconda scelta e più tossici, come gli antimalarici, la penicillamina, i glucocorticoidi, il metotrexato o agenti immunosoppressori.
Negli Stati Uniti il metotrexato è il farmaco di seconda scelta usato piu frequentemente, mentre in Europa è generalmente preferita la sulfasalazina.
Interazioni farmacologiche
La concentrazione plasmatica di salicilati generalmente è poco influenzata da altri farmaci, ma la somministrazione simultanea di aspirina abbassa le concentrazioni di indometacina, naprossene, chetoprofene e fenoprofene, almeno in parte a causa dello spiazzamento dalle proteine plasmatiche.
Interazioni importanti dell’aspirina con il warfarin, le sulfoniluree e il metotrexato sono già state discusse. Altre interazioni dell’aspirina includono l’antagonismo della natriuresi indotta dallo spironolattone e il blocco del trasporto attivo della penicillina dal liquor al sangue.
Utilizzo locale
La mesalazina (acido 5-aminosalicilico) è un salicilato che viene usato per i suoi effetti locali nel trattamento delle malattie infiammatorie intestinali.
Il farmaco non è efficace per via orale perché è poco assorbito e viene inattivato prima che raggiunga l’intestino terminale.
Attualmente è disponibile in supposte e come sospensione rettale per clistere per il trattamento delle proctosigmoiditi lievi e moderate: è in commercio anche una supposta per il trattamento della colite ulcerosa distale, della proctosigmoidite e della proctite.
Due formulazioni che rilasciano il farmaco nell’intestino terminale, l’olsalazina (sodio azodisalicilato, un dimero del 5-aminosalicilato legato mediante un legame —N=N—) e la mesalamina formulata in una preparazione orale ricoperta con un polimero sensibile al pH e in compresse a rilascio controllato, sono efficaci nel trattamento della malattia infiammatoria intestinale, in particolare la colite ulcerosa.
La sulfasalazina (salicilazosulfipiridina) contiene mesalamina legata covalentemente alla sulfapiridina; è scarsamente assorbita dopo somministrazione orale, ma è scissa nella sua componente attiva dai batteri del colon.
Il farmaco è utile nel trattamento delle malattie infiammatorie intestinali, principalmente per l’azione locale della mesalamina.
La sulfasalazina e l’olsalazina sono anche state utilizzate nel trattamento dell’artrite reumatoide e della spondilite anchilosante.
Salicilati e gravidanza.
Non vi sono evidenze che indichino che dosi terapeutiche di salicilati siano teratogene nell’essere umano; comunque, i bambini nati da donne che hanno fatto uso di salicilati per lunghi periodi possono presentare una significativa riduzione del peso alla nascita.
Quando questi farmaci vengono assunti durante il terzo trimestre, si osservano anche aumento della mortalità perinatale, anemia, emorragia pnma e dopo il parto, gestazione prolungata e conseguenti complicanze; quindi, l’uso di questi composti durante tale periodo dovrebbe essere evitato.
Come già detto, la somministrazione di FANS durante il terzo trimestre di gravidanza può anche causare la chiusura prematura del dotto arterioso.
L’uso di aspirina e stato suggerito da alcuni autori per il trattamento delle donne ad alto rischio di preeclampsia, ma si è stimato che è richiesto il trattamento di 90 donne per prevenire un solo caso di preeclampsia (Villar et al., 2004).
Effetti irritanti locali.
L’acido salicilico è irritante per la cute e per le mucose e distrugge le cellule epiteliali.
L’azione cheratolitica dell’acido libero è utilizzata per il trattamento topico di verruche, calli, infezioni fungine e alcuni tipi di dermatiti eczematose.
Dopo il trattamento con acido salicilico, le cellule del tessuto si rigonfiano, si ammorbidiscono e vanno incontro a desquamazione.
II metil-salicilato è irritante per la cute e per la mucosa gastrica ed è utilizzato per lenire il dolore muscoscheletrico di grado lieve.
Tossicità ed effetti collaterali dei salicilati
L’avvelenamento da salicilato o gravi intossicazioni si verificano spesso nei bambini e a volte sono fatali.
Questi farmaci non vanno considerati come rimedi domestici innocui, e l’intossicazione da salicilato dovrebbe essere presa in considerazione in tutti bambini in coma, con convulsioni o collasso cardiovascolare.
La dose fatale varia a seconda della preparazione del salicilato.
Decessi si sono verificati dopo l’assunzione di 10-30 g di sodio salicilato o aspirina in soggetti adulti, ma quantità più elevate (130 g di aspirina in un caso) sono state ingerite senza che ciò portasse all’exitus.
La dose letale del metil salicilato (olio di betulla dolce, olio di gaultheria, olio di betulla) è considerevolmente piu bassa di quella del sodio salicilato.
Meno di 4 ml (4.7 g) di metil salicilato possono essere fatali nei bambini.
I sintomi di avvelenamento da metil salicilato differiscono poco da quelli descritti piu avanti per l’aspirina.
La stimolazione centrale, l’iperpnea intensa e l’iperpiressia rappresentano le caratteristiche principali.
L’odore del farmaco può essere percepito facilmente nell’alito, nel vomito e nelle urine.
L’avvelenamento da acido salicilico si differenzia solo per la prevalenza dei sintomi gastrointestinali dovuti alla marcata irritazione locale.
Salicilismo.
La lieve intossicazione cronica da salicilato è chiamata salicilismo.
Quando è pienamente sviluppata, la sindrome comprende cefalea, vertigini, tinnito, ipoacusia, visione oscurata, confusione mentale, stanchezza, sonnolenza, ipersudorazione, sete, iperventilazione, nausea, vomito e occasionalmente diarrea.
Effetti neurologici.
Ad alte dosi i salicilati hanno effetti tossici sul SNC , che consistono in stimolazione (incluse le convulsioni) seguita da depressione.
Possono manifestarsi confusione, vertigini, tinnito, sordità per i toni alti, delirium, psicosi, stupor e coma.
Il tinnito e la perdita di udito dovuti ad avvelenamento da salicilato sono causati dall’aumentata pressione labirintica o dall’effetto sulle cellule ciliate della coclea, forse secondariamente alla vasocostrizione nella microcircolazione del sistema uditivo.
Il tinnito si osserva tipicamente a concentrazioni plasmatiche di salicilato di 200-450 pg/ml e vi e una stretta relazione tra l’estensione della perdita di udito e la concentrazione di salicilato nel plasma.
Occasionalmente un paziente può avvertire il tinnito a piu basse concentrazioni plasmatiche di salicilato.
Generalmente il tinnito si risolve entro 2 o 3 giorni dalla sospensione del farmaco.
I salicilati causano nausea e vomito, indotti dalla stimolazione di strutture che sono accessibili al liquor, probabilmente la zona bulbare chemorecettoriale.
Nell’uomo la nausea e il vomito indotti centralmente compaiono generalmente a concentrazioni plasmatiche di salicilato di circa 270 pg/ml, ma questi stessi effetti possono verificarsi in presenza di livelli plasmatici molto piu bassi, come risultato di un’irritazione gastrica locale.
Effetti sulla respirazione.
Gli effetti respiratori dei salicilati contribuiscono ai gravi disturbi dell’equilibrio acido-base che caratterizzano l’avvelenamento da parte di questa classe di composti.
I salicilati stimolano la respirazione direttamente e indirettamente.
Il disaccoppiamento della fosforilazione ossidativa porta a un’aumentata produzione periferica di CO2 e all’incremento compensatorio del volume minuto, di solito senza un cambiamento globale della PCO2.
Il disaccoppiamento della fosforilazione ossidativa conduce anche a un’eccessiva produzione di calore e la tossicità da salicilato è associata a ipertermia, particolarmente nei bambini.
I salicilati stimolano direttamente il centro respiratorio del bulbo.
Ciò da luogo a un aumento della profondità del respiro e a un pronunciato incremento della frequenza respiratoria.
I pazienti con avvelenamento da salicilato possono presentare un incremento importante del volume respiratorio al minuto e, di conseguenza, alcalosi respiratoria.
Questo può essere osservato in presenza di concentrazioni plasmatiche di salicilato di 350 pg/ml, mentre una marcata iperventilazione si verifica quando i livelli si avvicinano ai 500 pg/ml.
Comunque, se la tossicità da salicilato si associa alla co-somministrazione di barbiturici od oppiodi, la depressione centrale del respiro previene l’iperventilazione e il disaccoppiamento della fosforilazione ossidativa indotta dal salicilato determina un marcato aumento della PCO2 nel plasma e acidosi respiratoria.
L’esposizione prolungata ad alte dosi di salicilati porta a depressione bulbare, con depressione centrale del respiro e collasso circolatorio dovuto a depressione vasomotoria.
Poiché l’aumentata produzione di CO2 continua, ne consegue acidosi respiratoria. L’insufficienza respiratoria e la comune causa di morte nei casi fatali di avvelenamento da salicilato.
Equilibrio acido-base ed elettroliti.
Come descritto precedentemente, dosi terapeutiche elevate di salicilato sono associate ad alcalosi respiratoria primaria e ad acidosi renale compensatoria.
Cambiamenti successivi dello stato acido-base generalmente avvengono solo quando dosi tossiche di salicilati sono ingerite da lattanti e bambini oppure, occasionalmente, dopo l’assunzione di dosi elevate negli adulti.
La fase dell’alcalosi respiratoria primaria raramente è riconosciuta nei bambini con intossicazione da salicilato.
Essi presentano di solito uno stato congiunto di acidosi respiratoria e renale, caratterizzato da una diminuzione del pH ematico, da una bassa concentrazione di bicarbonato nel plasma e da una PCO2 plasmatica normale o pressoché normale.
La depressione diretta della respirazione indotta dal salicilato previene l’adeguata iperventilazione respiratoria per soddisfare l’incrementata produzione periferica di CO2.
Di conseguenza, la PCO2 plasmatica aumenta e il pH del sangue diminuisce. Poiché la concentrazione plasmatica di bicarbonato è gia bassa a causa dell’aumentata escrezione renale, lo stato acido-base in questo stadio è essenzialmente costituito da un’acidosi respiratoria scompensata.
Vi si sovrappone, comunque, un’acidosi metabolica reale causata dall’accumulo di acidi come conseguenza di tre processi.
- Primo: concentrazioni tossiche di salicilati spiazzano da 2 a 3 mEq per litro di bicarbonato plasmatico.
- Secondo: la depressione vasomotoria causata da dosi tossiche di salicilati compromette la funzionalita renale, con conseguente accumulo di acidi solforico e fosforico.
- Terzo: i salicilati a dosi tossiche possono diminuire il metabolismo aerobico come conseguenza dell’inibizione di svariati enzimi (questo squilibrio del metabolismo dei carboidrati porta all’accumulo di acidi organici, specialmente piruvico, lattico e acetacetico.
La medesima serie di eventi causa anche alterazioni dell’equilibrio idro-elettrolitico.
La bassa PCO2 plasmatica porta a una diminuzione del riassorbimento tubulare renale di bicarbonato e aumenta l’escrezione renale di Na+, K+ e acqua.
L’acqua viene persa anche a causa della sudorazione indotta dal salicilato (specialmente in presenza di febbre) e dell’iperventilazione; la disidratazione, che può essere marcata soprattutto nei bambini, si sviluppa rapidamente.
Poiché con la sudorazione viene persa attraverso i polmoni una maggiore quantità di acqua che di elettroliti, la disidratazione si associa a iperazotemia.
Prolungate esposizioni ad alte dosi di salicilato causano anche una deplezione di K+ dovuta a fattori sia renali che extrarenali.
Effetti cardiovascolari
Dosi tossiche di salicilati portano a un aumento incontrollato delle risposte cardiovascolari sfavorevoli che si osservano in seguito alla somministrazione di alte dosi terapeutiche e allo sviluppo di una paralisi vasomotoria centrale.
Si possono osservare petecchie a causa di un difetto della funzionalità piastrinica.
Effetti metabolici.
Metabolismo dei carboidrati.
Elevate dosi di salicilati possono causare iperglicemia e glicosuria e condurre a deplezione del glicogeno contenuto nei muscoli e nel fegato; questi effetti sono in parte spiegati dalla liberazione di adrenalina.
Tali dosi riducono anche il metabolismo aerobico del glucosio, aumentano l’attività della glucosio-6-fosfatasi e stimolano la secrezione di glucocorticoidi.
Nei bambini vi è un rischio maggiore di ipoglicemia con conseguenti danni cerebrali permanenti.
Metabolismo dell’azoto.
I salicilati, a dosi tossiche, conducono a un significativo bilancio negativo dell’azoto, caratterizzato da aminoaciduria.
L’attivazione corticosurrenale può contribuire allo sbilanciamento negativo dell’azoto aumentando il catabolismo proteico.
Metabolismo dei grassi.
I salicilati riducono la lipogenesi bloccando parzialmente l’incorporazione dell’acetato negli acidi grassi; essi inibiscono anche la lipolisi stimolata dall’adrenalina e spiazzano gli acidi grassi a catena lunga dal sito di legame con le proteine plasmatiche.
La combinazione di questi effetti porta a un aumento della captazione e dell’ossidazione degli acidi grassi nei muscoli, nel fegato e in altri tessuti, nonché a una diminuzione delle concentrazioni plasmatiche di acidi grassi liberi, fosfolipidi e colesterolo; aumenta anche l’ossidazione dei corpi chetonici.
Effetti endocrini.
Dosi molto elevate di salicilati stimolano la secrezione di steroidi da parte della corticale del surrene mediante un effetto sull’ipotalamo e aumentano temporaneamente le concentrazioni plasmatiche di corticosteroidi liberi, spiazzandoli dalle proteine del plasma.
Gli effetti terapeutici dei salicilati non dipendono da queste azioni.
Trattamento del sovradosaggio da salicilati
Terapia
L’avvelenamento da salicilati rappresenta un’emergenza medica acuta e la morte può sopraggiungere nonostante tutti gli sforzi.
Il monitoraggio dei livelli di salicilati rappresenta un’utile guida per il trattamento, ma devono essere valutate anche le condizioni cliniche generali del paziente, l’equilibrio acido-base, il tipo di formulazione di salicilato assunto, il momento dell’assunzione e la dose.<
Non vi sono antidoti specifici per l’avvelenamento da salicilati. Il trattamento inizia con una rapida valutazione, seguita dall’approccio A (airway, vie aeree), B (breathing, respirazione), C (circolazione), D (decontaminazione) tipico delle emergenze mediche.
Vie aeree.
Data la necessità dell’alcalosi respiratoria per compensare l’acidosi metabolica causata dai salicilati, l’intubazione deve essere evitata sino a quando il paziente non presenta ipoventilazione od ottundimento mentale.
Respirazione.
L’impiego di composti paralizzanti e la difficoltà nel raggiungere gli alti valori di volume minuto necessari tendono a indurre acidosi respiratoria.
L’aspirina (pKa = 3.5) diventa non ionizzata a pH acido e attraversa la barriera ematoencefalica più facilmente, aumentando i suoi effetti tossici a livello centrale.
È il livello tessutale, più che quello plasmatico, a essere pericoloso per il paziente.
L’edema polmonare non cardiogeno interferisce con l’ossigenazione del paziente e possono essere necessarie elevate concentrazioni di ossigeno inspirato.
Circolazione.
L’avvelenamento da aspirina porta a una vasodilatazione inappropriata con deplezione di volume e acidosi, che potenziano la vasodilatazione.
Si deve procedere al ripristino del volume plasmatico mediante liquidi per via endovenosa.
Lo scopo è raggiungere una diuresi sostenuta per eliminare i salicilati. Se necessario, possono essere somministrati agenti vasocostrittori (per es., noradrenalina, fenilefrina).
Decontaminazione
Il carbone attivo viene utilizzato per impedire un ulteriore assorbimento di salicilati nel tratto gastrointestinale.
Questo risulta di particolare importanza quando siano state ingerite forrnulazioni di aspirina rivestite, con assorbimento ritardato.
È opportuno somministrate bicarbonato di sodio per mantenere il pH tra 7.5 e 7.55 e, se possibile, il pH urinario al di sopra di 8.
La diuresi alcalina forzata aumenta al massimo l’eliminazione dei salicilati.
Se queste misure si rivelano inefficaci, può essere necessaria l’emodialisi, a cui si ricorre anche qualora si osservi un peggioramento clinico nonostante la terapia, oppure se i livelli plasmatici di salicilato risultano superiori a 1000 μ/ml.
I salicilati, il glucosio, il pH e il potassio ematici devono essere dosati frequentemente e la terapia va modificata di conseguenza.
Può verificarsi una diminuzione dei livelli di glucosio nel SNC nonostante la presenza di livelli plasmatici normali, quindi, va somministrato glucosio in caso di alterato stato mentale, indipendentemente dai livelli di glucosio plasmatici.

