Vaniglia
Tratto da “Piante Medicinali – Chimica, Farmacologia e Terapa” di R. Benigni, C. Capra e P.F.Cattorini
(Vanilla planifolia Andrews – Fam. Orchidacee/Monandree/Neottiee) (Sin. – Epidendron vanilla L. – Vanilla aromatica Swartz. – Vanilla fragrans Salisb. – Vanilla mexicana Mill.)
Vaniglia- Ultimo aggiornamento pagina: 27/02/2018
Indice dei contenuti
- Generalità
- Componenti principali
- Proprietà farmacologiche
- Estratti e preparati vari
- Preparazioni usuali e Formule
- Bibliografia
Generalità

Etimologia – Vanilla dallo spagnolo vaina = guaina, diminutivo vainilla = piccola guaina, piccolo baccello, baccello sottile.
planifolia, per le foglie quasi piane, carnose.
Epidendron, dal greco epi = sopra, su e dendron = albero, cioè sopra gli alberi, perchè pianta epifita, rampicante a mezzo di radici avventizie.
aromatica e fragrans, per il caratteristico profumo.
Nomi volgari – Tlilxochitl (Messico).
Vanille (fr.), Vanille (ted.), vanelloes, vanilla (ingl.), vainilla (spagn.), vanilha (port.). baunilha (brasil.), vanìl (russo).
Habitat – Originaria del Messico, spontanea epifita sul Myrtus pimenta L. il c.d. Pepe garofanato (regioni calde del Basso Messico ed ivi coltivata) (Vera Cruz). America tropicale, Antille, Colombia, Perù, Venezuela. Coltivata nelle regioni tropicali (Tahiti, Madagascar, Reunion (Bourbon), Mauritius, Seychelles, Giava, Ceylon).
Arbusto sarmentoso, epifita.
Parti usate – I frutti (cassule, dette stecche e, impropriamente, baccelli), colti prima della maturazione.
Componenti principali
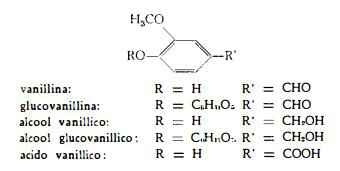
Nei frutti freschi, privi di odore, non si trova vaniglina; vi sono stati identificati invece tre glucosidi, l’uno, glucovanillina, producente per idrolisi glucosio e vaniglina, un secondo, alcool glucovanillico, scindibile per idrolisi in glucosio e alcool vanillico, il quale per ossidazione dà vaniglina, infine un terzo glucoside non definito, idrolizzabile con formazione di un etere profumato (1).
Dai frutti freschi, non profumati, dopo speciali manipolazioni, che favoriscono la formazione delle sostanze odorose, si ottengono i frutti di Vaniglia del commercio, che si presentano coperti di minuti cristalli di vaniglina.
Vaniglina o vanillina, C8H8O3, molto diffusa in natura, specialmente come prodotto secondario, derivante dall’idrolisi di glucosidi o dall’ossidazione di altri componenti (2), fu trovata per la prima volta come essudato cristallino dei frutti della Vaniglia (3). E’ stata successivamente preparata dalla coniferina da Tiemann e Haarmann (4) ed identificata all’etere metilico dell’aldeide 3-metossi-4-ossibenzoica (aldeide protocatechica). Due forme cristalline di vaniglina — aghi con p.f. 77-9° e cristalli tetragonali, p.f. 81-2° —sono state riconosciute presenti nell’essudato dei frutti (5).
Glucovanillina (vanilloside), C14H18O8, preparata in un primo tempo per ossidazione della coniferina (6), è stata poi trovata anche nei frutti verdi di Vaniglia (7). E’ stata denominata anche vanilloside da Goris (7).
Alcool glucovanillico (vanilloloside) C14H20O8, ottenuto dapprima come derivato della glucovanillina (8) ed identificato come glucoside dell’alcool vanillico C8H10O3, è stato in seguito riconosciuto come componente dei frutti verdi di Vaniglia (1) (7).
Acido vanillico. C8H8O4, preparato per la prima volta dalla coniferina
(4), fu poi trovato anche nei frutti della Vaniglia (8a).
Nei frutti della Vaniglia sono stati inoltre identificati i seguenti componenti:
— p-ossibenzaldeide (13), acido salicilico, probabilmente anche alcool coniferilico (8a), resine 8-14%, pectine 0,5-1,4%, zuccheri sino a 18%, grasso sino al 14,7%, acqua sino al 20,7% (14), enzimi: un’ossidasi ed un’idrolasi (15).
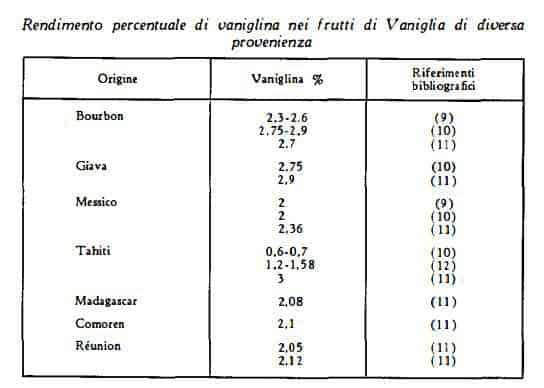
In base ai dati ricavati da numerose analisi Pritzker e Jungkunz (9) hanno stabilito i seguenti valori analitici, quale criterio di giudizio dei frutti di Vaniglia: acqua contenuto massimo 35%, ceneri totali al massimo 7 % e ceneri solubili in acido al massimo 0,5 % nella sostanza secca, vaniglina almeno 2%: non si deve trovare amido.
Dalla Vaniglia di Tahiti è stato estratto olio etereo 0,08% contenente principalmente alcool anisico, inoltre aldeide anisica, acido anisico (16) e piperonale (17).
Nella Vaniglia di Bourbon non sono stati trovati né alcool anisico, né aldeide anisica (12) e neppure piperonale, il quale è pure assente nella Vaniglia del Messico, di Giava e del Sud-America (17).
Le aldeidi negli estratti di Vaniglia subiscono processi di ossidazione e si trasformano negli acidi corrispondenti, come è stato dimostrato con analisi cromatografiche (18).
Proprietà farmacologiche ed impiego terapeutico
La Vaniglia venne introdotta in Europa dopo la conquista spagnola del Messico e dalla Spagna il suo uso venne poi propagato in Francia, in Inghilterra e negli altri paesi europei. Nel 1721 venne inscritta nella Farmacopea inglese.
La Vaniglia ha proprietà stimolanti e può essere impiegata, sola o associata ad altre droghe, nell’inappetenza e nell’atonia gastrointestinale. Oggi è quasi esclusivamente usata come aromatizzante in pasticceria, in liquoreria, in profumeria e, nella tecnica galenica, per la correzione e l’aromatizzazione di preparati a base di estratti di Boldo, di Cacao, di Caffè, di Camomilla, di Cannella, di Cola, di Genziana, di Rabarbaro, di sostanze amare, dolci, piccanti, inodori ed insipide e, inoltre, per l’aromatizzazione dell’olio di paraffina e dell’olio di Ricino (19). Entra nella composizione dell’elisir di Garus e di numerose altre preparazioni.
Per gli stessi scopi la Vaniglia viene spesso sostituita con la vaniglina sintetica, meno costosa ma sebbene il test del Federal food and Drug Administration indichi che il potere aromatizzante di una parte di Vaniglia corrisponde approssimativamente a quello di 0,07 parti di vaniglina, questa non ha lo stesso profumo della Vaniglia (20).
Secondo Brun (21) la Vaniglia, pur non essendo veramente dannosa, è dotata di una tossicità non del tutto trascurabile. Layet (22) ha descritto alcuni casi di vanillismo manifestatisi in operai addetti alla lavorazione della droga, con sintomi di eruzioni papulose, edemi della faccia e delle mani, con forte prurito e desquamazione forforacea, cefalgie, vertigini e irritazione genito-urinaria (23-24).
La tossicità della vaniglina non è elevata e, in considerazione delle dosi alle quali viene usualmente impiegata, essa può essere ritenuta del tutto trascurabile.
Secondo Preusse (25) la somministrazione di 2 g di vaniglina, in una sola dose al coniglio, non determina effetti tossici, ma dosi ripetute provocano perdita dell’appetito, diminuzione del peso, atonia muscolare e morte per coma.
La dose tossica di vaniglina nei ratti albini, è stata trovata da Dison (26), pari a g 1,5/kg per via endovenosa.
Deichmann e Kitzmiller (27) hanno determinato la d.l.m. per la vaniglina e per l’etilvaniglina nel coniglio ed hanno trovato che essa corrisponde a g 3/kg per os sia per l’una che per l’altra. La d.l. 50 nei ratti, per via sottocutanea, è pari a g 2,6/kg per la vaniglina e a g 2/kg per la etilvaniglina.
La dose mortale delle due sostanze induce negli animali, aumento della frequenza respiratoria, astenia muscolare, lacrimazione, dispnea, collasso, coma e morte.
Dosi subletali determinano la stessa sintomatologia, sebbene più attenuata e rapidamente reversibile.
La somministrazione di 20 mg/kg di vaniglina e di etilvaniglina nei ratti, per un periodo superiore ai 120 giorni, è risultata innocua. Dosi superiori provocano nei ratti e nei conigli, alterazioni istopatologiche di varia gravità, a carico del miocardio, dei reni, del fegato, dei polmoni, della milza e dello stomaco.
Questi composti possono determinare, secondo gli AA., avvelenamenti anche mortali nell’uomo, ma la loro relativa insolubilità in acqua fredda o nel latte e il sapore amaro degli estratti concentrati di Vaniglia, rendono molto rara la possibilità di gravi intossicazioni.
Concentrazioni superiori a g 0,5 di vaniglina o di g 0,15 di etilvaniglina per quarto di gallone (rispettivamente, g 0,37 e 0,11 per litro) negli alimenti, non producono, secondo Deichmann e Kitzmiller, effetti dannosi anche per somministrazione prolungata.
La massima parte di vaniglina viene ossidata nell’organismo, ad acido vanillico che viene eliminato con le urine sotto forma di un prodotto solfoconiugato. Tracce di vaniglina e di acido vanillico vengono eliminate come tali [Preusse (25)].
Secondo Caujolle e Meynier (28), l’impiego della vaniglina e della etilvaniglina sintetiche, in sostituzione della vaniglina naturale e degli estratti di Vaniglia non offre alcun inconveniente a condizione che i prodotti industriali vengano accuratamente purificati al fine di allontanare le impurezze rappresentate da sostanze più tossiche, quali le ortovanilline e le m-aldeidi.
Alla Vaniglia viene attribuita anche un’azione coleretica. Tale azione, già segnalata da Vinke e Nerer (29) nel 1938, venne successivamente confermata da Mercier e coll. (30), i quali trovarono che tale azione si ottiene sia per somministrazione orale che parenterale del sale sodico della vaniglina.
L’effetto coleretico è più marcato con l’omovaniglina, la quale si è dimostrata due volte più attiva della vaniglina e indipendentemente dalla via di somministrazione.
Nel cane in anestesia cloralosica o con dial, l’omovaniglina è capace di raddoppiare ed anche di triplicare, la secrezione biliare durante l’ora seguente la somministrazione.
Interessanti per la loro azione coleretica, sono alcuni altri derivati di sintesi della vaniglina, studiati da diversi autori.
Dubois e coll. (31) hanno studiato l’attività del divallidene cicloesanone e trovarono che oltre un’azione coleretica, questa sostanza può manifestare, sebbene non così costantemente, anche un’attività colecistocinetica, attività che venne successivamente confermata dal La Barre (32).
L’isovaniglina e l’etilisovaniglina sono state studiate da Caujolle e coll. (33) i quali hanno constatato che queste sostanze sono dotate di un’azione coleretica pronta, potente e prolungata.
L’attività coleretica dell’isovaniglina e della etilisovaniglina è superiore, rispettivamente, a quella della vaniglina e a quella della etilvaniglina e l’attività dell’etilisovaniglina è nettamente superiore a quella dell’isovaniglina e ciò, sia per quanto riguarda l’intensità che la durata d’azione.
L’interesse farmacologico di questo fatto, sarebbe tanto più grande, secondo gli AA., in quanto i derivati isovanillinici sono meno tossici dei derivati vanillinici omologhi.
Nella serie vanillinica esisterebbe dunque, secondo gli AA., una netta relazione fra struttura e azione coleretica: tale attività è più elevata allorché il gruppo aldeidico si trova in posizione meta rispetto al gruppo fenolico libero.
Verrebbero così estese a questi gruppi di composti, le osservazioni fatte da Chabrol e coll. (34-36), relativamente agli acidi fenolici.
Secondo Cima e Fassina (37) la vanillina e i suoi derivati, sono dotati di una notevole attività spasmolitica sugli organi a muscolatura liscia, attività cui gli AA. attribuiscono l’azione dell’alburno di Tiglio.
Estratti e preparati vari
a) Tintura di vaniglia alcool-idrosolubile al 10% di droga
b) Tintura vaniglia al 10% di droga.
Preparazioni usuali e formule galeniche
Sciroppo
Tintura vaniglia alcool idrosolubile……….. g 5
Sciroppo semplice F.U…………………………. g 95
Pozione stimolante aromatica
Tintura vaniglia
Tintura cannella…………….. ana g 10
Vino di Malaga g 100
Sciroppo corteccia arancio …….. g 50
(Gilbert e Michel)
(da consumarsi a più riprese).
BIBLIOGRAFIA
(1) GORIS, Compt. rend., 279, 70, 1924 – (2) SALGUES B. R., ibtd., 241, 987, 1955 – (3) GOBLEY, J. Pharnu. 34, 401, 1858 – (4) TIEMANN F. c HAARMANN W„ Ber.. ?, 608 c 613, 1874; «. 509, 1875; 9, 1287, 1876 . (5) VIOLANDA A. T., Philippirte Agr,. 37, 507, 1954; Chem. Abs.. 49, 7808, 1955 – (6) HAARMANN W. c REIMER K., Ber.. 17, 392, 1884; TIEMANN F., Ber., 18, 1595, 1885 – (7) GORIS A., Chem. Abs., 41. 7681, 1947 – (8) TIEMANN F., Ber., 18, 1595, 1885 – (8a) ANWAR M. H., AnalyL Chem.. 35. 1976, 1963 . (9) PRITZKER e JUNGKUNZ, ZeUschr. Untersuch. Lebensm., 55, 424, 1928 – (IO) DOHERTY, J.Proc. R. Sci. N.S.fV,. 57, 696, 1920 – (11) AMORETH, Profum. Italie., 2, 251, 1924 –
(12) GAUTIER c KLING, Ann. Falsific., 3. 200, 1910 – (13) STOLL S. c BOUTERVILLE Y., Ann. de falsile, et fraudes, 47, 183, 1954; Chem. Abs., 48, 13171 f, 1954 – (14) WEHMER C., Die Pflanzenstoffe, Il Cd., p. 189 – (15) LECOMTE, Compì, rend.. 133. 745, 1901 – (16) WALBAUM, WaUach-Fcstschrift, Gòttingcn 1909, 649 – (17) GNADINGER, J. Ind. Engin. Chem.. 18, 588, 1926 – (18) STOLL S. c PRAT Y., Ann, fats. et expert. chim., 53, 316. 1960 • (19) CAPRA C., Il Farmaco, ed. prat.. 13, 499, 1958 • (20) OSOL-FARRAR, Dispensatory o( U.S.A. 25* ed. Lippincott Comp. Philadelphla – Montreal 1955, p. 1481 – (21) BRUN P., Précis de Matièrc Médicalc, G. Doln e C. Ed., Paris, 1936, p. 103 – (22) LAYET, cit. da BRUN P. tbid. • (23) BRETIN Ph., De rorigine végétale des ceitaines dermites, Lyon 1909, cit. da BRUN P. Ibid. – (24) PLANCHON L. e BRETIN Ph., Précis ‘de Matière Médicale, Norbert Maloin Ed, Paris 1928, cit. da BRUN P. ibid. – (25) PREUSSE C, Z. physioL Chem., 4. 209, 1880 – (26) DISON G. M., Perfum. Essent. OH Record, 22, 4, 1931 – (27) DEICHMANN W. E. e KITZMILLER V., J.A.Ph.A., 29, 425, 1940 – (28) CAUJOLLE F. e MEYNIER D., Soc. Méd. Chir. et Pharm. de Toulouse, 30 marzo 1954; Presse Méd.. 62. 790, 1954 – (29) VINKE E. e NERER H. E., Arch. exp. Path. u. Pharmakor, 190. 733, 1938 – (30) MERCIER F., DETRIE J. c SESTIER M. R., Bull. Soc. Pharm. Marseille, p. 39, 1952; Ann. pharm. /ranf.. 10. 155, 1952 – (31) DUBOIS CH., VANLERENBERGER J. e VANLERENBERGER- ROTRU F., C. R. Soc. Biol.. 143, 1210, 1949 – (32) LA BARRE M., Thérapie. 10, 960, 1955 – (33) CAUJOLLE F., MEYNIER D. c GOUT R., Ann. pharm. /ranf., 14. 456, 1956 – (34) CHABROL E., CHARONNAT R-, MAXIMIN M. e BOQUETIN A., C. R. Soc. Biol., 103, 3, 1930 – (35) CHABROL E., CHARONNAT R., MAXIMIN M. e WAITZ R., ibid., 105, 439, 1930 – (36) CHABROL E., CHARONNAT R., MAXIMIN M. c WAITZ R., ibid., 107, 1240, 1931 – (37) CIMA L. e FASSINA G., Arch. il. sci. farm. 11. 288, 1961.

